Обзор фармакологических особенностей интерфероновых препаратов в условиях потенциального риска 3-й волны пандемии инфекции COVID-19
Известно, что в процессе биологической эволюции природа наградила организм человека великолепным механизмом противостояния вирусным атакам, который реализован в системе цитокиновых белков – интерферонов…
Эра интерферонов началась в 1957 году, когда англичанин Айзекс и швейцарец Линдеман во время экспериментальных опытов открыли явление вирусной интерференции: зараженные вирусами клетки производили особый белок, который ингибировал рост этих вирусов и защищал интактные клетки от вирусной агрессии. С этого времени человечество вступило в эру интерферона, иными словами приобрело мощное естественное средство в борьбе с вирусными инфекциями. Уже в 1961 году английский вирусолог Тирелл впервые испытал на себе и своих сотрудниках интраназальный интерферон. И что поразительно, предварительное закапывание в нос раствора интерферона и последующее заражение вирусом Коксаки вызвало лишь легкое недомогание, но никак не заболевание, без всяких побочных явлений 2.
Уже через 5 лет после открытия, ВОЗ определила интерферон как «белок, способный препятствовать заражению здоровых/незараженных клеток». В международной классификации лекарственных средств интерферону альфа-2b, который используется в большинстве препаратов на основе интерферона присвоен код L03AB05 [5].
В настоящее время в мировой научной медико-биологической литературе наблюдается настоящий «бум» публикаций, посвященных терапевтическим возможностям интерферонов при лечении инфекции COVID-19. Так, например китайские авторы лечили COVID-19 либо распыленным препаратом интерферона-а2в, либо комбинацией его в сочетании с умифеновиром (Арбидол). Данная терапия значительно сокращала продолжительность обнаруживаемого вируса в верхних дыхательных путях и параллельно снижала продолжительность повышенного уровня в крови маркеров воспаления, в частности IL-6 [6].
Также в Китае, авторы, на основе национальных рекомендаций по лечению COVID-19 рекомендуют вводить пациентам вводить 5 млн. МЕ интерферона-α путем вдыхания паров два раза в день в комбинации с рибавирином [7].
Американские исследователи доказали, что EC50 (полумаксимальная эффективная концентрация) при лечении вирусной инфекции, вызываемой вирусом SARS-CoV-2 интерфероном-α составляет 1,35 МЕ/мл [8].
Комбинация препарата интерферона I типа с лопинавиром/ритонавиром, рибавирином или ремдесивиром может повысить его эффективность, поскольку эффективность таких комбинаций наблюдается in vitro и у других коронавирусов [10].
В ряде обзорных и проблемных статей 2020 года, иностранные авторы приводят убедительные доказательства необходимости и целесообразности применения препаратов интерферона при терапии COVID-19.
Таким образом, на сегодняшний день можно с уверенностью сказать, что интерферонотерапия новой коронавирусной инфекции заняла прочное место в арсенале клиницистов многих стран мира [11,12].
Более того, Временные методические рекомендации Минздрава России «Профилактика, диагностика и лечение новой коронавирусной инфекции COVID-19» (Версия 10 от 08.02.2021) рекомендуют использовать препараты интерферона- α в свечах, особенно с антиоксидантами.
Важно иметь ввиду, что в инструкциях всех рассматриваемых противовирусных препаратов есть показания – ОРВИ. Как известно, инфекция COVID-19 также является по сути ОРВИ, поэтому применение данных препаратов против коронавирусных агентов этио-патогенетически оправдано.
Препарат обладает иммуномодулирующим, противовоспалительным и противовирусным действием, применяется в схемах лечении ОРВИ и COVID-19 [15].
Препарат ВИФЕРОН обладает выраженными противовирусными и иммуномодулирующими свойствами, а витамины С и Е в его составе обеспечивают антиоксидантный, противовоспалительный, мембраностимулирующий и регенеративный эффекты. Препарат в указанных лекарственных формах практически лишен побочных эффектов и может применятся у детей с первых дней жизни, беременных и пациентов различных возрастных категорий [17].
Анализируя эффективность тех или иных интерфероновых препаратов, следует отметить, что выбор лекарственной формы имеет важное значение. Так, исследованиями, проведенными учеными МГУ было доказано, что действующее вещество в гелевых субстанциях и композициях фармакологических препаратов, легко преодолевают эпителиальные барьеры слизистых оболочек, поскольку обладая гидрофильными свойствами, гелевая лекарственная форма выделяет действующее вещество из своей композиции в течение 5 часов [18].
Учитывая риск наступления 3-й волны пандемии, представляется целесообразным применение препаратов интерферонового ряда в качестве средств активной профилактики инфекции COVID-19.
Интерферон человеческий лейкоцитарный : инструкция по применению
Состав
Препарат представляет собой группу белков (интерфероны альфа), синтезированных лейкоцитами здоровых доноров, в ответ на воздействие вируса-индуктора интерферона (вирус болезни Ньюкасла или вирус Сендай). Препарат не содержит консервантов и антибиотиков. Поверхностный антиген вируса гепатита В и антитела к ВИЧ 1, ВИЧ 2, вирусу гепатита С отсутствуют.
Описание
Пористая аморфная масса или порошок белого или от светло-желтого до розового цвета, гигроскопичен.
Фармакотерапевтическая группа
Интерфероны. Интерферон альфа естественный. Код ATX: [L03AB01].
Интерферон альфа обладает способностью стимулировать фагоцитарную активность макрофагов, а также цитотоксическую активность Т-клеток и NK-клеток, оказывает непрямое противовирусное действие, индуцируя в клетках состояние резистентности к вирусным инфекциям и модулируя ответную реакцию иммунной системы, направленную на нейтрализацию вирусов или уничтожение инфицированных ими клеток.
Интерферон быстро всасывается через слизистые оболочки. Из организма выводится в виде естественных метаболитов.
Показания к применению
Профилактика и лечение гриппа и других острых респираторных вирусных инфекций.
Противопоказания
Повышенная чувствительность к препаратам белкового происхождения.
Способ применения и дозы
Препарат применяют путем закапывания (с помощью медицинской пипетки или шприца без иглы) или распыления. Распыление производится распылителями любой системы или с помощью прилагаемой насадки-распылителя.
Для профилактики введение препарата следует начинать при непосредственной угрозе заражения и продолжать до тех пор, пока опасность заражения сохраняется. Препарат применяют интраназально путем закапывания по 5 капель или распыления по 0,25 мл в каждый носовой ход 2 раза в сутки с интервалом не менее 6 часов.
Для лечения препарат применяют на ранней стадии заболевания при появлении первых клинических симптомов интраназально по 0,25 мл (5 капель) в каждый носовой ход через 1-2 ч не менее 5 раз в сутки. Эффективность препарата тем выше, чем раньше начато его применение.
Правила применения насадки-распылителя:
Надеть иглу на шприц, наполнить его растворенным препаратом в объеме 0,25 мл (отметка 10 по шкале 40 ед. или отметка 25 по шкале 100 ед.).
Снять иглу и плотно надеть насадку-распылитель.
Поднести вплотную к носовому ходу насадку-распылитель и резким нажатием на поршень шприца впрыснуть препарат в носовой ход.
Снять насадку-распылитель, надеть иглу и набрать в шприц 0,25 мл препарата из ампулы.
Снять иглу, снова плотно надеть насадку-распылитель и ввести препарат в другой носовой ход в соответствии с пунктом 3.
Насадку-распылитель вводят на глубину 0,5 см в носовые ходы, предварительно очищенные от слизи. Пациент при этом должен находиться в сидячем положении со слегка запрокинутой головой и оставаться в этом положении в течение 1 минуты после введения препарата. Допускается использование одной насадки только у одного пациента.
Введение препарата путем инъекций категорически запрещается.
Применять с осторожностью лицам с аллергическими заболеваниями.
Применение в педиатрии
Детям с неонатального периода (с рождения) препарат применяется путем распыления и закапывания.
Применение в период беременности и лактации
Данных по опыту применения у беременных нет. Поэтому препарат применяют по назначению врача с учетом соотношения ожидаемой пользы для матери и возможного риска для плода и ребенка.
В период лактации ограничений по применению нет.
Особенности влияния лекарственного средства на способность управлять транспортным средством и потенциально опасными механизмами
Особенности влияния лекарственного средства у лиц с нарушением функции печени и почек и в геронтологической практике
Не выявлено особенностей применения лекарственного препарата у лиц с нарушением функции печени и почек. Не выявлено особенностей применения в геронтологической практике
Побочное действие
Аллергические реакции. Если Вы заметили любые побочные эффекты, не указанные в инструкции, сообщите об этом врачу. При аллергических реакциях немедленного типа проводить симптоматическую терапию.
Передозировка
Случаи передозировки не описаны.
Взаимодействие с другими лекарственными средствами
Применяют в комплексной терапии с другими лекарственными средствами. Допускается использовать одновременно с другими противовирусными и сосудосуживающими средствами для местного применения.
Условия хранения
Хранить при температуре от 2 до 8 °C в защищенном от света и недоступном для детей месте.
Срок годности
2 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускается без рецепта.
ФГУП «НПО «Микроген» Минздрава России
Россия, 450014, Республика Башкортостан, г. Уфа, ул. Новороссийская, д. 105, тел.: (347) 229-92-01.
Cобственный интерферон —
лучший из возможных
Как организм вырабатывает интерферон. Эффективность естественных интерферонов для иммунитета. Бактериальные лизаты как естественный активатор иммунной системы и стимуляции собственного интерферона.
Человек борется с вирусами с незапамятных времен. За миллионы лет эволюции наш организм выработал универсальную стратегию борьбы с неприятелем. Одним из ключевых игроков этого противостояния являются интерфероны. Это вещества, помогающие организму в короткий срок справиться с вирусами. Сегодня существует большое количество препаратов, содержащих в своем составе те или иные интерфероны. Но так ли они эффективны как собственный интерферон, вырабатываемый организмом?
Что такое интерферон?
В настоящее время известно более 20 интерферонов, которые подразделяются на три типа 3,4 :
Как работают собственные интерфероны человека?
Противовирусные свойства интерферонов вызывали у исследователей большой интерес с точки зрения терапии ряда заболеваний. И со временем благодаря различным медицинским и технологическим возможностям удалось получить лекарственные препараты, которые содержат в своем составе интерферон.
Использование препаратов интерферона в медицине
Препараты интерферона активно используются в лечении широкого спектра вирусных заболеваний. В частности, речь идет о вирусе папилломы человека, вирусных гепатитах, герпетической инфекции, а также гриппа и простудных заболеваний. Важным фактором выбора препаратов, содержащих интерферон для лечения того или иного заболевания, будет являться концентрация интерферона в препарате, то, каким способом он получен и какой тип интерферона (α, β, γ или λ) содержит в своем составе. Несмотря на то, что существуют препараты интерферона, которые отпускаются без рецепта, все же с врачом лучше заранее проконсультироваться, поскольку в отношении этих препаратов есть ряд противопоказаний. По способу получения препараты интерферона можно поделить на 4 типа 6,7 :
Преимущества и недостатки привнесенных интерферонов
К преимуществам препаратов, содержащих в своем составе интерфероны, можно отнести их доступность. Немаловажное преимущество интерферонов – возможное их применение против широкого спектра вирусов.
Сравнительно высокий уровень безопасности препаратов интерферона позволяет их применять и детям, которые, как известно, часто болеют гриппом и другими ОРВИ.
Экстренная иммунозащита от вирусов
Наш организм в процессе эволюции приспособился к борьбе с вирусами, однако при необходимости мы можем ему помочь, не сильно вмешиваясь в его работу.
Интерферонотерапия, применение в клинике и перспективы развития
Интерфероны (IFNs) были впервые описаны в 1957 г. Исааком и Линдеманом как противовирусные соединения, вырабатываемые организмом. С тех самых пор было описано множество свойств этих цитокинов, а изучение их многогранных эффектов на функции клеток и всего организма продолжаются и по сей день. Влияние интерферонов на иммуный ответ позволяет использовать их в качестве терапевтических агентов. Учитывая разнонаправленные эффекты IFNs, сформировались несколько различных направлений в их клиническом применении, а также много методик находится в стадии разработки.
Общее описание интерферонов
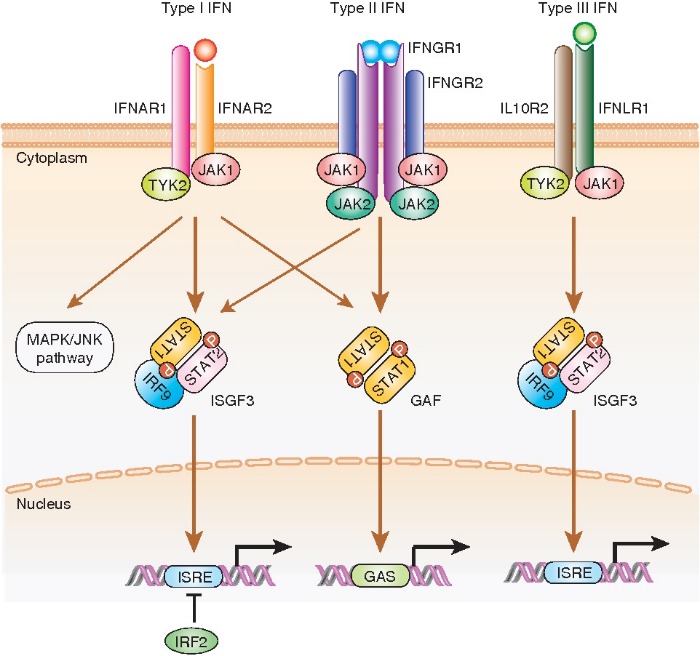
В настоящий момент описано 3 класса интерферонов: IFN-I, IFN-II, IFN-III. Первый класс интерферонов (IFN-I) является самым большим: в него входят IFN-α, IFN-β, IFN-ε, IFN-κ и IFN-ω. IFN-α у человека содержит 13 подтипов, все остальные члены класса представлены по одному экземпляру. Все IFN-I передают сигнал через гетеродимерный рецепторный комплекс, состоящий из IFNAR1 и IFNAR2 субъединиц. Эти субъединицы экспрессируются на большинстве клеток организма, что позволяет IFN-I воздействовать на множество клеточных линий. Однако различные типы IFN-I по-разному экспрессируются в тканях и различаются аффинностью связывания с рецепторным комплексом, а следовательно различные подтипы проявляют неодинаковое действие. Связывание IFN-I с рецепторным комплексом активирует фосфорилирование рецептор-зависимых членов семейства JAK-киназ: JAK1 (Janus kinase I) и TYK2 (тирозинкиназа 2). Далее происходит активация сигнальных преобразователей и активаторов транскрипции STAT1 и STAT2. К их гетеродимеру присоединяется IRF9 с образованием комплекса ISGF3 (интерферон-стимулированный эффекторный фактор 3), который транслоцируется в ядро, где вызывает экспрессию интерферон-стимулированных генов (ISG) посредством связывания с элементом ISRE на целевых промоторах. Таким образом, активируется экспрессия множества генов, имеющих данный элемент в промоторе. Этим и объясняется наличие большого количества разных свойств интерферонов.
Единственным представителем класса IFN-II является IFN-γ. Он связывается с субъединицами IFNGR1 и IFNGR2, которые также присутствуют на большинстве типов клеток. Затем происходит связывание еще одного комплекса IFN-γ-IFNGR1-IFNGR2, что активирует передачу. Происходит фосфорилирование JAK1 и JAK2; дальнейшая активация STAT1 и образование гомодимеров STAT1. Димеризованный STAT1 перемещается в ядро, где связывает последовательность GAS в IFN-γ-индуцибельными генами и активирует их транскрипцию.
Последним классом является IFN-III, открытый относительно недавно. В него входят IFN-λ1 (IL-29), IFN-λ2 (IL28A), IFN-λ3 (IL-28B) и IFN-λ4. Сигнал от IFN-λ проводится через рецептор, состоящий из субъединиц IFNλR1 и IL-10R2. Экспрессия этого рецепторного комплекса ограничена эпителиальными клетками, что снижает системное действие IFN-III, однако и уменьшает их побочные эффекты при клиническом использовании. Дальнейший сигнальный путь JAK-STAT не отличается от такового у IFN-I.
Все интерфероны имеют многогранные эффекты, включая противовирусный, иммуномодулирующий, противоопухолевый. Иммуномодулирующий эффект проявляется как иммуностимулирующим действием, так и иммуноподавляющим. Результирующий эффект зависит от многих факторов и заслуживает отдельного обзора. Противоопухолевый эффект представлен влиянием IFNs как на сами опухолевые клетки (антипролиферативный), так и на микроокружение опухоли (ангиостатический, иммуностимулирующий). Однако это свойство тоже непостоянно, и интерфероны также могут способствовать прогрессии опухоли. Поэтому клиническое использование IFNs, как правило, должно быть комплексным, для поддержания нужных и нивелирования нежелательных свойств этих цитокинов. Различия в генах, стимулированных IFN-I и IFN-II классов, а также разную экспрессию рецепторов IFN-I и IFN-III классов, дают обоснования для дифференцированного клинического применения различных видов интерферонов.
Применение IFN-I
IFN-I первыми начали применять в клинической практике и на данном этапе они больше других классов интегрированы в практическую медицину.
Противовирусное действие
IFN-I обладают выраженным противовирусным эффектом. Совокупность ISG способна влиять на каждый этап жизненного цикла вируса: проникновение в клетку, трансляцию и репликацию вируса, а также выход из клетки. На каждый этап существует множество различных механизмов, которые могут как влиять непосредственно на различные компоненты вируса, так и изменять состояние зараженной клетки, например, метаболизм. В настоящее время IFN-I в качестве противовирусного средства применяются для терапии вирусных гепатитов В (HBV) и С (HCV), а также в качестве этиотропной терапии саркомы Капоши, вызванной человеческим герпес вирусом-8 (HHV-8).
В терапии гепатита С используются комбинации IFN-α с другими противовирусными, например, нуклеозидами (рибаварин), или используют их модифицированную форму, представляющую коньюгат с полиэтиленгликолем — пегинтерферон. Это позволяет уменьшить его почечный клиренс и значительно увеличить период его полувыведения примерно с 5 до практически 90 часов. При комбинированной терапии с рибавирином или применением пегинтерферона более 75 % пациентов с HCV не 1 генотипа (nongenotype 1 HCV) поддерживают устойчивый ответ против HCV, в то время как до 50 % пациентов, инфицированных генотипом 1 HCV, реагируют на это комбинированное лечение.
В настоящее время хронический гепатит В лечат комбинацией пегинтерферона и одного из нескольких нуклеотидных препаратов, которые ингибируют репликацию генома HBV (ламивудин, адефовир, энтекавир или тенофовир). При терапии пегинтерфероном с ламивудином около 60 % пациентов демонстрируют значительный противовирусный ответ, который более эффективен, чем при монотерапии данными препаратами.
Поскольку саркома Капоши вызвана вирусом, было логично попытаться лечить ее с помощью IFN-α. Это лечение может быть местным или системным. Уровень успеха приближается к 60 %, когда терапия IFN-α сочетается с эффективным антиретровирусным лечением. Некоторые вирус-ассоциированные опухоли также поддаются данной терапии. К ним относятся рецидивирующий респираторный папилломатоз и генитальные бородавки.
Противовирусная терапия интерфероном не лишена недостатков. В первую очередь, многие вирусы имеют механизмы, противостоящие IFNs, и такая устойчивость совершенствуется. Поэтому лучшее понимание функций ISG может привести к разработке новых терапевтических средств. К примеру, идет разработка и использование новых химерных IFNs и IFN-подобных молекул, влияющих на определенные ISG. Это позволит минимизировать побочные эффекты, в то же время обеспечивая мощное противовирусное действие. Также возможно использование активации отдельных компонентов сигнального пути IFN.
Противоопухолевое действие
IFN-I проявляют противоопухолевое действие как напрямую, индуцируя повреждения и апоптоз опухолевых клеток, так и стимулируя иммунитет организма на борьбу с опухолью. Показано также, что успех химиотерапевтических средств, таргетных противоопухолевых агентов, лучевой терапии и иммунотерапии зависит от сигнализации IFN типа I. В мышиных моделях рака при нейтрализации IFNAR1 моноклональными антителами отменяется терапевтический эффект моноклональных антител против рецептора 2 эпидермального фактора роста человека (ERBB2). Эффективность химиотерапии на основе антрациклинов против трансплантированных опухолей у мышей также теряется при совместном введении IFNAR1-нейтрализующих моноклональных антител. Показано, что противоопухолевые эффекты облучения теряются у специальной линии мышей с выключенным Ifnar1-геном. Имиквимод — синтетический агонист TLR7 и TLR8, который местно применяется для лечения рака кожи, способствует IFNAR1-зависимому перемещению pDC в опухолевое окружение. Отсутствие Tlr7 или Ifnar1 отменяет терапевтическую активность имиквимода у мышей, несущих меланомы, что коррелирует с уменьшенной экспрессией цитотоксических молекул путем инфильтрации опухоли pDCs. IFN типа I могут участвовать в терапевтической активности блокаторов контрольных точек. Так синергические противоопухолевые эффекты, достигаемые одновременной блокадой CTLA4 и PD-лиганда 1 у мышей с меланомой были потеряны при нарушении стимуляции IFN-I. Пегилированный IFNα-2b используется для лечения резецированной меланомы II и III стадий. Гепатоцеллюлярная карцинома, ассоциированная с HBV, также может лечится с применением IFN-α. Пегилированный IFN-α в сочетании с мультикиназным ингибитором иматинибом может увеличить реакцию на терапию у пациентов с хроническим миелоидным лейкозом (ХМЛ). Более того, лечение пегилированным IFN-α после отмены иматиниба вызывает устойчивую ремиссию у большинства пациентов с ХМЛ. Важно отметить, что у таких пациентов более высокие пропорции циркулирующих CD4+ эффекторных Т-клеток памяти с улучшенной секреторной способностью и центральных CD8+ клеток памяти, чем у здоровых индивидуумов. Перспективные результаты уже получены у пациентов с острым миелоидным лейкозом, хроническим лимфоцитарным лейкозом, первичной кожной лимфомой, рецидивирующей фолликулярной лимфомой, системным мастоцитозом, полицитемией vera, карциномой предстательной железы, устойчивой к кастрации, и тестикулярной тератомой.
Несмотря на важное значение IFN-I для противоопухолевого иммунитета, системная терапия IFN-I не является универсальной. Такая терапия, как было показано, может применяться не для всех типов рака. К тому же, IFN-I обладают и иммуносупрессивными свойствами (например, увеличением производства противовоспалительных IL-10 и IL-27 или индуцированием экспрессии иммунодепрессантного фермента (IDO1) индоламина 2,3-диоксигеназы 1), а его системное введение сопровождается побочными эффектами, такими как повышенная утомляемость, анорексия, гепатотоксичность, гриппоподобный синдром и тяжелая депрессия. По этим причинам ведется активная работа по модификации IFN-I. Так был произведен ряд работ по улучшению доставки IFN-I в микроокружение опухоли. Одним из таких методов является конъюгация интерферона-I с моноклональными антителами. Такие молекулы получили название иммуноцитокины. Иммуноцитокин C22b2b, содержащий тетрамер IFNα-2b, связанный с hL243 (человеческое моноклональное антитело к HLA-DR), показал эффективность против миеломы человека и ксенотрансплантатов лимфомы. IFNβ, конъюгированный с цетуксимабом (клинически одобренным EGFR-нацеливающим моноклональным антителом), ограничивает рост экспрессирующих EGFR опухолей мыши, которые не реагируют на немодифицированный цетуксим. Также конъюгаты IFNα или IFNβ со специфическим моноклональным антителом HER2 более эффективны против HER2-экспрессирующих опухолей, чем немодифицированное моноклональное антитело. Другой подход представляет собой генную модификацию различных клеток таким образом, чтобы усиленно производить IFN-I. NK-клетки, генетически сконструированные для экспрессии человеческого IFNα, улучшили цитотоксичность против клеток гепатоцеллюлярной карциномы in vitro, а также в ксенотрансплантантных моделях опухолей. Мезенхимальные стволовые клетки, модифицированные для экспрессии мышиного IFN, эффективно останавливают рост меланомы, зависимым от Т-клеток и NK-клеток способом. Также практикуется введение индукторов IFN-I в опухоль. 5′-трифосфатные РНК (ppp-РНК) способны стимулировать RIG-I, что приводит к инициированию гибели раковых клеток, а также к получению IFN типа I и других факторов, способствующих врожденному иммунитету. Предпринимаются также попытки генерации новых мультиплексоров CpG-олигодезоксинуклеотидов (ODN) в качестве нанокристаллов, поскольку эти структуры сильно стимулируют продукцию IFNα плазмоцитоидными дендритными клетками и вызывают активные противоопухолевые иммунные ответы. Местное введение полиинозино-полицитиловой кислоты (полиI: С), которая является агонистом TLR3, RIG-I может стимулировать IFNAR1, что приводит к миграции иммунных клеток к неопластическим очагам, индуцируя терапевтически значимые реакции в доклинических моделях меланомы.
Иммуномодулирующее действие
Как было уже упомянуто, IFN-I имеют противовоспалительные и иммуносупрессирующие эффекты. На данном этапе в клинической практике только IFN-β нашел применение в качестве иммуномодулирующего агента. Речь идет о терапии аутоиммунного заболевания — рассеянного склероза (РС). Исследования показали, что внутримышечное лечение IFN-β приводит к снижению годовых рецидивов РС. Добавление натализумаба, рекомбинантного моноклонального антитела к интегринам, увеличивает способность IFN-β подавлять скорость прогрессирования РС. Однако это не единственный случай, к которому может быть применен IFN-I в контексте иммуномодулятора. Мыши с дефицитом рецептора IFN типа I сверхчувствительны к колиту, в моделях этого заболевания, что указывает на то, что IFN типа I играют роль в кишечном гомеостазе. В одном небольшом исследовании большинство пациентов с неспецифическим язвенным колитом (НЯК), которые систематически получали интерферон-β-a1, показали снижение проявления болезни (в качестве клинической меры было использовано ректальное кровотечение). Однако другие исследования не смогли показать терапевтический эффект от IFN-I у пациентов с НЯК, что обосновывает необходимость дальнейшего исследования роли IFN-I в кишечном гомеостазе. Также IFNs подавляют образование остеокластов, клеток, ответственных за эрозию костей. Исследования показали, что образование остеокластов усиливается во время коллаген-индуцированного артрита у мышей с инактивированным IFN-β. Таким образом, IFNs, в частности IFN-β, очевидно, обладают способностью улучшать патологическую резорбцию кости, хотя данное свойство требует всестороннего изучения перед введением в клиническую практику.
Применение IFN-II
IFN-γ является сильным активатором иммунного ответа, одновременно поляризуя его по направлению клеточного иммунного ответа. Он участвует в образовании Th1, активирует фагоцитарное звено иммунитета, усиливает окислительный метаболизм тканевых макрофагов, антителозависимую клеточную цитотоксичность (АЗЦТК) и активность естественных киллеров (NK-клеток).
Клиническое применение
В настоящее время IFN-γ применяется в практической медицине в двух случаях: терапия злокачественного остеопетроза и хронической гранулематозной болезни. Злокачественный остеопетроз — врожденное заболевание с дефектом работы остеокластов, из-за чего страдает физиологическая резорбция кости. В результате увеличения костной массы и уменьшения полости костного мозга возникает тромбоцитопения, анемия и инфекционные осложнения, что обычно приводит к смерти в течение первого десятилетия жизни. Использование IFN-γ эффективно: было отмечено 96 % снижение частоты инфекций. Было обнаружено также, что IFN-γ увеличивает костную резорбцию и улучшает кроветворение. Другая патология — хроническая гранулематозная болезнь — также является наследственной. Наблюдается дефект в продукции фагоцитами бактерицидных супероксидных анионов, что приводит к рецидивирующим опасным для жизни бактериальным и грибковым инфекциям. IFN-γ вызывал 67 % снижение относительного риска серьезных инфекций и двукратное сокращение числа первичных серьезных инфекций по сравнению с группой плацебо. Более того, продолжительность госпитализации была значительно меньше для всех клинических случаев в группе IFN-γ.
IFN-γ-1b также рассматривается как привлекательный вариант терапии пациентов с рефрактерным туберкулезом легких с множественной лекарственной устойчивостью. Аэрозольная форма IFN-γ-1b была признана хорошо переносимой и полезной в качестве адъюванта у пациентов с туберкулезом с множественной лекарственной устойчивостью. Аналогичные результаты из другого исследования, в котором IFN-γ-1b вводили подкожным путем, были обнадеживающими.
Противоопухолевая активность
Практическое применение IFN-γ на данном этапе связано в основном с его противоинфекционной активностью. Однако IFN-γ был рассмотрен и в иных областях, к примеру, в онкологии. Недавно некоторые исследования показали, что активация иммунной системы необходима для эффективной лучевой терапии, а IFNγ играет ключевую роль в эффективности терапии ионизирующим излучением. В мышиной модели рака толстой кишки ионизирующая лучевая терапия не влияет на рост опухоли у мышей с инактивированным IFN-γ, но уменьшает опухолевую нагрузку у интактных мышей. Было выяснено, что IFN-γ уменьшает рост опухолевых клеток путем индукции остановки опухолевого клеточного цикла, апоптоза и некроптоза. Более того, в клеточных линиях колоректального рака IFN-γ выявляет апоптоз путем индукции митохондриальных активных форм кислорода, которые зависят от активации цитозольной фосфолипазы A2. Также IFN-γ способен воздействовать на строму опухоли: он вызывает регресс сосудистой сети опухоли, что приводит к снижению кровотока и последующему коллапсу опухолей. Это напоминает ишемический некроз в отличие от геморрагического некроза, индуцированного TNF-α. Среди иммунных клеток IFN-γ активирует антигенпредставляющие клетки для усиления экспрессии цитокинов (IL-12 и IL-18) и костимулирующих молекул CD86, которые усиливают дифференцировку Th1 и цитотоксическую функцию Т-лимфоцитов (CTL). Сигналы IFN-γ также способствуют устранению опухоли путем ингибирования функций некоторых супрессивных иммунных клеток в опухолях, таких как регуляторные CD4+ Т-клетки (Tregs), миелоидные супрессорные клетки (MDSCs) и связанные с опухолью макрофаги (ТАМ). Список противоопухолевых эффектов обширен, однако есть обстоятельства, мешающие активному клиническому применению IFN-γ в противоопухолевой терапии. Дело в том, что IFN-γ обладает также свойствами, поддерживающими опухолевую прогрессию. К примеру, IFN-γ может вызывать экспрессию iNOS (синтаза оксида азота) в моноцитарных MDSC-полученных макрофагах. iNOS играет ключевую роль в усилении супрессивной активности моноцитарных MDSC и, в свою очередь, уменьшает противоопухолевые Т-клеточные ответы. Индуцированные IFN-γ клетки меланомы экспрессируют ген CTLA-4 человека, который зависит от сигнальных путей IFNGR/STAT1. IFN-γ также индуцирует эпителиально-мезенхимальный переход (EMT) в клетках папиллярного рака щитовидной железы человека (PTC) и увеличивает миграционное и инвазивное поведение клеток PTC. Таким образом, необходимы специальные стратегии лечения, в которых IFN-γ комбинируется с другим средством для снижения подобных эффектов интерферона. Было продемонстрировано, что обработка IFN-γ может побуждать большую часть клеточных линий выражать высокие уровни поверхностного супрессивного PD-L1. Однако обработка IFN-γ клеток опухоли желудка с последующим применением антител к PD-L1 приводит к усилению противоопухолевой CTL-активности. Еще одна перспективная стратегия была указана в исследовательских работах. Обработка клеток аденокарциномы легких с помощью IFN-γ привела к активации путей JAK2-STAT1 и PI3K-AKT. Активация JAK2-STAT1 способствует антипролиферативному эффекту IFN-γ, в то время как активация PI3K-ACT индуцирует экспрессию PD-L1 и снижает его антипролиферативный эффект. Поэтому предполагается, что блокада PI3K может максимизировать опосредованный IFN-γ противоопухолевый эффект. Противоопухолевая активность IFN-γ была продемонстрирована в терапии рака яичников в сочетании с циклофосфамидом и цисплатином, что значительно продлевает выживаемость без прогрессирования. Кроме того, до настоящего времени существует 8 текущих клинических испытаний с участием только IFN-γ или в сочетании с другими противоопухолевыми препаратами. Но в настоящее время, несмотря на то, что IFN-γ имеет ключевое значение для иммунотерапии рака, этот цитокин не был одобрен для лечения пациентов с различными типами рака. Дальнейшее изучение свойств IFN-γ, может привести к появлению новых стратегий терапии рака, поэтому это направление весьма перспективно.
Иммуномодулирующее действие
Применение IFN-III
IFN-λ были открыты сравнительно недавно, поэтому в клинической практике они в настоящее время не используются. Однако, согласно последним исследованием, IFN-λ имеют большой потенциал в практическом применении. Несмотря на то, что сигнальные пути IFN-III соответствуют сигнальным путям IFN-I, существуют различия в их функциональной активности. IFN-λ запускает слабый, но устойчивый ответ ISG; наоборот, IFN-α создает сильный кинетический профиль экспрессии генов, который быстро развивается и подавляется. Различия в локализации рецепторов также дифференцируют ответы IFN-I и III классов.
Противовирусная активность
IFN-λ являются доминирующим классом интерферона, продуцируемым в печени человека и шимпанзе, при инфицировании HCV, при этом IFN-λ ингибирует репликацию HBV. В экспериментах с кишечной ротавирусной инфекцией показано, что IFN-λ необходим для контроля инфекции, но не IFN-I. Сообщается, что IFN-λ способствует устойчивости к гриппу A, гриппу B, SARS, коронавирусу и H1N1 у мышей. IFNs-λ способны ингибировать репликацию нескольких других вирусов, включая ВИЧ, вирус простого герпеса типа 2 (HSV 2), цитомегаловирус (CMV) и вирус энцефаломиокардита (EMCV). Эти данные свидетельствуют о перспективности IFN-λ в противовирусной терапии. Также вследствии ограниченой экспрессии их рецепторов, IFN-III будут иметь меньше системных реакций, чем IFN-I. PEGIFN-λ1 был исследован в клинических испытаниях против HCV; успешное испытание II фазы
продемонстрировало, что IFN-λ1 был столь же эффективным (или несколько более) как PEGIFN-α и имел значительно меньшее количество внепеченочных побочных эффектов, включая тромбоцитопению нейтропении, гриппоподобный синдром, аутоиммунный тиреоидит и легочную артериальную гипертензию. Несмотря на то, что в настоящее время проводится несколько испытаний III фазы, в которых PEGIFN-λ1 комбинируется с другим препаратом, по прогнозам, IFN-λ с меньшей вероятностью будет играть роль для терапии вирусного гепатита С в будущем. Тем не менее, IFN-λ очень перспективен в отношении терапии отдельных инфекций с эпителиальным тропизмом, например, для кишечной инфекции, вызванной ротавирусами или норовирусами, а также респираторных инфекций, вызванных вирусами гриппа или коронавирусами (SARS и MERS). Следует отметить, что эффективность IFN типа III слабее, чем у IFN I типа, и только IFN-λ1 из всех представителей класса в настоящее время разрабатывается как терапевтический препарат.
Противоопухолевое действие
Противоопухолевая активность IFN-III аналогична IFN-I. IFN-λ индуцирует апоптоз у некоторых типов опухолей, в зависимости от экспрессии рецептора (только на эпителиальных клетках). Недавнее исследование показало, что мыши с отсутствием Ifnlr1 более восприимчивы к образованию саркомы и имею большую смертность в трансплантированных опухолевых моделях. Важно отметить, что лечение IFN-λ задерживало летальность и уменьшало развитие саркомы. IFNs-λ индуцируют апоптоз в клетках колоректального рака сильнее, чем IFN-α/β или IFN-γ. В другом недавнем исследовании, где сравнивались противоопухолевые эффекты IFN-α и IFN-λ в модели гепатомы мыши, оба IFN демонстрировали сопоставимую противоопухолевую активность, но комбинация IFN-λ и IFN-α достигала более существенных противоопухолевых эффектов по сравнению с использованием только одного класса IFN. Это дает основания для разработки схем комбинированной терапии интерферонами. На данный момент нельзя сказать, сможет ли IFN-λ стать заменой IFN-I, однако, есть возможность комбинированной терапии интерферонами, а также сочетания с другими противоопухолевыми препаратами. Например, был описан синергетический эффект IFN-λ с бортезомибом или темозолимидом при терапии меланомы. Лечение карциномы пищевода комбинацией IFN-λ и CDDP (цисплатин) или 5-FU (фторурацил) проявляло аддитивный эффект.
Иммуномодулирующее действие
В настоящее время имеющиеся данные свидетельствуют об различных вкладах передачи сигналов IFN-λ в аутоиммунных состояниях. Предполагаются противовоспалительные функции IFN-λ. В экспериментальной мышиной модели аутоиммунного артрита лечение IFN-λ2 приводило к регрессу заболевания и повреждения суставов путем подавления ответов IL-1 и IL-17, а также вербовки нейтрофилов, которые выражают IFN-λR1. Авторы утверждают, что поскольку IFN-λ структурно связан с IL-10 (общая субъединица в рецепторе), он может иметь противовоспалительную активность. Была предложена защитная роль для IFN-λ при аллергической астме. В мышиной модели астмы введение IFN-λ снижает иммунные адаптивные изменения и сводит к минимуму тяжесть заболевания; это связано с производством IL-13 и IL-5, а также снижением Th17-клеточных ответов и инфильтрации легких эозинофилами. В этой модели защитная активность IFN-λ зависела от IFN-γ и IL-12, что приводило к опосредованному IFN-λ Th1-перекосу. Таким образом, существует обоснование терапевтического введения рекомбинантных IFNs-λ при обострениях астмы с целями снижения вирусной нагрузки и модулирования аллергической основы заболевания. Аналогично, введение IFN-λ может быть вариантом лечения ревматоидного артрита.
Обобщая вышесказанное, интерфероны представляют собой чрезвычайно биологически активные молекулы с широким спектром действия и разнообразными эффектами. Разные классы интерферонов демонстрируют свои особенности влияния на организм, однако прослеживаются три основных направления клинического применения интерферонов: противоинфекционное, противоопухолевое и иммуномодулирующее. Соответственно, интерферонотерапия применима к таким областям медицины как онкология, инфекционные и аутоиммунные патологии. Дальнейшее изучение как свойств самих интерферонов, так и комбинирования IFNs с другими препаратами позволит открыть множество новых эффективных терапевтических стратегий в отношении широкого круга заболеваний.