С чем взаимодействует бор
Среди элементов IIIa группы один лишь бор относится к неметаллам. Представляет собой аморфное кристаллическое вещество красного или темного цвета, может быть бесцветным.
Общая характеристика элементов IIIa группы
От B к Tl (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Природные соединения
Получение
Бор получают путем пиролиза бороводородов, методом металлотермии (вытеснением активным металлом) и термическим разложением бромида бора в присутствии катализатора
BBr3 + H2 → (вольфрам, t = 1000-1200 С°) B + HBr
Химические свойства
Необходимо заметить, что бор довольно инертный неметалл. При комнатной температуре без нагревания он реагирует только со фтором:
При нагревании бор реагирует с другими галогенами, азотом, фосфором, углеродом и кислородом.
При сильном нагревании бор способен восстановить кремний из его оксида:
Ионы бора окрашивают пламя в оттенки зеленого цвета.
Оксид и гидроксид бора
Оксид и гидроксид бора (борная кислота) проявляют кислотные свойства.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Бор, свойства атома, химические и физические свойства
Бор, свойства атома, химические и физические свойства.
10,806-10,821 1s 2 2s 2 2p 1
Бор — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 5. Расположен в 13-й группе (по старой классификации — главной подгруппе третьей группы), втором периоде периодической системы.
Общие сведения:
| 100 | Общие сведения* | |
| 101 | Название | Бор |
| 102 | Прежнее название | |
| 103 | Латинское название | Borum |
| 104 | Английское название | Boron |
| 105 | Символ | B |
| 106 | Атомный номер (номер в таблице) | 5 |
| 107 | Тип | Неметалл |
| 108 | Группа | |
| 109 | Открыт | Жозеф Луи Гей-Люссак и Луи Жак Тенар, Франция, 30 июня 1808 г., Гемфри Дэви, Великобритания, 9 июля 1808 г. |
| 110 | Год открытия | 1808 г. |
| 111 | Внешний вид и пр. | Бесцветные, тёмно-серые, тёмно-коричневые, тёмно-красные или бурые кристаллы. Либо тёмно-серое или чёрное аморфное вещество |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | Более 10 аллотропных модификаций бора, в т.ч.: |
— α-R-бор (B12) с ромбоэдрической (тригональной) кристаллической решёткой и 12 атомами в элементарной ячейке,
— β-R-бор с ромбоэдрической (тригональной) кристаллической решёткой и
105 атомами в элементарной ячейке,
— α-T-бор ((B12)4B2) с тетрагональной кристаллической решёткой и 50 атомами в элементарной ячейке,
— β-T-бор с тетрагональной кристаллической решёткой,
— γ-бор с орторомбической кристаллической решёткой и 28 атомами в элементарной ячейке,
— сверхпроводящий бор с неизвестной кристаллической решёткой.
Большинство аллотропных модификаций бора основаны на икосаэдрических мотивах B12
γ-бор получается путем сжатия других аллотропных модификаций бора до 12 – 20 ГПа и нагревания до 1500 – 1800 °C. γ-бор остаётся стабильным после понижения температуры и давления.
α-T-бор и β-T-бор получаются путем сжатия других аллотропных модификаций бора до 12 – 20 ГПа и нагревания до 1800 – 2200 °C.
Свойства атома бора :
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса)* | 10,806-10,821 а.е.м. (г/моль) |
| 202 | Электронная конфигурация | 1s 2 2s 2 2p 1 |
| 203 | Электронная оболочка | K2 L3 M0 N0 O0 P0 Q0 R0 |
(в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле)

Химические свойства бора:
| 300 | Химические свойства | |
| 301 | Степени окисления | -1, 0, +1, +2, +3 |
| 302 | Валентность | III |
| 303 | Электроотрицательность | 2,04 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 800,64 кДж/моль (8,298019(3) эВ) |
| 305 | Электродный потенциал | |
| 306 | Энергия сродства атома к электрону | 26,989(3) кДж/моль (0,279723(25) эВ) |
Физические свойства бора:
| 400 | Физические свойства | |
| 401 | Плотность | 2,34 г/см 3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело), |
2,46 г/см 3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело) — α-R-бор,
2,35 г/см 3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело) — β-R-бор,
2,36 г/см 3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело) — β-Т-бор,
2,52 г/см 3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело) — γ-бор,
2,08 г/см 3 (при температуре плавления 2076 °C и иных стандартных условиях, состояние вещества – жидкость)
27,4 Вт/(м·К) (при 300 K)
0,1 мм.рт.ст. (при 2358°C),
1 мм.рт.ст. (при 2625°C),
10 мм.рт.ст. (при 2957°C)
2,1 эВ – γ-бор
Кристаллическая решётка бора:
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | α-R-бор |
| 512 | Структура решётки | Ромбоэдрическая (тригональная) |

Дополнительные сведения:
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-42-8 |
Примечание:
100* Данные в таблице приводятся применительно к кристаллическому бору.
201* Указан диапазон значений атомной массы в связи с различной распространённостью изотопов данного элемента в природе.
205* Эмпирический радиус атом бора [1] и [3] составляет 90 пм и 98 пм соответственно.
206* Ковалентный радиус бора согласно [1] составляет 84±3 пм.
402* Температура плавления бора согласно [3] составляет 2075 °C (2 348 K, 3767°F).
403* Температура кипения бора согласно [3] составляет 3865 °C (4 138 K, 6989 °F).
407* Удельная теплота плавления (энтальпия плавления ΔHпл) бора согласно [3] и [4] составляет 23,60 кДж/моль и 23 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) бора согласно [3] и [4] составляет 504,5 кДж/моль и 530 кДж/моль соответственно.
410* Молярная теплоемкость бора согласно [3] составляет 11,09 Дж/(K·моль).
С чем взаимодействует бор
(молярная масса)
(первый электрон)
Бор (B, лат. borum ) — химический элемент 13-й группы, второго периода периодической системы (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе III группы, или к группе IIIA) с атомным номером 5. Бесцветное, серое или красное кристаллическое либо тёмное аморфное вещество. Известно более 10 аллотропных модификаций бора, образование и взаимные переходы которых определяются температурой, при которой бор был получен.
Содержание
История и происхождение названия
Впервые получен в 1808 году французскими химиками Ж. Гей-Люссаком и Л. Тенаром нагреванием борного ангидрида B2O3 с металлическим калием. Через несколько месяцев бор получил Хэмфри Дэви электролизом расплавленного B2O3.
Название элемента произошло от арабского слова бурак (араб. بورق ) или персидского бурах (перс. بوره ), которые использовались для обозначения буры.
Нахождение в природе
Среднее содержание бора в земной коре составляет 4 г/т. Несмотря на это, известно около 100 собственных минералов бора; в «чужих» минералах он почти не встречается. Это объясняется, прежде всего, тем, что у комплексных анионов бора (а именно в таком виде он входит в большинство минералов) нет достаточно распространённых аналогов. Почти во всех минералах бор связан с кислородом, а группа фторсодержащих соединений совсем малочисленна. Элементарный бор в природе не встречается. Он входит во многие соединения и широко распространён, особенно в небольших концентрациях; в виде боросиликатов и боратов, а также в виде изоморфной примеси в минералах входит в состав многих изверженных и осадочных пород. Бор известен в нефтяных и морских водах (в морской воде 4,6 мг/л), в водах соляных озёр, горячих источников и грязевых вулканов.
Основные минеральные формы бора:
Также различают несколько типов месторождений бора:
Крупнейшее месторождение России находится в Дальнегорске (Приморье). Оно относится к боросиликатному типу. В этом одном компактном месторождении сосредоточено не менее 3 % всех мировых запасов бора. На действующем при месторождении горно-химическом предприятии выпускается боросодержащая продукция, которая удовлетворяет потребности отечественной промышленности. При этом 75 % продукции идёт на экспорт в Корею, Японию и Китай.
Получение
Физические свойства
Чрезвычайно твёрдое вещество (уступает только алмазу, нитриду бора (боразону), карбиду бора, сплаву бор-углерод-кремний, карбиду скандия-титана). Обладает хрупкостью и полупроводниковыми свойствами (широкозонный полупроводник).
У бора — самый высокий предел прочности на разрыв 5,7 ГПа.
Изотопы бора
В природе бор находится в виде двух изотопов 10 B (19,8 %) и 11 B (80,2 %).
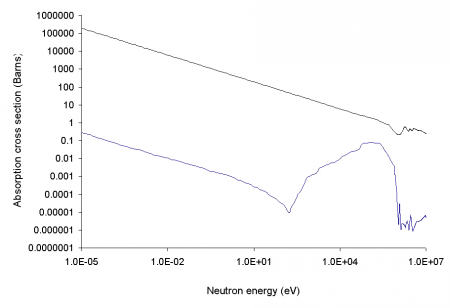
10 B имеет очень высокое сечение захвата тепловых нейтронов, равное 3837 барн (для большинства нуклидов это сечение близко к единицам или долям барна), причём при захвате нейтрона образуются два нерадиоактивных ядра (альфа-частица и литий-7), очень быстро тормозящиеся в среде, а проникающая радиация (гамма-кванты) при этом отсутствует, в отличие от аналогичных реакций захвата нейтронов другими нуклидами:
10 B + n → 11 B* → α + 7 Li + 2,31 МэВ.
Поэтому 10 B в составе борной кислоты и других химических соединений применяется в атомных реакторах для регулирования реактивности, а также для биологической защиты от тепловых нейтронов. Кроме того, бор применяется в нейтрон-захватной терапии рака.
Кроме двух стабильных, известно ещё 12 радиоактивных изотопов бора, из них самым долгоживущим является 8 B с периодом полураспада 0,77 с.
Происхождение
Все изотопы бора возникли в межзвёздном газе в результате расщепления тяжелых ядер космическими лучами, или при взрывах сверхновых.
Химические свойства
По многим физическим и химическим свойствам неметалл бор напоминает кремний.
Химически бор довольно инертен и при комнатной температуре взаимодействует только со фтором:
При нагревании бор реагирует с другими галогенами с образованием тригалогенидов, с азотом образует нитрид бора BN, с фосфором — фосфид BP, с углеродом — карбиды различного состава (B4C, B12C3, B13C2). При нагревании в атмосфере кислорода или на воздухе бор сгорает с большим выделением теплоты, образуется оксид B2O3:
С водородом бор напрямую не взаимодействует, хотя известно довольно большое число бороводородов (боранов) различного состава, получаемых при обработке боридов щелочных или щелочноземельных металлов кислотой:
При сильном нагревании бор проявляет восстановительные свойства. Он способен, например, восстановить кремний или фосфор из их оксидов:
Данное свойство бора можно объяснить очень высокой прочностью химических связей в оксиде бора B2O3.
При отсутствии окислителей бор устойчив к действию растворов щелочей. Растворяется в расплаве смеси гидроксида и нитрата калия:
В горячей азотной, серной кислотах и в царской водке бор растворяется с образованием борной кислоты H3BO3.
Оксид бора B2O3 — типичный кислотный оксид. Он реагирует с водой с образованием борной кислоты:
При взаимодействии борной кислоты со щелочами возникают соли не самой борной кислоты — бораты (содержащие анион BO3 3− ), а тетрабораты, например:
В 2014 г. исследователями из Германии был получен бис(диазаборолил) бериллия, в котором атомы бериллия и бора образуют двухцентровую двухэлектронную связь (2c-2e), впервые полученную и нехарактерную для соседних элементов в Периодической таблице.
Применение
Элементарный бор
Бор (в виде волокон) служит упрочняющим веществом многих композиционных материалов.
Также бор часто используют в электронике в качестве акцепторной добавки для изменения типа проводимости кремния.
Бор применяется в металлургии в качестве микролегирующего элемента, значительно повышающего прокаливаемость сталей.
Бор применяется и в медицине при бор-нейтронозахватной терапии (способ избирательного поражения клеток злокачественных опухолей).
Соединения бора
Карбид бора применяется в компактном виде для изготовления газодинамических подшипников.
Пербораты / пероксобораты (содержат ион [B2(O2)2(OH)4]2 − ) [B4O12H8] − ) применяются как окислительные агенты. Технический продукт содержит до 10,4 % «активного кислорода», на их основе производят отбеливатели, не содержащие хлор («персиль», «персоль» и др.).
Отдельно также стоит указать на то, что сплавы бор-углерод-кремний обладают сверхвысокой твёрдостью и способны заменить любой шлифовальный материал (кроме алмаза, нитрида бора по микротвёрдости), а по стоимости и эффективности шлифования (экономической) превосходят все известные человечеству абразивные материалы.
Сплав бора с магнием (диборид магния MgB2) обладает, на данный момент, рекордно высокой критической температурой перехода в сверхпроводящее состояние среди сверхпроводников первого рода. Появление вышеуказанной статьи стимулировало большой рост работ по этой тематике.
Борная кислота (B(OH)3) широко применяется в атомной энергетике в качестве поглотителя нейтронов в ядерных реакторах типа ВВЭР (PWR) на «тепловых» («медленных») нейтронах. Благодаря своим нейтронно-физическим характеристикам и возможности растворяться в воде применение борной кислоты делает возможным плавное (не ступенчатое) регулирование мощности ядерного реактора путём изменения её концентрации в теплоносителе — так называемое «борное регулирование».
Борная кислота применяется также в медицине и ветеринарии.
Нитрид бора, активированный углеродом, является люминофором со свечением от синего до жёлтого цвета под действием ультрафиолета. Обладает самостоятельной фосфоресценцией в темноте и активируется органическими веществами при нагреве до 1000 °C. Изготовление люминофоров из нитрида бора, состава BN/C не имеет промышленного назначения, но широко практиковалось химиками-любителями в первой половине XX века.
Боросиликатное стекло — стекло обычного состава, в котором заменяют щелочные компоненты в исходном сырье на окись бора (B2O3).
Фторид бора BF3 при нормальных условиях является газообразным веществом, используется как катализатор в оргсинтезе, а также как рабочее тело в газонаполненных детекторах тепловых нейтронов благодаря захвату нейтронов бором-10 с образованием ядер лития-7 и гелия-4, ионизирующих газ (см. реакцию выше).
Бороводороды и борорганические соединения
Ряд производных бора (бороводороды) являются эффективными ракетными топливами (диборан B2H6, пентаборан, тетраборан и др.), а некоторые полимерные соединения бора с водородом и углеродом стойки к химическим воздействиям и высоким температурам (как широко известный пластик Карборан-22).
Боразон и его гексагидрид
Нитрид бора (боразон) подобен (по составу электронов) углероду. На его основе образуется обширная группа соединений, в чём-то подобных органическим.
Биологическая роль
Бор — важный микроэлемент, необходимый для нормальной жизнедеятельности растений. Недостаток бора останавливает их развитие, вызывает у культурных растений различные болезни. В основе этого лежат нарушения окислительных и энергетических процессов в тканях, снижение биосинтеза необходимых веществ. При дефиците бора в почве в сельском хозяйстве применяют борные микроудобрения (борная кислота, бура и другие), повышающие урожай, улучшающие качество продукции и предотвращающие ряд заболеваний растений.
Один из редких типов дистрофии роговицы связан с геном, кодирующим белок-транспортер, предположительно регулирующий внутриклеточную концентрацию бора.