С21н30о2 что за формула
| Фармакологические форумы |  Помощь Помощь  Поиск Поиск  Участники Участники  Репутация Репутация  Текстовая версия Текстовая версия |
| Здравствуйте Гость ( Вход | Регистрация ) | Выслать повторно письмо для активации |

В этом разделе запрещены не проверенные администрацией объявления оптовых скупок и распродаж лекарств.
  |
 |   |
Подписаться на тему
Уведомление на e-mail об ответах в тему, во время Вашего отсутствия на форуме.
Подписка на этот форум
Уведомление на e-mail о новых темах на форуме, во время Вашего отсутствия на форуме.
Скачать/Распечатать тему
Скачивание темы в различных форматах или просмотр версии для печати этой темы.
В. Г. Лазурьевский, Л. А. Николаева
Главная > Документ
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
Фракция «сырой протеин» не обладает какой-либо специфичностью, то есть не отличается от обычного растительного белка, что было установлено нами по аминокислотному составу.
Отдельными пробами в анализированном образце гашиша доказано отсутствие сапонинов, алкалоидов и флаваноидов. Качественная проба на кумарины положительная.
По содержанию и соотношению каннабиноидов образцы гашиша различного происхождении заметно отличаются. Показана определенней зависимость состава фенольных компонентов от географических условий произрастания конопли.
Каннабиноиды обнаружены не только в цветущих метелках, но и в других частях растения, однако содержание их в листьях и стеблях более низкое, чем в гашише. (Фактический материал, относящийся к этому вопросу, приведен в IV главе.)
В литературе некоторое время дискутировался вопрос о наркотической ценности гашиша в зависимости от сортности и места произрастания конопли.
3. Специфические вещества конопли – каннабиноиды
Своеобразное действие гашиша на организм животных и человека издавна интересовало ботаников, химиков фармакологов, врачей. Прежде всего необходимо было выявить химическую природу веществ, являющихся носителями наркотических свойств, а также пути их образования в растении, определить их содержание в зависимости от почвенно-климатических условий, разработать методы обнаружения и другие вопросы. В ранее опубликованных статьях было немало ошибочных данных и толкований отдельных наблюдений, что частично объясняется лабильностью физиологически активных соединений конопли.
Реальные результаты в химии гашиша были достигнуты лишь в 30-е годы нашего столетия; описаны способы выделения трех индивидуальных соединений (каннабинол, каннабидиол и тетрагидроканнабинол) и впервые приведены их правильные суммарные формулы.
Природа этих веществ была установлена в большой серии работ таких известных химиков, как Адаме (США) и Тодд (Англия). Они же осуществили первые синтезы каннабиноидов [15, 16. 17].
В исследованиях 30-х и 40-х годов разделение смеси фенольных соединений проводилось разгонкой в вакууме. Выход конечных продуктов был крайне низким и они не были свободны от примесей; при термическом воздействии возможны изомеризация, декарбоксилирование и другие реакции, приводящие к образованию вторичных продуктов.
Даже очищенная многократной перегонкой в вакууме сумма каннабиноидов — это красно-бурое масло, темнеющее при хранении. Ацетилирование частично стабилизирует его и облегчает процесс разделения. В работах ученых за последние десять лет было показано, что фенольные соединения конопли фактически представляют собой трудно разделяемую смесь структурных, оптических и геометрических изомеров. Расшифровать эти тонкие детали строения оказалось возможным лишь при использовании новейших физических методов и хроматографии.
Успехи в этой заключительной стадии исследования были достигнуты главным образом в Химическом институте университета в Бонне (ФРГ) под руководством Кортэ [20] и в Институте Вейзмаша под руководством Гаопи и Мехулэма (Израиль). Последние опубликовали наиболее полный обзор по химии гашиша[18].
Нами приведены формулы 9-фенольных соединений, выделенных из конопли, строение доказано с полной достоверностью, а также их важнейшие константы и сокращенные обозначения, которыми в дальнейшем мы будем пользоваться.
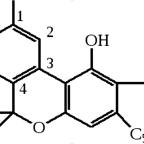
Среди фенольных соединений конопли описай также каннабициклол (КБЦ) (С 21 Н 30 О 2 ) с т. пл. 152-153 0 С, строение которого показано ниже, но оно не сразу было строго установлено [18]. В 1971 г. в спиртовом экстракте листьев и цветочных головок конопли обнаружен «необычный» пропильный гомолог ТГК (C 19 H 26 О 2 ), названный тетрагидроканнабидиваролом (ТГКВ) [19].
Как видно из приведенных формул, все каннабиноиды имеют родственное строение и с полным основанием могут быть объединены в одну группу природных фенолов.
Следует отметить, что у многих авторов, публикующих химические работы по гашишу, до последнего времени не было единообразия в терминологии. В работах Адамса применялась нумерация, установленная для дибензопирана, Кортэ с сотрудниками обозначали те же вещества, как принято для производных дифенила. Мы будем пользоваться наиболее удачной номенклатурой, предложенной Гаони и Мехулэмом, в которой природные каннабиноиды и их синтетические аналоги рассматриваются как фенилированные монотерпены. Это согласуется с требованиями современной рациональной номенклатуры.
В количественном содержании каннабиноидов в конопле нет постоянства. Варьирует также и соотношение между отдельными веществами в зависимости от сорта и места произрастания растения, сроков и способов сбора гашиша, продолжительности и условий хранения.
Однако, как правило, в смеси преобладают три вещества — КБН, КБД и ТГК и некоторые их кислотные производные. Остальные каннабиноиды содержатся в минорных и следовых количествах.
Из всех фенольных компонентов гашиша только КБН отличается химической устойчивостью и сравнительно легко выделяется в кристаллическом состоянии. Это объясняется полной его ароматичностью и отсутствием изомеров. В случаях, где циклогексановое кольцо частично дегидрировано, вещества могут быть в виде структурных, геометрических и пространственных изомеров. Смеси их представляют собой вязкие масла, трудно поддающиеся разделению на индивидуальные соединения.
Не просто установить и место локализации двойной связи в цикле из-за возможной ее миграции.
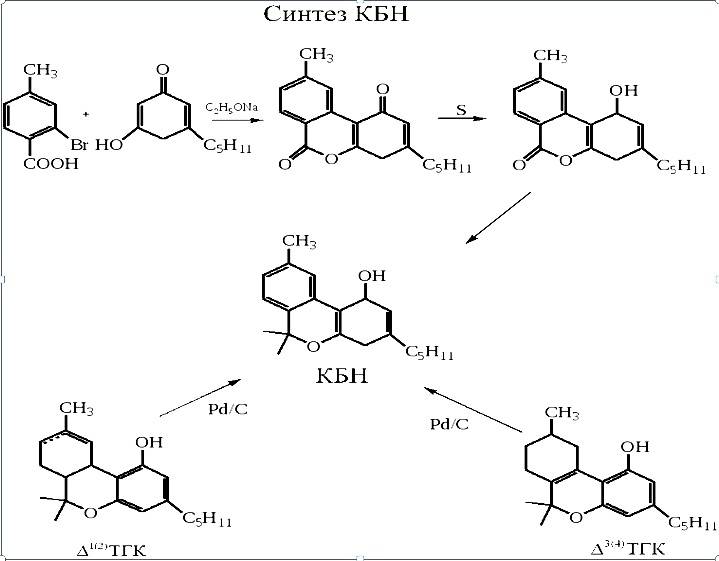
Строение КБН безупречно доказано на основании аналитических данных и встречного синтеза, схема которого приведена ниже[15]. Дигидрооливетол, полученный при каталитическом восстановлении оливетола, конденсировался с 2-бром-4метилбензойной кислотой в присутствии алкоголята натрия и ацетата меди. Образовавшийся лактон дегидрировался серой и обрабатывался иодидом метилмагния.
Это вещество в дальнейшем неоднократно использовалось для доказательства строения углеродного скелета изомеров ТГК, которые при дегидрировании превращались в легко идентифицируемый КБН.
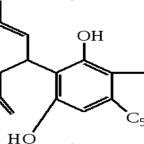
Формула КБД выводится из дачных анализа, наличия двух фенольных гидроксилов (получение диметиловых эфиров), двух легко гидрируемых кратных связей, на основании образования муравьиной кислоты при окислении, свидетельствующей о том, что одна из кратных связей находится на конце боковой цепи.
Переход КБД в ТГК при нагревании с кислыми катализаторами, сопровождающийся уменьшением числа двойных связей и фенольных гидроксилов, свидетельствует о происходящей циклизации в производное бензопирана.
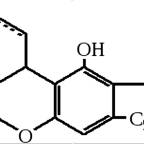
Структура ТГК вытекает из взаимосвязи его с КБН и КБД (стр. 18-19). Описаны также многовариантные синтезы структурных, геометрических и пространственных изомеров. Из всех известных каннабиноидов только изомеры ТГК отличаются высокой психотомиметической активностью; остальные фактически не являются наркотиками, хотя рассматриваются как биогенетические предшественники или как потенциальные их источники. Поэтому изучению строения изомеров ТГК уделялось особенно большое внимание.
Вместе с тем возникли трудности, обусловленные лабильностью ТГК и множеством изомеров. Преодоление этих трудностей является одним из крупных достижением современной органической химии.
Альтернативное положение двойной связи при Δ 1(2) и Δ 1(6) в природном ТГК устанавливалось на основании спектров ПМР [21], где выявляется триплет 0,88 м.д. (алифатическая метильная группа), синглеты 1,08; 1,38, 1,65 м.д. (три метальные группы, при двойной связи или по соседству с кислородом), широкий дуплет 3,14 м.д. (протон при третичном углеродном атоме), широкий синглет 6,35 м.д. (олефиновый протон), дуплеть 6,00; 6,18 м.д. (два ароматических протона).
Сопоставляя химические сдвиги протонов при С 2 и С 3 в природном транс-ТГК и в синтезированном цис-ТГК, а также в КБД (где имеет место свободное вращение циклов), авторы делают вывод о преобладании транс-Δ 1(2) ТГК в анализируемых образцах.
Казалось, что изомеры ТГК можно получить направленным синтезом, где положение двойной связи должно быть фиксировано в зависимости от строения исходных веществ (стр.24, схема III, IV). Однако в действительности всегда получались смеси, обогащенные тем или иным изомером. Методом газовой хроматографии Кортэ и Зипер обнаружили в гашише минимум три разных по свойствам ТГК [22]. При высокой температуре (около 200°) КБД превращается по меньшей мере в пять веществ, различающихся по хроматографической подвижности.
Превращение КБД и ТГК под действием кислых реагентов было подтверждено и нашими опытами. Более того, мы обнаружили и противоположный процесс, свидетельствующий о лабильности ТГК. Хроматографически однородный ТГК был оставлен на длительное хранение. По истечении 8 месяцев появились ранее отсутствовавшие примеси (пятна на хроматограмме) других фенольных соединеий, в том числе и КБД, то есть зафиксирована реакция размыкания окисного кольца
Гаони и Мехулэм [18] установили, что КБД при взаимодействии с кислыми реагентами частично циклизуются в ТГК. Если реакцию проводить в абсолютном спирте насыщенным хлористым водородом, то образуется преимущественно Δ 1(2) ТГК, если же в бензоле с пара-толуолсульфокислотой, то Δ 1(6) ТГК. Второй изомер считается более стабильным, при хранении его содержание возрастает за счет уменьшения первого. При проведении реакции с хлористым водородом в присутствии хлористого цинка в растворе хлористого метилена из оптически деятельного стабильного изомера (-)-транс Δ 1(6) ТГК образуется (-)-хлоргексагидроканнабинол, который при нагревании при нагревании с амилатом калия в бензоле вновь отщепляет хлористый водород и превращается в нестабильный (
Однако в процессе очистки и хранения проходит обратная изомеризация. поэтому дальнейшая работа по разделению изомеров была признана бессмысленной. В каждом образце ТГК можно лишь ориентировочно определить соотношение двух изомеров, с этой целью и в случае оптически деятельных соединений достаточно замерить удильное вращение, которое выше для (-)-Δ 1(6) ТГК.
При сравнении масс-спектров ТГКВ и ГГ’К установлено, что относительные интенсивности пиков их молекулярных ионов являются величинами одного порядка (соответственно 0,68 и 0,81). В области высоких массовых чисел в обоих случаях наблюдается доброе 15 m/е (происходит потеря метильной группы), причем интенсивности пиков с m/е 271 соответственно тm/е 299 также соизмеримы. Учитывая идентичность масс-спектров, можно утверждать, что ТГ’КВ, так же как и ТГK, имеет Δ 1(2) двойную связь и циклогексановом кольце.
Конопля и химия
Учеными-химиками также было показано, что фенольные соединения конопли представляют собой трудно разделяемую смесь структурных, оптических и геометрических изомеров. В Химическом институте университета в Бонне (ФРГ) под руководством Кортэ и в Институте Вейзмаша (Израиль) под руководством Гаопи и Мехулэма с помощью физических методов и хроматографии смогли расшифровать тонкие детали строения этих изомеров и пришли к выводу, что все каннабиноиды имеют родственное строение и относятся группе природных фенолов.
Каннабиноловая кислота (КБНК),
(КВДК)
Тетрагидроканнабинол, (ТГК)
Тетрагидроканнабиоловая кислота, (ТГКК)
КБН сравнительно легко выделяется в кристаллическом состоянии, отличается химической устойчивостью и не имеет изомеров. Лишь в случаях, когда циклогексановое кольцо частично дегидрировано, обнаруживаются структурные, геометрические и пространственные изомеры. Их смеси представляют собой вязкие масла, трудно поддающиеся разделению на индивидуальные соединения. Строение КБН безупречно доказано на основании аналитических данных и встречного синтеза., при котором дигидрооливетол, полученный при каталитическом восстановлении оливетола, конденсировался с 2-бром-4метилбензойной кислотой в присутствии алкоголята натрия и ацетата меди. Образовавшийся лактон дегидрировался серой и обрабатывался иодидом метилмагния.
Формула КБД выводится из данных анализа, показывающих наличие двух фенольных гидроксилов (получение диметиловых эфиров), двух легко гидрируемых кратных связей, на основании образования муравьиной кислоты при окислении, свидетельствующей о том, что одна из кратных связей находится на конце боковой цепи. Переход КБД в ТГК при нагревании с кислыми катализаторами, сопровождающийся уменьшением числа двойных связей и фенольных гидроксилов, свидетельствует о происходящей циклизации в производное бензопирана. Положение двойной связи в циклогексановом кольце КБД было установлено Мехулэмом с помощью спектров ПМР, сопоставляемых со спектрами тетрагидроканнабидиола и моноэпоксида. В первом случае химический сдвиг1 протона при С3 составляет 3,0 м. д., во втором — 3,14 м. д. Это может быть объяснено только тем, что двойная связь находится при Δ1(2).
Гаони и Мехулэм установили, что КБД при взаимодействии с кислыми реагентами частично циклизуются в ТГК. Если реакцию проводить в абсолютном спирте насыщенным хлористым водородом, то образуется преимущественно Δ1(2) ТГК, если же в бензоле с пара-толуолсульфокислотой, то Δ1(6) ТГК. Второй изомер считается более стабильным, при хранении его содержание возрастает за счет уменьшения первого. При проведении реакции с хлористым водородом в присутствии хлористого цинка в растворе хлористого метилена из оптически деятельного стабильного изомера (-)-транс Δ1(6) ТГК образуется (-)-хлоргексагидроканнабинол, который при нагревании при нагревании с амилатом калия в бензоле вновь отщепляет хлористый водород и превращается в нестабильный ()-транс-Δ1(2) ТГК. Однако в процессе очистки и хранения проходит обратная изомеризация. поэтому дальнейшая работа по разделению изомеров была признана бессмысленной. В каждом образце ТГК можно лишь ориентировочно определить соотношение двух изомеров, с этой целью и в случае оптически деятельных соединений достаточно замерить удильное вращение, которое выше для (-)-Δ1(6) ТГК.
Из всех известных каннабиноидов только изомеры ТГК отличаются высокой психотомиметической активностью; остальные фактически не являются наркотиками. Удельное вращение ТГК колеблется в широких пределах: от [α]D – 1200 до 2600 Значения длин волн максимума поглощения в УФ-спектре λ макс. 208-227 нм также непостоянны. Это можно объяснить различным соотношением изомеров ТГК различного происхождения. Положение двойной связи в циклогексановом кольце было постулировано еще Адамсом, который на основании химических превращений показал невозможность локализации двойной связи при Δ4(5), Δ5(6), Δ2(3). Синтезированный им Δ3(4) ТГК оптически недеятелен.
Альтернативное положение двойной связи при Δ1(2) и Δ1(6) в природном ТГК устанавливалось на основании спектров ПМР, где выявляется триплет 0,88 м.д. (алифатическая метильная группа), синглеты 1,08; 1,38, 1,65 м.д. (три метальные группы, при двойной связи или по соседству с кислородом), широкий дуплет 3,14 м.д. (протон при третичном углеродном атоме), широкий синглет 6,35 м.д. (олефиновый протон), дуплет 6,00; 6,18 м.д. (два ароматических протона).
Сопоставляя химические сдвиги протонов при С2 и С3 в природном транс-ТГК и в синтезированном цис-ТГК, а также в КБД (где имеет место свободное вращение циклов), можно сделать вывод о преобладании транс-Δ1(2) ТГК в анализируемых образцах.
Методом газовой хроматографии Кортэ и Зипер обнаружили в гашише минимум три разных по свойствам ТГК. При высокой температуре (около 200°) КБД превращается по меньшей мере в пять веществ, различающихся по хроматографической подвижности.
При сравнении масс-спектров ТГКВ и ГГ’К установлено, что относительные интенсивности пиков их молекулярных ионов являются величинами одного порядка (соответственно 0,68 и 0,81). В области высоких массовых чисел в обоих случаях наблюдается доброе 15 m/е (происходит потеря метильной группы), причем интенсивности пиков с m/е 271 соответственно тm/е 299 также соизмеримы. Учитывая идентичность масс-спектров, можно утверждать, что ТГ’КВ, так же как и ТГK, имеет Δ1(2) двойную связь и циклогексановом кольце.
В судебно-медицинской практике иногда возникают ситуации, при которых необходимо ответить на вопрос, является ли образец гашишем. Заключение не должно основываться только на таких показателях, как внешний вид, цвет, запах, которых варьируют в широких пределах в зависимости от происхождения условий хранения гашиша и наличия в нем наполнителей. Поэтому для идентификации гашиша используют метод хроматографического определения. Объективным критерием также может служить быстрая (до 2 мин.) «проба на гашиш». Она основана на реакции диазотированных ароматических аминов с фенольными соединениями, всегда содержащимися в конопле.
Небольшое количество испытываемого вещества (около 0,2 г.) растирают шпателем на часовом стекле или в ступке с 1-2 мл спирта. Затем с помощью стеклянного капилляра, в который заправлен ватный тампончик, набирают каплю спиртового раствора и переносят ее на листок фильтровальной бумаги. После испарения спирта, бумагу опрыскивают из пульверизатора диазотированным раствором п-нитроанилина или бензидина. Появление окрашенного в оранжевый цвет пятна подтверждает наличие гашиша в испытуемом материале.
Для более четкого воспроизведения реакции в одно и то же место на бумаге наносят несколько капель экстракта, что повышает в пробе количество каннабиноидов и соответственно чувствительность реакции. Окрашенное пятно сохраняется долгое время, и отрезок бумаги может быть приобщен к делу в качестве вещественного доказательства.
По материалам книги: Каннабиноиды, В.Г. Лазурьевский, Л.А.Николаева, сайтов
Методы решения задач по химии. Задачи на вывод химической формулы вещества
Разделы: Химия
С задачами на вывод химической формулы вещества учащиеся встречаются при прохождении программы химии с 8 по 11 классы. К тому же, данный тип задач довольно часто встречается в олимпиадных заданиях, контрольно – измерительных материалах ЕГЭ (части В и С). Диапазон сложности данных задач достаточно широк. Как показывает опыт, у школьников часто возникают затруднения уже на первых этапах решения при выводе молярной массы вещества.
В данной разработке предлагаются задачи на нахождение формулы вещества, исходя из разных параметров в условиях. В представленных задачах приведены различные способы нахождения молярной массы вещества. Задачи составлены таким образом, чтобы учащиеся могли освоить оптимальные методы и различные варианты решения. Наглядно демонстрируются наиболее общие приёмы решений. Для учащихся предлагаются решённые задачи по принципу нарастания сложности и задачи для самостоятельного решения.
Вывод химической формулы вещества:
Номер задачи
(пример решения)
Вычисление молярной массы вещества
Задачи для самостоятельного решения
— на основании массовых долей (%) атомов элементов
Определить химическую формулу соединения, имеющего состав: натрий – 27,06%; азот – 16,47 %; кислород – 57,47%. Ответ: NaNO3
— на основании массовых долей (%) атомов элементов и плотности соединения
Относительная плотность паров органического кислородсодержащего соединения по кислороду равна 3, 125. Массовая доля углерода равна 72%, водорода – 12 %. Выведите молекулярную формулу этого соединения. Ответ:C6H12О
— по плотности вещества в газообразном состоянии
М (в-ва) = ρ · М (газообр. в-ва)
Относительная плотность паров предельного альдегида по кислороду равна 1,8125. Выведите молекулярную формулу альдегида. Ответ: C3Н6О
— на основании массовых долей (%) атомов элементов и массе соединения
М находится по соотношению,
или
M
Углеводород содержит 81,82 % углерода. Масса 1 л. этого углеводорода (н.у.) составляет 1,964 г. Найдите молекулярную формулу углеводорода.
Ответ: C3Н8
— по массе или объёму исходного вещества и продуктам горения
М (в-ва)=Vm·ρ
Относительная плотность паров кислородсодержащего органического соединения по гелию равна 25,5. При сжигании 15,3 г. этого вещества образовалось 20,16 л. СО2 и 18,9 г. Н2О. Выведите молекулярную формулу этого вещества.Ответ: C6H14О
Приводится пример решения задачи № 6 на применение уравнения Менделеева – Клайперона
Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу кислоты.
Решение:
Рассчитать молярную массу кислоты CnН2n (N Н2) CОOH
w (О) =
M кислоты 
Найти число атомов углерода в молекуле кислоты и установить её формулу М = 12 n + 2 n + 16 + 45 =75
14 n = 14, n = 1
Ответ: формула кислоты NН2CН2CОOH
М (NН2CН2 CОOH) = 75 г/моль
Вывести формулу соединения
CnН2n (N Н2) CОOH
Относительная плотность углеводорода по водороду, имеющего состав: w(С) = 85,7 %; w (Н) = 14,3 %, равна 21. Выведите молекулярную формулу углеводорода.
Дано:
w (С) = 85,7 %
w (Н) = 14,3 %
D Н2 (CхНу) = 21

m (Н) = 42г. /100% · 14,3 %= 6 г.
Находим количество вещества атомов углерода и водорода
n (С) = 36г :12 г/моль = 3 моль
n (Н) = 6г.: 1 г/моль = 6 моль
Ответ: истинная формула вещества C3Н6.
Определите молекулярную формулу алкана, если известно, что его пары в 2,5 раза тяжелее аргона.
Дано:
Пары алкана в 2,5 раза тяжелее аргона
Решение:
По относительной плотности можно найти молярную массу алкана: М (C n Н 2 n + 2) = 14 n + 2 = 2,5 · М(Ar) = 100 г/моль
Откуда n = 7.
Ответ: формула алкана C7Н14
Вывести формулу алкана
C n Н2 n + 2
Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73 %, кислорода 53,30 %. Масса 300 мл. (н.у.) этого соединения равна 2,41 г. Выведите молекулярную формулу этого вещества.
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г. его в кислороде образовалось 6,72 л. СО2 и 7,2 г. Н2О.
Дано:
M (CхHу) = 4,4 г.
ρ (н.у.) = 1,97 г/л
V (СО2) = 6,72 л.
m (Н2О) = 7,2 г.
Решение:
1. Находим относительную молярную массу углеводорода, исходя из величины его относительной плотности:
М (CхHу) = Vm · ρ
М (CхHу) = 22,4л/моль · 1,97г/л = 44г/моль
2. Записываем в алгебраическом виде уравнение реакции горения газа, выразив коэффициенты через х и у.
Составляем пропорции:
4,4 / 44 = 6, 72/ х · 22,4
х = 44 · 6, 72/ 4,4 · 22,4 = 3
у = 44 · 7,2/ 4,4 · 9 = 8
Формула соединения C3H8; М (C3H8) = 44 г/моль
Ответ: молекулярная формула соединения C3H8
Соединение содержит 62,8% S и 37,2% F. Масса 118 мл данного соединения при 70 и 98,64 КПа равна 0,51 г. Вывести формулу соединения.
Дано:
w (S) = 62,8 %
w (F) = 37,2 %
m (CхHу) = 0,51 г
V (CхHу) = 118 мл.
Т = 70
Р = 98,64 кПа
n(S) : n(F) = 62,80/32 : 37,2/19 = 1,96 : 1,96 = 1 : 1
Простейшая формула S F
M
Следовательно, формула соединения S2 F2