Синдром рэа это что
Раковый эмбриональный антиген (РЭА) – это вещество белковой природы, которое используется в лабораторной практике в качестве тканевого маркера онкологических заболеваний.
Карциноэмбриональный антиген, раково-эмбриональный антиген.
Синонимы английские
Carcino Embryonic Antigen, Carcinoembryonic Antigen, CEA.
Нг/мл (нанограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Раковый эмбриональный антиген – это разновидность белков нормальных тканей, которая у здорового человека в очень малых количествах вырабатывается в клетках некоторых внутренних органов. По химической структуре РЭА представляет собой соединение белка и углеводов (гликопротеин). Его предназначение у взрослых неизвестно, а в период внутриутробного развития он интенсивно синтезируется в органах желудочно-кишечного тракта и выполняет важные функции, связанные со стимуляцией размножения клеток. РЭА также обнаруживается в тканях органов пищеварения и у взрослых людей, но в значительно меньшем количестве.
Определение уровня РЭА используется для диагностики ряда злокачественных опухолей, в первую очередь рака толстой и прямой кишки. Если в норме содержание РЭА очень низкое, то при онкологическом процессе оно резко возрастает и может достигать очень больших значений. В связи с этим его относят к тканевым маркерам онкологических заболеваний, или онкомаркерам.
Однако повышение РЭА характерно не только для злокачественного процесса – его продукция может усиливаться при различных воспалительных, аутоиммунных и других доброкачественных заболеваниях внутренних органов.
Название этого онкомаркера – раковый эмбриональный антиген – отчасти отражает его биологическую природу, но в большей степени те свойства, которые являются ценными для лабораторного исследования. «Раковый» относится к его использованию для диагностики рака. Определение «эмбриональный» связано с физиологическими функциями РЭА в период внутриутробного развития человека. Слово «антиген» указывает на возможность его идентификации в биологических средах с помощью иммунохимического анализа (связывания антигена с антителом), в то время как в организме он не проявляет каких-либо антигенных свойств.
Анализ на РЭА применяется для ранней диагностики, наблюдения за течением заболевания и контроля за результатами его лечения при некоторых опухолях, в первую очередь если это рак толстого кишечника и прямой кишки – при них тест обладает наибольшей чувствительностью, что позволяет использовать его в первичной диагностике.
Кроме опухоли толстого кишечника и прямой кишки, РЭА может повышаться при раке желудка, поджелудочной, молочной железы, легких, простаты, яичников, метастазах рака различного происхождения в печень и кости, хотя при этих состояниях чувствительность метода существенно ниже.
Помимо первичной диагностики рака, тест на РЭА используется для контроля за результатами его лечения. После успешной операции по удалению всего объема опухолевой ткани уровень РЭА возвращается к норме максимум в течение двух месяцев. В дальнейшем регулярные анализы помогают контролировать состояние пациента после лечения. Выявление повышенного уровня РЭА на ранних сроках позволяет вовремя обнаружить рецидив заболевания.
Анализ на РЭА также используется в целях контроля эффективности терапии злокачественных процессов. Снижение уровня РЭА в крови в течение курса процедур или после него свидетельствует о положительном результате проводимого лечения.
Тем не менее данный тест не является абсолютно специфичным для опухолей. РЭА может умеренно повышаться и при многих заболеваниях внутренних органов воспалительного и другого (доброкачественного) характера. Его концентрация немного увеличивается у 20-50 % больных с доброкачественными заболеваниями кишечника, поджелудочной железы, печени и легких, а также при циррозах печени, хронических гепатитах, панкреатитах, язвенных колитах, болезни Крона, пневмонии, бронхитах, туберкулезе, эмфиземе, муковисцидозе и аутоиммунных заболеваниях. Показатель повышается при обострении болезни, но в случае улучшения самочувствия возвращается к норме. При злокачественном же процессе уровень РЭА неуклонно растет на протяжении всего периода заболевания.
Кроме того, повышение РЭА может быть связано не с патологией, а, например, с регулярным курением и употреблением алкоголя.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Изолированное использование исследования в целях скрининга и диагностики онкологических заболеваний недопустимо. Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. Диагностика любого заболевания строится на основании разностороннего обследования с использованием различных, не только лабораторных методов и осуществляется исключительно врачом.
Нормальное количество РЭА в сыворотке крови указывает на низкий риск онкологического заболевания. Кроме того, такой результат возможен, если данный тест нечувствителен к тому или иному типу опухоли.
Причины повышения уровня РЭА
Небольшое повышение уровня РЭА может быть связано с доброкачественными заболеваниями внутренних органов в их острой стадии, однако не исключает начальной стадии онкологического заболевания.
Значительное повышение концентрации РЭА (кратное) возникает при злокачественных опухолях. При метастазах обычно наблюдается повышение в десятки раз.
Причины снижения уровня РЭА
Кто назначает исследование?
Врач общей практики, терапевт, гастроэнтеролог, онколог, хирург.
Ацетилсалициловая кислота и синдром Рея
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
НИИ физико-химической медицины МЗ РФ, Москва
Н естероидные противовоспалительные средства (НПВП) представляют собой группу лекарственных средств, которые широко применяются в клинической практике, при этом большинство из них находится в безрецептурном отпуске. Более тридцати миллионов людей в мире ежедневно принимают НПВП. Среди стационарных больных около 20% получают НПВП. Большая «популярность» НПВП объясняется тем, что они обладают противовоспалительным, анальгезирующим и жаропонижающим эффектами и приносят облегчение больным с соответствующими симптомами (воспаление, боль, лихорадка), которые сопутствуют многим заболеваниям.
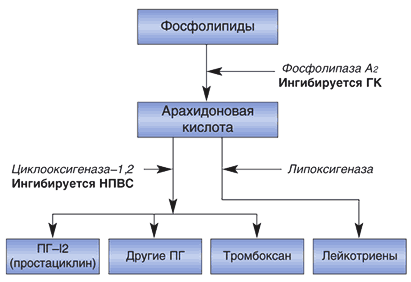
Ацетилсалициловая кислота (АСК) является старейшим и наиболее широко используемым в общеклинической практике препаратом из группы НПВП. В основе механизма действия АСК (рис. 1) лежит угнетение синтеза простагландинов (ПГ) из арахидоновой кислоты путем ингибирования фермента циклооксигеназы (простагландинсинтетазы).
Рис. 1. Метаболизм арахидоновой кислоты
В последние годы было установлено, что существуют, как минимум, два изофермента циклооксигеназы (ЦО), которые ингибируются НПВП. Первый изофермент – ЦОГ–1 – контролирует выработку простагландинов, регулирующих целостность слизистой оболочки желудочно–кишечного тракта, функцию тромбоцитов и почечный кровоток, а второй изофермент – ЦОГ–2 – участвует в синтезе простагландинов при воспалении. Причем ЦОГ–2 в нормальных условиях отсутствует, а образуется под действием некоторых тканевых факторов, инициирующих воспалительную реакцию (провоспалительные цитокины). В связи с этим предполагается, что противовоспалительное действие НПВП обусловлено ингибированием ЦОГ–2, а их нежелательные реакции – ингибированием ЦОГ–1. Соотношение активности НПВП в плане блокирования ЦОГ–1/ЦОГ–2 позволяет судить об их потенциальной токсичности. Чем меньше эта величина, тем более селективен препарат в отношении ЦОГ–2 и тем самым – менее токсичен. АСК обладает выраженной селективностью в отношении ЦОГ–1, что обусловливает многие побочные эффекты ацетилсалициловой кислоты.
Фармакодинамика ацетилсалициловой кислоты зависит от суточной дозы:
– малые дозы (до 325 мг) оказывают дезагрегационное действие (тормозят агрегацию тромбоцитов);
– средние дозы (1,5–2 г) оказывают анальгезирующее и жаропонижающее действие;
– большие дозы (4–6 г) обладают противовоспалительным эффектом; в дозе более 4 г ацетилсалициловая кислота усиливает экскрецию мочевой кислоты (урикозурическое действие), при назначении в меньших дозах ее выведение задерживается.
Широко известно, что НПВП противопоказаны при эрозивно–язвенных поражениях желудочно–кишечного тракта, особенно в стадии обострения, выраженных нарушениях функции печени и почек, цитопениях, индивидуальной непереносимости, беременности. НПВC должны с осторожностью назначаться больным бронхиальной астмой, а также лицам, у которых ранее выявлялись нежелательные реакции при приеме любых других НПВП в связи с опасностью развития бронхоспазма.Такие противопоказания, как бронхиальная астма и ЯБ желудка и двенадцатиперстной кишки, часто учитываются при назначении АСК, в то время как о возможности развития такого грозного осложнения, как синдром Рея, в отечественной медицинской литературе упоминается редко. И это несмотря на то, что при синдроме Рея смертность составляет около 20% (колеблется от 2% при I стадии неврологических нарушений до 80% при IV и V стадиях).
Синдром Рея – острое состояние, возникающее у детей и подростков (чаще в возрасте 4–12 лет) на фоне лечения лихорадки вирусного происхождения (грипп, корь, ветряная оспа) АСК–содержащими препаратами и характеризующееся быстро прогрессирующей энцефалопатией (вследствие отека головного мозга) и развитием жировой инфильтрации печени. Синдром Рея сопровождается гипераммониемией, повышением уровня АСТ, АЛТ в сыворотке крови (более 3 норм) при нормальном уровне билирубина [2,8].
Каковы же клинические проявления синдрома Рея?
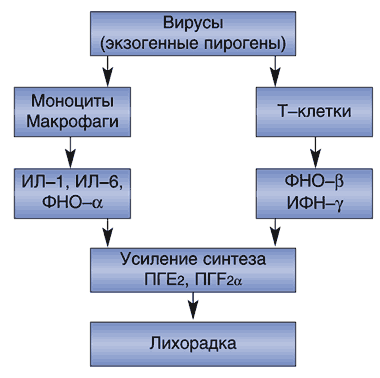
1. Вирусы являются экзогенными пирогенами, которые при попадании в организм стимулируют выработку клетками иммунной системы эндогенных пирогенов, наиболее значимыми из которых являются ИЛ–1, ИЛ–6, ФНО- a (рис. 2). При этом было выявлено, что ФНО непосредственно способен ингибировать окислительное фосфорилирование, а на фоне приема АСК возможно возрастание уровня ФНО в сыворотке крови больных вирусными инфекциями [1,8].
Рис. 2. Патогенез лихорадки при вирусных заболеваниях
Таким образом, клинические проявления при синдроме Рея обусловлены генерализованной митохондриальной дисфункцией у лиц с врожденными дефектами митохондриальных ферментов (не имевших клинических проявлений до развития данного состояния) [8]. Важно отметить, что синдром Рея развивается у больных, принимавших АСК в терапевтических дозах, вследствие чего следует отличать данное состояние от передозировки ацетилсалициловой кислоты. В эксперименте было подтверждено, что не существует минимальной дозы ацетилсалициловой кислоты, которая могла бы гарантировать отсутствие развития синдрома Рея [7,8,9].
Риск возникновения этого опасного осложнения явился основанием для принятия ограничительных мер по использованию ацетилсалициловой кислоты и салицилатов в большинстве стран мира, в том числе и в России (Международный фонд по эффективным и безопасным лекарствам. Министерство здравоохранения РФ, Бюллетень №10,1996) [2]. В инструкции по применению препаратов (включая и отпускаемые без рецепта) было рекомендовано внести предостережение о возможности развития синдрома Рея с описанием его клинических проявлений. В соответствии с принятыми ограничительными мерами: ацетилсалициловая кислота и препараты, содержащие ацетилсалициловую кислоту, для приема внутрь и ректально не должны назначаться детям и подросткам, которые болеют или находятся в стадии выздоровления после ветряной оспы, гриппа или гриппоподобных инфекций [2,8].
К сожалению, не все производители ацетилсалициловой кислоты в нашей стране пересмотрели инструкции по применению этого препарата. Учитывая отсутствие «минимальной безопасной дозы АСК», быстрое прогрессирование неврологической симптоматики, отсутствие четких предикторов развития синдрома Рея (возникновение синдрома Рея у пациентов с асимптомными дефектами митохондриальных ферментов) и высокий уровень смертности при отсутствии ранней адекватной терапии, необходим категорический запрет на использование АСК у детей и подростков на фоне лихорадки вирусного происхождения. При появлении на фоне лечения АСК–содержащими препаратами таких симптомов, как тошнота, рвота и внезапное повышение температуры, следует немедленно отменить препарат и обратиться к врачу с целью своевременной диагностики тяжелого лекарственного осложнения и оказания неотложной помощи в условиях специализированного стационара.
В настоящее время НПВП широко используются в симптоматическом лечении лихорадки при ОРВИ. Однако мало внимания отводится немедикаментозным (физическим) методам снижения температуры тела, что особенно важно в педиатрической практике. Хочется напомнить, что физические методы снижения температуры (такие как обтирание тела слабым раствором уксуса, прикладывания холода на область крупных артерий, влажное обертывание, теплая (не холодная!) ванна, клизма с водой комнатной температуры) рекомендуются не только в отечественной, но и в современной зарубежной литературе, могут быть достаточно эффективными и не имеют побочных эффектов. Необходимо помнить о таких правилах ухода за лихорадящими больными, как адекватный питьевой режим, щадящая диета, обязательное проветривание помещение, запрещение «укутывать» больного, так как последнее препятствует теплоотдаче [1].
Детям с температурой тела ниже 38,9°С обычно не требуется назначения жаропонижающих средств, кроме случаев ее плохой переносимости. Учитывая международные рекомендации, при повышении температуры тела более 38,9°С возможно назначение ацетаминофена или ибупрофена в возрастных дозировках. При соблюдении возрастных суточных дозировок отмечается хорошая переносимость данных препаратов и минимальное количество побочных эффектов.
1. Дидковский Н.А., Танасова А.Н., Лихорадка // Русский медицинский журнал, Пульмонология, том 11, №4 (176), 2003, 189–91
2. Международный фонд по эффективным и безопасным лекарствам. Министерство здравоохранеия РФ. Российский университет дружбы народов. Безопасность лекарств. Экспресс–информация. Бюллетень №10, 1996.
4. Br Beutler, St M. Beutler, The Pathogenesis of Fever //CECIL Textbook of Medicine, 19 th edition, 1994, 1568–1571
6. Clark I, Whitten R, Molynex M, Taylor T, Saicylates, nitric oxide, malaria, and Reye,s syndrome// Lancet 2001 Feb 24, 357(9256): 625–7
7. Glasgow JF, Middleton B, Moore R, Gray A, Hill J, The mechanism of inhibition of beta–oxidation by aspirin metabolites in skin fibroblasts fron Reye s syndrome patients and control//Biochim Biophys Acta 1999 May 31, 1454(1):115–25
8. Glasow.J.F.T., Middleton B, Reye syndrome – insights on causation and prognosis// Arch Dis Child, 2001, 85, 351–353
9. Crocker JF, Digout SC, LeeSH, RozeeKR, Effects of antypyretics on mortality due to influenza B virus in mouse model of Reye s syndrome// Clin Invest Med 1998 Aug–Oct, 21(4–5):192–202
10. Thabet F, Dudand P, Chevret L, FabreM et al, Severe Reye syndrome : report of 14 cases managed in a pediatric intensive care until over 11 years // Arch Pediatr 2002 Jun, 9(6): 581–6
Раково-эмбриональный антиген (Carcinoembryonic antigen)
| Исследуемый биоматериал | Кровь венозная (сыворотка) |
| Метод исследования | ИХЛА |
| Cрок исполнения с момента поступления биоматериала в лабораторию | 1 к.д. |
Описание
Раково-эмбриональный антиген представляет собой соединение белка и углеводов, которое синтезируют некоторые клетки нашего организма в минимальном количество. Во время внутриутробного развития, это вещество продуцируют клетки закладывающегося и развивающегося ЖКТ, что в итоге приводит к необходимому делению клеток и формированию ЖКТ. Но после рождения необходимости в таком размножении клеток нет, поэтому продукция РЭА значительно снижается. До сих пор до конца неизвестна роль РЭА после рождения. Образование его клетками желудочно-кишечного тракта в незначительном количестве у здорового человека доказана, но какое влияние эта концентрация оказывает на ткани и органы, пока остается загадкой. Тем не менее, в ходе масштабных исследований стало точно известно, что нездоровые, а именно раковые клетки, способны синтезировать РЭА в большом количестве. Эта способность легла в основу диагностики злокачественных образований различных органов путем исследования уровня РЭА.
Так, исследование РЭА обязательно проводится при подозрении на рак толстого отдела кишечника и прямой кишки. При наличии даже начальных злокачественных изменений опухолевые клетки продуцируют РЭА в большем количестве, что отражается на его концентрации в крови. Также анализ проводится при ряде других заболеваний, особенно при высокой вероятности наличия опухолевых заболеваний не только ЖКТ, но и легких, яичников, простаты, молочных желез. Таким образом, РЭА рассматривается как показатель онкологических процессов, являясь при этом онкомаркером ряда заболеваний. Но не всегда РЭА повышается лишь при злокачественных процессах. На фоне аутоиммунных заболеваний, выраженных воспалительных изменений, во время чрезмерного употребления алкоголя или курения, уровень РЭА также повышается.
Следует учитывать, что данное исследование не может рассматриваться как абсолютно специфическое, так как повышение РЭА наблюдается и при неопухолевых процессах. Также не всегда злокачественное образование того или иного органа сопровождается повышением РЭА. Но если при онкологическом процессе РЭА стойко повышается, то при иных изменениях (воспаление, доброкачественная опухоль) РЭА снижает после обострения, в стадию ремиссии.
Подготовка
Взятие крови производится натощак (не ранее, чем через 3 часа после последнего приема пищи). Можно пить воду без газа
Показания
Формат результата, единицы измерения
Интерпретация результата
Нормальный уровень РЭА не исключает наличие онкологического заболевания иных органов, для которых данный онкомаркер не является специфичным. В большинстве случаев, уровень РЭА отражает состояние толстого кишечника, прямой кишка и ряда других органов.
Важно!
Как и другие онкамаркеры, РЭА не может рассматриваться как единственный диагностический критерий, и никогда не должен выступать в качестве метода самодиагностики онкологии. Так как в последнее время участились случаи оценки онкамаркеров без показаний для этого, без учета рекомендаций врача, мы еще раз уделяем внимание тому факту, что оценка уровня РЭА происходит исключительно в комплексе с результатами других методов исследований для исключения новообразований.
Повышенный уровень РЭА обычно коррелирует с развитием злокачественных изменений толстой и прямой кишки, молочных желез, легких, яичек, простаты, а также при метастазировании в печень и кости. При рецидиве ранее диагностируемого онкологического процесса уровень РЭА также повышается, поэтому динамическое наблюдение в таких случаях очень важно. При ряде неопухолевых заболеваний, а также при доброкачественных опухолях, РЭА также повышается, но обычно превышение нормы незначительно.
Сниженный уровень обычно отмечается в динамике при необходимости контроля РЭА.
Результаты лабораторных исследований не являются единственным критерием, учитываемым лечащим врачом при постановке диагноза и назначении соответствующего лечения, и должны рассматриваться в комплексе с данными анамнеза и результатами других возможных обследований, включая инструментальные методы диагностики.
В медицинской компании «LabQuest» Вы можете получить персональную консультацию врача службы «Doctor Q» по результатам исследований во время приема или по телефону.
Публикации в СМИ
Синдром Рея
Синдром Рея — острая энцефалопатия с отёком мозга и жировой инфильтрацией органов (преимущественно, печени), возникает у ранее здоровых новорождённых, детей и подростков (чаще в возрасте 4–12 лет), часто связан с предшествующей вирусной инфекцией (например, ветряная оспа или грипп А) и приёмом препаратов, содержащих ацетилсалициловую кислоту.
Клиническая картина • Через 6 дней после начала вирусного заболевания (при ветряной оспе — на 4–5 день после появления высыпаний) — тошнота и неукротимая рвота, сопровождающиеся внезапным изменением психического статуса (варьирует от лёгкой заторможённости до глубокой комы и эпизодов дезориентации, психомоторного возбуждения) • Ухудшение состояния больного с угнетением сознания (гипоксическая энцефалопатия): быстрое развитие коматозного состояния с подавлением основных функций жизнеобеспечения (нарушения ритма дыхания, сердечной деятельности, развитие артериальной гипотензии). Темп развития комы прямо определяет возможный прогноз синдрома (начало заболевания с внезапной потери сознания прогностически благоприятнее постепенного, в течение нескольких часов «входа» в кому) • Увеличение печени в 40% случаев, желтуху наблюдают крайне редко • Развитие тромбогеморрагического синдрома (связанного как с ДВС, так и с явлениями печёночной недостаточности) с типичными проявлениями: от необильной петехиальной сыпи и носовых кровотечений до массивных кровотечений, прямо угрожающих жизни больного. Развернутая клиническая картина тромбогеморрагического синдрома всегда прогностически неблагоприятна • Время от момента госпитализации до наступления смерти — 4 дня • Развитие синдрома всегда следует предполагать у ребёнка, симптоматика заболевания у которого представлена внезапной потерей сознания, судорогами и повторной рвотой (необходимо лабораторное обследование для выявления активности АЛТ, ПТИ и содержания глюкозы крови).
Методы исследования • Анализ крови •• Увеличение содержания АСТ и АЛТ более чем в 3 раза •• Нормальное содержание билирубина •• Повышенное содержание аммиака •• Снижение ПТИ •• Снижение концентрации глюкозы в крови •• Повышение давления ликвора без плеоцитоза (8–10 лейкоцитов/мкл) •• Смешанный дыхательный алкалоз и метаболический ацидоз •• Повышение содержания аминокислот (глутамина, аланина, лизина) • ЭЭГ
Дифференциальная диагностика • Сепсис • Гипертермия (особенно у детей до 1 года) • Нейроинфекции (энцефалиты, менингиты) • Острый гепатит • Отравления (например, фосфором) • Врождённые аномалии синтеза мочевины или окисления жирных кислот • Врождённые нарушения углеводного обмена • Аминоацидурии.
ЛЕЧЕНИЕ
Диета. Исключается пероральное питание.
Тактика ведения • Экстренная госпитализация • Постоянное наблюдение за состоянием ЦНС, ССС, дыхательной системы, водно-электролитным балансом • Контроль за ВЧД (экстренная дегидратация диуретиками с целью декомпрессии мозга) • Катетеризация артерий для исследования газового состава крови и её рН, АД • Интубация трахеи и ИВЛ в режиме гипервентиляции.
Лекарственная терапия • Маннитол 0,5–1 г/кг в/в в возрастной дозировке • Введение в/в жидкости и р-ров электролитов, содержащих 5–10% (иногда до 50%) глюкозы • Антибиотики, не всасывающиеся в ЖКТ, например неомицин 100 мг/кг/сут внутрь в 4 приёма • При выраженном тромбогеморрагическом синдроме — инфузии свежезамороженной плазмы, ингибиторы фибринолиза.
Осложнения Основным осложнением синдрома Рея является вклинение вещества мозга в костные образования черепа (большое затылочное отверстие, вырезка намета мозжечка) с остановкой дыхания и сердечной деятельности • Массивные кровотечения.
Прогноз. Летальность — до 80%. У выживших, длительное время пребывавших в коме возможно развитие резидуальных явлений со стороны ЦНС. Рецидивы редки.
Профилактика. Следует избегать назначения салицилатов при лечении детей с вирусными заболеваниями.
Синоним. Белая печёночная болезнь
МКБ-10 • G93.7 Синдром Рейе
Код вставки на сайт
Синдром Рея
Синдром Рея — острая энцефалопатия с отёком мозга и жировой инфильтрацией органов (преимущественно, печени), возникает у ранее здоровых новорождённых, детей и подростков (чаще в возрасте 4–12 лет), часто связан с предшествующей вирусной инфекцией (например, ветряная оспа или грипп А) и приёмом препаратов, содержащих ацетилсалициловую кислоту.
Клиническая картина • Через 6 дней после начала вирусного заболевания (при ветряной оспе — на 4–5 день после появления высыпаний) — тошнота и неукротимая рвота, сопровождающиеся внезапным изменением психического статуса (варьирует от лёгкой заторможённости до глубокой комы и эпизодов дезориентации, психомоторного возбуждения) • Ухудшение состояния больного с угнетением сознания (гипоксическая энцефалопатия): быстрое развитие коматозного состояния с подавлением основных функций жизнеобеспечения (нарушения ритма дыхания, сердечной деятельности, развитие артериальной гипотензии). Темп развития комы прямо определяет возможный прогноз синдрома (начало заболевания с внезапной потери сознания прогностически благоприятнее постепенного, в течение нескольких часов «входа» в кому) • Увеличение печени в 40% случаев, желтуху наблюдают крайне редко • Развитие тромбогеморрагического синдрома (связанного как с ДВС, так и с явлениями печёночной недостаточности) с типичными проявлениями: от необильной петехиальной сыпи и носовых кровотечений до массивных кровотечений, прямо угрожающих жизни больного. Развернутая клиническая картина тромбогеморрагического синдрома всегда прогностически неблагоприятна • Время от момента госпитализации до наступления смерти — 4 дня • Развитие синдрома всегда следует предполагать у ребёнка, симптоматика заболевания у которого представлена внезапной потерей сознания, судорогами и повторной рвотой (необходимо лабораторное обследование для выявления активности АЛТ, ПТИ и содержания глюкозы крови).
Методы исследования • Анализ крови •• Увеличение содержания АСТ и АЛТ более чем в 3 раза •• Нормальное содержание билирубина •• Повышенное содержание аммиака •• Снижение ПТИ •• Снижение концентрации глюкозы в крови •• Повышение давления ликвора без плеоцитоза (8–10 лейкоцитов/мкл) •• Смешанный дыхательный алкалоз и метаболический ацидоз •• Повышение содержания аминокислот (глутамина, аланина, лизина) • ЭЭГ
Дифференциальная диагностика • Сепсис • Гипертермия (особенно у детей до 1 года) • Нейроинфекции (энцефалиты, менингиты) • Острый гепатит • Отравления (например, фосфором) • Врождённые аномалии синтеза мочевины или окисления жирных кислот • Врождённые нарушения углеводного обмена • Аминоацидурии.
ЛЕЧЕНИЕ
Диета. Исключается пероральное питание.
Тактика ведения • Экстренная госпитализация • Постоянное наблюдение за состоянием ЦНС, ССС, дыхательной системы, водно-электролитным балансом • Контроль за ВЧД (экстренная дегидратация диуретиками с целью декомпрессии мозга) • Катетеризация артерий для исследования газового состава крови и её рН, АД • Интубация трахеи и ИВЛ в режиме гипервентиляции.
Лекарственная терапия • Маннитол 0,5–1 г/кг в/в в возрастной дозировке • Введение в/в жидкости и р-ров электролитов, содержащих 5–10% (иногда до 50%) глюкозы • Антибиотики, не всасывающиеся в ЖКТ, например неомицин 100 мг/кг/сут внутрь в 4 приёма • При выраженном тромбогеморрагическом синдроме — инфузии свежезамороженной плазмы, ингибиторы фибринолиза.
Осложнения Основным осложнением синдрома Рея является вклинение вещества мозга в костные образования черепа (большое затылочное отверстие, вырезка намета мозжечка) с остановкой дыхания и сердечной деятельности • Массивные кровотечения.
Прогноз. Летальность — до 80%. У выживших, длительное время пребывавших в коме возможно развитие резидуальных явлений со стороны ЦНС. Рецидивы редки.
Профилактика. Следует избегать назначения салицилатов при лечении детей с вирусными заболеваниями.
Синоним. Белая печёночная болезнь
МКБ-10 • G93.7 Синдром Рейе