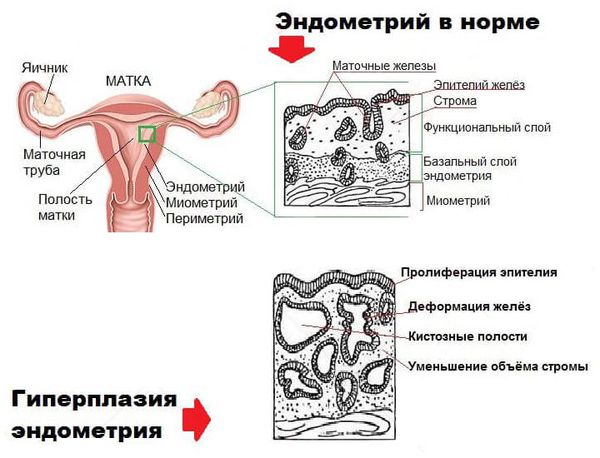
Что такое гиперплазия эндометрия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Анькина А. О., врача УЗИ со стажем в 9 лет.
Определение болезни. Причины заболевания
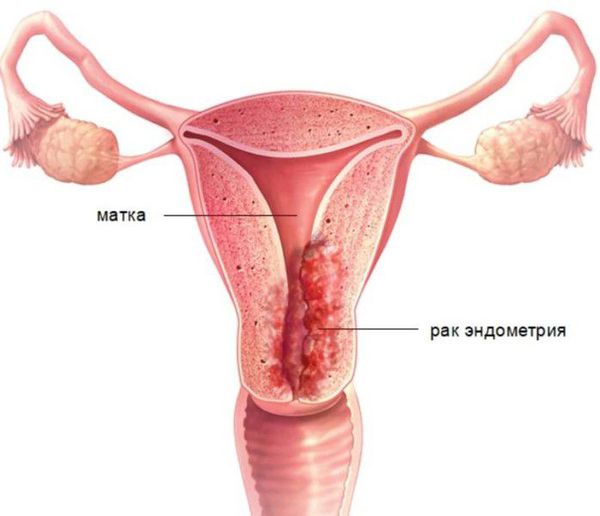
Диагноз « гиперплазия эндометрия » ставится только по заключению гистологического исследования. Без своевременной диагностики и целенаправленного лечения повышается риск развития рака эндометрия.
В составе маточного эндометрия есть специфические рецепторы, которые делают его органом-мишенью для половых гормонов. При гормональном сбое нарушается рост и дифференцировка эндометриальных клеток, что приводит к разрастанию эндометрия.
Факторы риска развития гиперплазии эндометрия [1] [8] [11] :
Симптомы гиперплазии эндометрия
В период перехода к менопаузе основным симптомом заболевания являются нерегулярные обильные менструации, сменяющиеся длительными мажущими кровянистыми выделениями.
Женщины менопаузального возраста жалуются на скудные кровянистые выделения из половых путей. Они могут проявляться эпизодически либо быть продолжительными.
Патогенез гиперплазии эндометрия
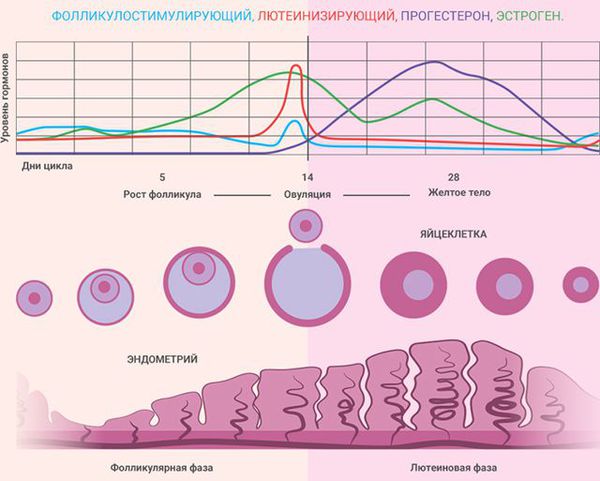
Состояние эндометрия зависит от фазы менструального цикла:
В патогенезе гиперплазии эндометрия выделяют два варианта развития событий:
В случае гиперплазии эндометрия с атипией избыток желёз эндометрия сочетается с клеточными мутациями (атипическим перерождением). Атипическая гиперплазия эндометрия является предраковым состоянием.
Классификация и стадии развития гиперплазии эндометрия
Международная классификация болезней 10-го пересмотра (МКБ-10):
Пересмотренная классификация ВОЗ 2014 года:
Осложнения гиперплазии эндометрия
Анемия. Для гиперплазии эндометрия характерны аномальные маточные кровотечения. В связи с этим женщины часто страдают от хронического малокровия разной степени выраженности.
Бесплодие. Гормональные изменения отражаются на качестве эндометрия, что создаёт риск неудачной имплантации эмбриона. Помимо этого, гиперплазия эндометрия часто выявляется на фоне хронической ановуляции, при которой зачатие невозможно.
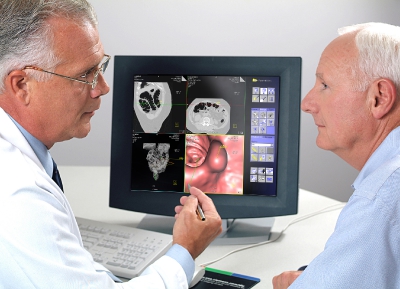
Диагностика гиперплазии эндометрия
Диагностика основана на анализе данных анамнеза пациентки (истории болезни), клинической картины заболевания (жалоб и физикального осмотра), а также на результатах ультразвукового и гистероскопического исследования с обязательным патоморфологическим анализом соскоба из полости матки.
Диагноз «гиперплазия эндометрия» ставится только на основании гистологического исследования материала, полученного при диагностическом выскабливании слизистой оболочки матки или удалении матки.
Анамнез и клиническая картина
При сборе анамнеза врач-гинеколог задаёт пациентке вопросы:
Физикальный осмотр включает в себя местный осмотр наружных половых органов, исследование влагалища и шейки матки в зеркалах, а также бимануальное (двумя руками) исследование матки и придатков. Осмотр проводится на первичном приёме, чтобы исключить воспалительные заболевания и/или объёмные опухолевые образования.
Инструментальная диагностика
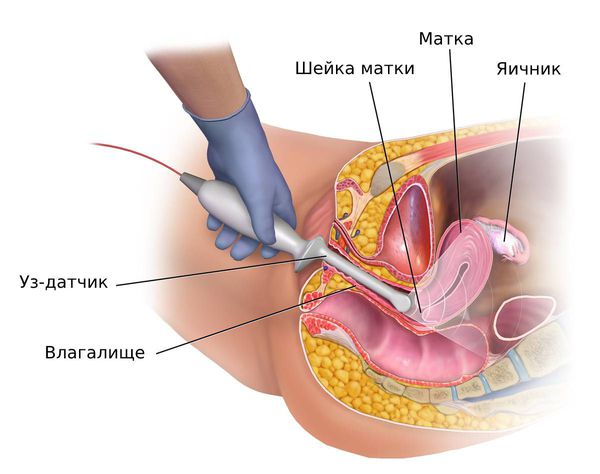
У женщин репродуктивного и пременопаузального возрастов при подозрении на гиперплазию эндометрия ТВУЗИ органов малого таза проводится на 5 – 7-й день менструального цикла. В норме в это время толщина эндометрия не превышает 6 мм. Патологию эндометрия подозревают, когда его толщина не соответствует определённой фазе менструального цикла:
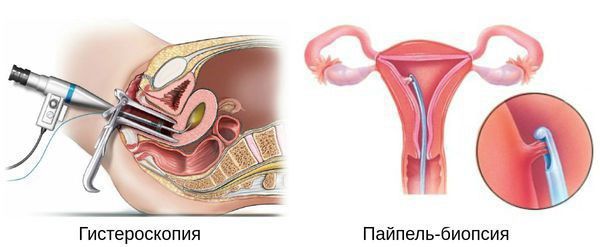
Гистероскопия с раздельным диагностическим выскабливанием (РДВ) матки и цервикального канала — информативный метод в диагностике гиперпластических процессов эндометрия. При помощи гистероскопа (эндоскопического прибора для осмотра полости матки) врач оценивает состояние слизистой оболочки матки и цервикального канала. При необходимости удаляет локальные поражения и обязательно берёт материал для последующего гистологического исследования.
Если выскабливание проводят как лечебную процедуру при обильном маточном кровотечении, врач полностью удаляет слизистую оболочку матки под контролем гистероскопии.
Дифференциальная диагностика гиперплазии эндометрия проводится с полипом эндометрия, субмукозной (подслизистой) миомой матки, эндометритом, прервавшейся беременностью и раком эндометрия.
Лечение гиперплазии эндометрия
Лечение патологии эндометрия основывается на трёх принципах:
Тактика лечения будет зависеть от результата гистологического исследования эндометрия, полученного в ходе выскабливания, от возраста женщины, сопутствующих заболеваний и репродуктивных планов.
Гиперплазия эндометрия без атипии:
Гиперплазия эндометрия с атипией:
Медикаментозное лечение гормональными препаратами проводится пациенткам репродуктивного возраста с неатипической гиперплазией эндометрия при наличии симптомов, факторов риска, отсутствии регресса за 6 месяцев наблюдения и при атипической гиперплазии эндометрия у женщин, планирующих беременность.
Гормональную терапию назначают не менее чем на 6 месяцев:
В качестве негормональной терапии возможно применение препаратов:
Лечение нужно сочетать с низкокалорийной диетой и достаточной физической нагрузкой согласно общему физическому развитию женщины. При необходимости врач назначает препараты, которые нормализуют метаболизм углеводов в организме: подавляют образование глюкозы клетками печени, повышают чувствительность тканей к инсулину, расщепляют сложные сахара.
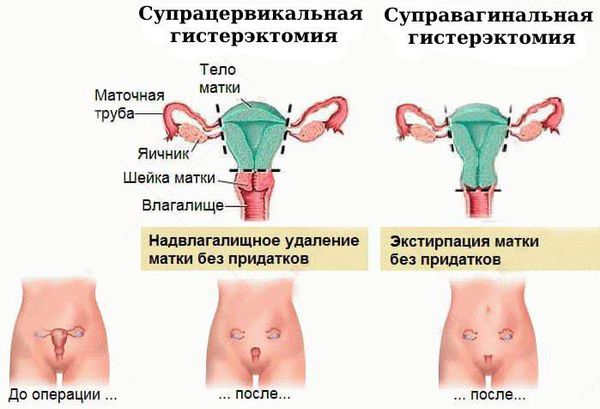
Хирургическое лечение. Атипическая гиперплазия эндометрия на начальном этапе требует обязательной консультации онкогинеколога, который должен установить, нужна ли операция и в каком объёме.
Чаще всего выполняется надвлагалищная ампутация матки — суправагинальная гистерэктомия (удаление тела и шейки матки). Вопрос о сохранении яичников решается строго индивидуально, зависит от возраста пациентки и факторов риска.
Показания к гистерэктомии:
Прогноз. Профилактика
Обследование для исключения гиперплазии или рака эндометрия показано в следующих случаях:
1. Если есть аномальные маточные кровотечения [29] [31] :
2. Если по результатам цитологического исследования соскоба шейки матки отмечается:
Профилактика:
Болезнь крона симптомы и лечение ВЗК кишечника
Под аббревиатурой ВЗК, воспалительные заболевания кишечника, скрываются хронические недуги, имеющие различный характер, но один общий симптом — воспаление стенки кишечника. Причина их появления, к сожалению, пока не выяснена, но распространенность ВЗК во всем мире растет очень быстро. Причем болеют не только люди категории 50+, но и 20–30–летняя молодежь, и даже дети, начиная с 4–5–летнего возраста. Заболевания в равной степени поражают как сторонников активного образа жизни, так и приверженцев здорового питания, придерживающихся диеты с повышенным содержанием клетчатки.
Чем опасно воспаление стенок кишечника?
В последнее время количество россиян с диагностированным ВЗК в среднем ежегодно увеличивается на 10–12%. Чаще всего жители современных мегаполисов страдают от неспецифического язвенного колита и болезни Крона. В первом случае поражается слизистая оболочка толстой кишки, а во втором — окончание тонкой и начало толстой кишки. Воспаление приводит к образованию кровоточащих язв и быстро прогрессирует, при отсутствии диагностики и лечения приводя к необратимым повреждениям тканей.
Даже на начальной стадии заболевания кишечника проявляются неприятными признаками, заметно снижающими качество жизни.
ВЗК у детей: под угрозой — рост и развитие организма
Язвенный колит у детей может проявиться даже в возрасте до года и очень быстро привести к тотальному поражению толстой кишки. При отсутствии лечения болезнь может обернуться серьезным нарушением физиологичного процесса развития детского организма: задержкой роста или отставанием в физическом развитии. Если эндокринная патология при этом не выявляется, хороший детский врач педиатр обязательно назначит ребенку диагностику ЖКТ. Кроме того, и у малышей и у школьников такая патология вызывает серьезные психологические проблемы.
Симптомы заболеваний кишечника: когда нужно обратиться к врачу?
Заболевание часто проявляется интимными признаками, с которыми основная масса больных пытается бороться самостоятельно, не торопясь на платный прием к проктологу или гастроэнтерологу. Кроме того, воспаление кишечника часто сопровождается «маскирующими» симптомами: например, только стоматитом, как при болезни Крона, или только воспалением вокруг ануса — перианальным дерматитом, или поражениями глаз или суставов. Поэтому больной часто попадает к врачу уже с тяжелой формой, когда путь к выздоровлению оказывается и более продолжительным, и более затратным финансово.
Насторожить любого человека должны следующие признаки:
Вероятность поражения толстой и тонкой кишки повышена у людей, регулярно и в больших количествах употребляющих темные сорта мяса и продуктов его переработки (сосиски, колбаса, ветчина, бекон и пр.). Но следует знать, что и приверженность диете с преобладанием овощей, фруктов, продуктов питания, приготовленных из цельного зерна, панацеей не является.
Определенную роль играет генетический фактор: склонность к воспалению кишечника может передаваться по наследству. Среди болеющих преобладают люди, злоупотребляющие курением. Также имеют значение недостаток в организме витамина D, частый и бесконтрольный самостоятельный прием жаропонижающих фармпрепаратов.
Прием проктолога в Москве рекомендован не только людям с неустойчивым стулом. Чтобы не полнить армию больных колоректальным раком, даже здоровый в целом человек после 45 лет должен с профилактической целью посещать врача не реже чем раз в пять лет. Отсутствие видимых признаков воспаления не исключает возможности скрытого протекания заболевания. Выявленные на ранней стадии симптомы рака кишечника позволяют медикам спасти пациента и добиться стойкой ремиссии.
Как диагностируют воспалительные заболевания и рак кишечника?
Специалисты многопрофильной клиники «Трит» владеют всеми методиками, позволяющими выявить даже самые мелкие изменения слизистой кишечника.
«Золотой стандарт» исследования — это современная эндоскопическая методика, колоноскопия кишечника под наркозом. При наличии у пациента внекишечных проявлений заболевания к диагностике привлекаются и врачи соответствующих специальностей — окулист, дерматолог или ревматолог.
Колоноскопия кишечника: оправданы ли опасения пациентов?
Диагностированный на ранней стадии недуг создает меньше всего проблем заболевшему. Поэтому высокоинформативная скрининговая колоноскопия входит в государственные программы борьбы с раком кишечника в США, Израиле и европейских государствах. Граждан развитых стран постоянно информируют о необходимости регулярных обследований для профилактики и ранней диагностики колоректального рака.
Специфика проведения столь интимной процедуры вызывает не самые положительные эмоции у россиян. Боль является основным сдерживающим фактором даже для тех людей, которые полностью осознают необходимость проведения обследования. Но разве можно сравнить возникающие при колоноскопии ощущения с теми мучениями, которые испытывают пациенты, страдающие от уже развившейся онкологии!
Следует понимать, что щадящая технология диагностики, которую можно пройти под наркозом, позволит в дальнейшем избежать опасных симптомов, пугающих диагнозов и проведения солидного комплекса диагностических процедур.
Преимущества эндоскопического обследования в платной клинике
Колоноскопия под наркозом проводится после соответствующей подготовки — соблюдения особой диеты и полного очищения кишечника при помощи сильнодействующих слабительных препаратов.
Будьте внимательны к своему здоровью! Если внезапно проявившиеся проблемы с кишечником не проходят в течение 2–3 недель, обратитесь за консультацией к специалисту.
Интерстициальное заболевание легких
Интерстициальные заболевания легких – группа болезней, поражающих легочную ткань, преимущественно хронического характера. Возникают вследствие поражения альвеолярных мешочков. При отсутствии надлежащего лечения приводят к пневмофиброзу, повреждению альвеолярных стенок, эндотелии легочных капилляров альвеолиту.
Причины возникновения
Сегодня известны три группы причин, провоцирующих возникновение и развитие интерстициальных заболеваний. К ним относятся:
Симптоматика заболевания
Поскольку речь идет сразу о группе болезней легких, единую клиническую картину сформировать нельзя. Однако для всех из них характерно постепенное нарастание симптомов. Если у пациента, например, наблюдается дыхательная недостаточность, со временем она приведет к снижению выносливости. Легкое покашливание перерастет в непрекращающийся, сухой кашель. Также на поздних стадиях практически всегда происходит посинение губ и/или ступней и опухание пальцев рук.
Диагностика и лечение
Интерстициальные заболевания легких можно обнаружить при помощи КТ-сканирования или рентгенографии. На снимке отчетливо видно затемнение легких, наличие в них единичных мелких узелков или целой сетки. В особо запущенных случаях (например, при прогрессирующем пневмофиброзе) можно наблюдать полное или частичное разрушение альвеол и формирование кистозных образований. Из-за них легкие приобретают схожесть с медовыми сотами.
После того, как заболевание обнаружено, наступает очередь анализов. Врач отправляет пациента проверить содержание кислорода в крови и протестировать работу легких. В отдельных случаях, если КТ-сканирование не дает однозначных результатов, назначается биопсия. Хирургическим путем из легкого изымается ткань для анализа.
Лечение интерстициальных заболеваний зависит от степени их развития. При относительно легких болезнях (саркоидозе, аллергическом альвеолите экзогенной этиологии) назначают кус противовоспалительных препаратов и противорубцовую терапию. При пневмофиброзе и схожих с ним заболеваниях не обойтись без кислородной терапии и продолжительной реабилитации. В особо тяжелых случаях может потребоваться трансплантация легких.
С каким бы интерстициальным заболеванием легких вы ни столкнулись, пульмонолог медицинского центра «Гармония» сможет помочь. Наша клиника оснащена современным оборудованием, которое позволяет диагностировать болезни на самых ранних стадиях. А опытный врач подберет лечение, подходящее именно вам. Поэтому, если ощущаете, что самочувствие ухудшилось, не затягивайте с визитом. Запишитесь на прием по телефону или через онлайн-форму.
Синдром Альстрема
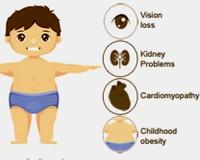
Синдром Альстрема – это генная патология, при которой развивается ожирение, пигментный ретинит, сахарный диабет 2 типа, сенсоневральная тугоухость, кардиопатия, нефропатия. Уже на первом десятилетии жизни отмечается прогрессирующее снижение зрения и слуха, в дальнейшем присоединяется инсулинорезистентность, артериальная гипертензия, сердечная недостаточность, протеинурия, гипогонадизм. Для подтверждения диагноза проводится ЭхоКС, офтальмоскопия, ЭРГ, аудиометрия, биохимия крови, ДНК-диагностика. Лечение симптоматическое: диета, сахароснижающие препараты, ингибиторы АПФ, подбор слухового аппарата, тонированных линз.
МКБ-10
Общие сведения
Синдром Альстрема относится к редким генетическим расстройствам с низкой популяционной частотой (менее 1 случая на 1 000 000 населения). В настоящее время в международном реестре зарегистрировано свыше 1050 таких пациентов более чем из 60 стран. Описаны случаи рождения 2-3 детей с данным заболеванием в одной семье. Патология стала известна и получила свое название в 1959 г. благодаря шведскому офтальмологу К. Альстрёму, молекулярно-генетическая основа синдрома была открыта в 1997 г. Клиническая значимость генетического нарушения заключается в раннем дебюте и развитии тяжелых системных осложнений.
Причины
Синдром Альстрема связан с аутосомно-рецессивным наследованием копий дефектных генов от обоих родителей, которые выступают бессимптомными носителями мутаций. Ген заболевания ‒ ALMS1 – расположен на коротком плече 2-й хромосомы в локусе 2р13. Продуктом данного гена является одноименный белок, который участвует в формировании микротрубочек и ресничек, транспорте веществ внутри клетки. Синдром Альстрема относят к группе цилиопатий. На данный момент описано несколько десятков мутаций гена ALMS1, которые в гомозиготном состоянии вызывают развитие генетического расстройства.
Патогенез
Ген ALMS1 экспрессируется во многих тканях организма: в большей степени в половых железах, головном мозге, сетчатке глаза, в меньшей – в почках, селезенке, печени. Его мутации приводят к синтезированию дефектного рецепторного белка, вызывающего структурные и функциональные аномалии ресничек – цилий. В результате цилии лишаются возможности выполнять свои сенсорные и двигательные функции в первую очередь в тех органах, где отмечается повышенная экспрессия ALMS1.
Предполагается, что продукция аномального белка в палочках и колбочках сетчатки вызывает ее пигментную инфильтрацию, дистрофию и атрофию нейроэпителия. Дисфункция половых желез сопровождается развитием гипогонадотропного гипогонадизма, поджелудочной железы – нарушением толерантности к глюкозе. Поражение клеточных структур головного мозга, в частности, обонятельной луковицы, приводит к перееданию. Механизм развития некоторых расстройств при синдроме Альстрема остается невыясненным.
Симптомы
Большинство клинических признаков синдрома Альстрема дебютирует уже в раннем детстве, другая часть – в течение первого или второго десятилетия жизни. Наиболее ранние симптомы ‒ светобоязнь и нистагм ‒ появляются к 6-15 месяцам и сигнализируют о прогрессирующей дистрофии сетчатки. Дети с синдромом Альстрема рождаются с нормальной массой тела, но ближе к 1-2 годам у них развивается ожирение. Снижение слуха регистрируется примерно с 5 лет. В любом возрасте и периоде заболевания может возникнуть дилатационная кардиомиопатия.
Между 1,5 и 5 годами возникает инсулинорезистентность, которая к 20-30 годам трансформируется в сахарный диабет второго типа. Характерны и другие эндокринные нарушения: гипотиреоз, у юношей ‒ гипогонадотропный гипогонадизм, крипторхизм, у девушек – аменорея, гирсутизм, СПКЯ, позднее – эндометриоз. Во втором десятилетии развивается гепатолиенальный синдром, нефропатия, макропротеинурия. Возможно недержание мочи.
Рост ребенка до пубертата опережает костный возраст на 1-3 года, однако из-за раннего закрытия зон роста конечный рост обычно бывает ниже, чем в популяции. Из аномалий скелета часто присутствуют нарушения осанки, брахидактилия. Выявляются дефекты верхнего зубного ряда. Из кожных проявлений наиболее типичны черный акантоз, алопеция. Интеллект при синдроме Альстрема, как правило, не снижен, у некоторых пациентов описана ЗПР.
Осложнение
Прогрессирование пигментного ретинита приводит к полной слепоте в возрасте 7-8 лет. Возможно развитие гипергликемии, диабетического кетоацидоза. У всех пациентов отмечается бесплодие. В любом возрастном периоде высок риск внезапной смерти вследствие сердечной недостаточности, обусловленной кардиомиопатией. Почечная недостаточность выступает причиной смерти в зрелом возрасте. Продолжительность жизни обычно не превышает 40 лет.
Диагностика
Ведением пациентов с синдромом Альстрема занимаются врачи разных специальностей: педиатры, окулисты, сурдологи, эндокринологи, кардиологи. При физикальном обследовании у пациентов определяется повышенный ИМТ, избыточное развитие подкожно-жирового слоя, гиперпигментация кожи в складках тела, часто – артериальная гипертензия. Для уточнения диагностической гипотезы выполняется:
Дифференциальная диагностика
Синдром Альстрема необходимо отличать от других генетических и врожденных патологий, протекающих с метаболическими нарушениями, пигментным ретинитом, дисфункцией внутренних органов:
Лечение синдрома Альстрема
Коррекция патологии требует привлечения междисциплинарной команды специалистов. Ввиду отсутствия специфического лечения возможно исключительно проведение симптоматической терапии. Используются поведенческие, медикаментозные, хирургические методы:
Прогноз и профилактика
Продолжительность жизни больных синдромом Альстрема снижена. Причинами гибели становятся тяжелые метаболические осложнения, сердечная и почечная недостаточность. Систематическое наблюдение и выполнение всех врачебных назначений позволяет добиться компенсации симптомов, улучшить качество и продлить жизнь. Профилактика заключается в исключении близкородственных браков, проведении генетического консультирования семей, столкнувшихся с синдромом Альстрема.
Предраковые заболевания желудка
Облигатный предрак — заболевания, на почве которых всегда или в большинстве случаев, если их не лечить, возникает рак. К таким заболеваниям относят каллезную язву желудка, ригидный антральный гастрит, полипы, полипоз желудка.
факультативный предрак — хронические заболевания желудка, при которых рак развивается относительно редко, но чаще, чем У здоровых людей. Это хронический атрофический гастрит, болезнь оперированного желудка, пернициозная анемия, болезнь Менетрие и др.
Национальный раковый конгресс в Японии трактует ряд заболеваний, на фоне которых может возникнуть рак желудка, как фоновые, объединяя в одну группу облигатный и факультативный предрак.
По данным Национального ракового конгресса, рак желудка может развиться на фоне хронического атрофического гастрита в 0-13% случаев, пернициозной анемии — в 0,5-12,3%, хронической язвы желудка — в 1-2%, гиперпластического полипа — в 1-2%, плоской аденомы — в 6-21%, папилловирусной аденомы — в 20-75%, болезни Менетрие — в 5-10%, резекции желудка в анамнезе — в 0,4-7,8% случаев.
С морфологической точки зрения мультицентрически расположенные участки пролиферации атипического эпителия называются дисплазией.
Дисплазия — это нарушение структуры ткани, характеризующееся патологической пролиферацией и атипией эпителия. В слизистой оболочке желудка дисплазия может быть трех степеней (легкая, умеренная и тяжелая).
При дисплазии I и II степени изменения слабо выражены и носят обратимый характер. Изменения же, относящиеся к дисплазии III степени, постоянны и могут рассматриваться как рак in situ. У 40-45% людей в возрасте старше 60 лет в слизистой оболочке желудка происходит перестройка эпителия по кишечному типу — кишечная метаплазия (тонкокишечная, толстокишечная). Толстокишечная метаплазия трактуется как предраковое состояние.
Хронический гастрит — самое распространенное заболевание среди патологии желудочно-кишечного тракта, которое составляет 35% всех болезней органов пищеварения и 85% болезней желудка.
Хронический гастрит — заболевание полиэтиологическое. Существует много причин, вызывающих его, однако в соответствии с этиопатогенезом их можно объединить в три основные группы:
•I группа — инфекционные (экзогенные), связанные с желудочным хеликобактером (гастрит В — бактериальный);
•II группа — эндогенные аутоиммунные, обусловленные образованием антител к обкладочным клеткам желез желудка (гастрит А — аутоиммунный) — атрофический гастрит;
•III группа — экзоэндогенные, связанные с частичными термическими раздражениями, медикаментозными воздействиями выражаются гастродуоденальным рефлюксом (гастрит С — реактивный или химический).
На фоне хронического атрофического гастрита в 0-13% случаев возникает рак желудка.
Клиника. В клинической картине хронического гастрита нет типичных характерных признаков, на основании которых можно было бы распознать те или иные его формы.
Основные жалобы: нарушение аппетита, неприятные ощущения в эпигастральной области, связанные с приемом пищи отрыжка, изжога, тошнота, иногда рвота.
Синдромы желудочной и кишечной диспепсии могут быть в самых различных сочетаниях (чувство переполнения желудка пищей, метеоризм, урчание в животе, тенезмы, запоры, сменяющиеся поносами).
Диагностика. Рентгенологический метод исследования в диагностике хронического гастрита играет относительную роль. Он больше пригоден для выявления язвенного, полипозного и опухолевого поражения желудка. Исключение составляет ригидный антральный гастрит. Решающее значение в распознавании различных форм хронического гастрита принадлежит гастрофиброскопии и гастробиопсии. Диагноз: кишечная метаплазия, дисплазия разной степени выраженности, инфекция, вызванная Helicobacter pylori (HP), — только цитологический и гистологический.
Лечение. К терапевтическим мероприятиям при хроническом гастрите неинфекционной этиологии относятся: устранение основных факторов, способствующих развитию заболевания или поддерживающих его, диетотерапия, седативные средства в период обострений, средства, улучшающие микроциркуляцию и трофику слизистой оболочки, витаминотерапия, санаторно-курортное лечение.
Особого отношения требует инфекционный гастрит, вызванный микроорганизмами Helicobacter pylori. На сегодняшний день учеными мира доказано, что 30-50% населения земного шара — носители HP-инфекции (больной человек или бактерионоситель). HP-бактерии обычно размножаются под слоем слизи над слизистой оболочкой привратника, прикрепляются к апикальной части клеток эпителия, выделяют энзимы — цитотоксины и уреазу, и в эпителии развиваются отек, гиперемия, нарушение трофики, дегенерация клеток слизистой оболочки. Процессы воспаления и атрофии тесно связаны между собой и имеют инфекционно-иммунное происхождение.
В последние 10 лет многих исследователей интересуют проблемы хеликобактериоза и рака желудка. На сегодняшний день доказано, что Helicobacter pylori вырабатывается множество патогенных ферментов и токсинов, некоторые из них могут быть вовлечены в канцерогенез.
•Показана взаимосвязь между наличием HP-инфекции и кишечной метаплазией, разновидность которой — неполная кишечная метаплазия — считается предраковым состоянием.
•Установлено, что HP с помощью энзима экстрацеллюлярной уреазы расщепляет мочевину с образованием аммиака, активизирует процессы перекисного окисления липидов, повышает концентрацию свободных радикалов — производных кислорода, что стимулирует процессы канцерогенеза.
•В экспериментах in vitro показана способность HP стимулировать рост культуры опухолевых клеток.
Рак желудка в большинстве случаев сопровождается инфицированием слизистой оболочки HP; при этом НР-инфекция имеет большую распространенность, чем при язвенной болезни, приобретает характер тотального обсеменения всех отделов желудка, в том числе и самой опухоли.
Хеликобактерный гастрит (гастрит В) требует особого лечения. Чтобы уничтожить эти бактерии, необходимо обязательное применение трех препаратов, обладающих антибактериальной активностью: амоксициллина или ампициллина, производного нитронидазола (метронидазола) и производного нитрофурина (фуразолидона). Базисный препарат — де-нол (соль лимонной кислоты с висмутом).
Язва желудка. Малигнизация рецидивирующих и каллезных язв желудка отмечается у 2-10% больных.
Клиника. В отличие от хронического гастрита хроническая язва желудка имеет довольно четкую клиническую картину.
Наиболее постоянный симптом язвенной болезни — боль, связанная с приемом пищи. Боли могут быть ранними, возникающими либо сразу после приема пищи, либо через 0,5-1 ч, и поздними, наступающими через 2-3 ч после приема пищи и позднее. Иногда боли возникают ночью и проходят после приема пищи (молока).
Для язвенной болезни желудка характерна также сезонность — обострения в осенне-зимние и весенние месяцы, ремиссии в летний период.
Важным симптомом заболевания является изжога; у большей половины больных бывает рвота, тошнота. В рвотных массах — кислая жидкость с примесью пищи. При рубцовых стенозах привратника рвота становится более частой, при этом рвотные массы обильны, с остатками пищи, съеденной накануне. Нередко отмечаются нарушения функции кишечника — запоры часто сменяются поносами.
Диагностика. В распознавании язвенной болезни желудка, кроме клинической семиотики, определенную роль играет исследование желудочного сока. У большинства больных имеет место повышение секреции и кислотообразования. Лишь при длительном течении заболевания, особенно при каллезных язвах, кислотность желудочного сока понижается. Важно также исследование кала на скрытую кровь.
При рентгенологическом исследовании желудка главным симптомом является ниша. Большая ниша с окружающим валом и конвергенцией складок слизистой оболочки указывает обычно на каллезный характер язвы. Отличить доброкачественную язву желудка от злокачественной помогает эндоскопическое, цитологическое исследование, а также множественная биопсия с разных участков язвы.
Лечение. Острые и рецидивирующие язвы в стадии обострения лечатся, как правило, консервативным путем. Обычно для заживления язвы требуется от 4 до 8 нед, а при больших или застарелых язвах — и более длительный промежуток времени. Эндоскопический или рентгеноскопический контроль проводится через 8 нед и до полного заживления. Если полное заживление не наступает, проводится повторная биопсия.
При осложнениях язвы (пенетрация, перфорация, рубцовый стеноз, повторяющиеся кровотечения), отсутствии эффекта от консервативной терапии, частом рецидивировании неосложненной пептической язвы, лишающем больного трудоспособности, подозрении на злокачественную язву желудка показано хирургическое лечение.
Полипы и полипоз желудка. Полипы бывают гиперпластическими и аденоматозными.
Гиперпластические изменения встречаются в 80-90% случаев всех полипозных образований в желудке и относятся к опухолеподобным поражениям. В 10-20% случаев возникают аденоматозные полипы — доброкачественные эпителиальные опухоли. Обычно они имеют вид выступающих в просвет желудка округлых образований, расположенных на тонкой ножке или широком основании.
К числу предраковых относят железистые аденоматозные полипы. Дисплазия разной степени выраженности в аденоматозных полипах отмечается в 40-60% случаев, а дисплазия III степени — в 5-10%. Если гиперпластические полипы перерождаются в рак в 1-2% случаев, то плоская аденома — в 6-21%, а папилловирусная аденома — в 20-75% случаев;
Клиника. Одиночные полипы могут протекать бессимптомно и быть случайной находкой. Клинически они проявляются, как правило, при сопутствующем хроническом гастрите. При распаде опухоли возможны кровотечения, при ущемлении полипа — приступ боли в эпигастрии, тошнота, рвота.
Диагностика. Ведущая роль в распознавании полипоза и полипов желудка принадлежит рентгенологическому и гастроскопическому методам.
Биопсия при эндоскопии позволяет дать цитологическую и морфологическую характеристику полипов.
Лечение. Аденоматозные полипы лечат хирургически. При одиночных полипах возможна эндоскопическая полипэктомия, при множественных — выполняется резекция желудка или гастрэктомия.
Оперированные больные находятся под диспансерным наблюдением. Не реже одного раза в 6 мес проводится эндоскопическое исследование, также периодически комплексное лечение, включающее рациональную диету, витаминотерапию, седативные средства, санаторно-курортное лечение.
Пернициозная анемия (болезнь Аддисона) может быть определена как отсутствие внутреннего фактора Касла, связанное с полной атрофией слизистой оболочки фундального отдела желудка и потерей париетальных клеток. Болезнь диагностируется, когда отмечается полная атрофия слизистой оболочки фундального отдела желудка, как правило, это бывает после 50 лет. На момент обнаружения болезни воспаление в слизистой оболочке отсутствует, т. е. патологический процесс представляет собой атрофию без гастрита.
Некоторые данные указывают на иммунологическую и наследственную основу пернициозной анемии, называемой также гастритом типа А.
При этой болезни в 90% случаев в организме присутствуют антитела к париетальным клеткам желудка; а в 60% случаев — антитела к внутреннему фактору Касла (как блокирующие, так и связывающие его). Анемия обычно развивается постепенно и незаметно, прогрессируя по мере истощения запасов витамина В в печени.
Рак желудка при пернициозной анемии встречается в 0,5-12,5% случаев.
Больные с пернициозной анемией обычно наблюдаются у терапевта и гематолога. Для больных старше 50 лет обязательно эндоскопическое исследование желудка 1 раз в год.
Болезнь Менетрие — поражение желудка неизвестной этиологии, проявляющееся очень большими желудочными складками, большими железами с незначительным их воспалением и кистозным расширением; при этом изредка затрагивается подслизистый слой; часто процесс ограничивается телом и дном желудка (антральный отдел обычно не поражается). Иногда ширина и высота складок достигает 3,5 см. Характерно повышенное слизеобразование, гипосекреция соляной кислоты и пепсина, Уменьшение содержания сывороточных белков, приводящее к появлению гипоальбумических отеков.
Клиника. Характерны боль в эпигастрии, потеря массы тела, тошнота.
Течение заболевания хроническое (ремиссии, обострения), иногда наступает спонтанное выздоровление либо переход в атрофический гастрит.
Болезнь Менетрие, как правило, встречается в возрасте 30-60 лет.
Диагностика. При рентгенологическом и эндоскопическом исследовании выявляются очень крупные складки, которые никогда не переходят на пилорический отдел (показана биопсия на всю толщину складки). В 5-10% случаев развивается рак желудка.
Лечение — консервативное; в случае тяжелой гипоальбуминемии может быть необходимой резекция желудка.
Атрофический гастрит резецированного желудка. Закономерным исходом резекции желудка является развитие хронического гастрита в культе, который сопровождается дисплазией и кишечной метаплазией эпителия вследствие снижения кислотности желудочного сока и заброса желчи в культю желудка.
Рак культи желудка возникает у 0,4-7,8% больных из числа оперированных по поводу неопухолевых заболеваний желудка через 10, 15, 20 лет после операции.
Пациенты с резецированным желудком нуждаются в постоянном диспансерном наблюдении на протяжении всей жизни. Один раз в год им должно выполняться гастроскопическое обследование культи желудка.