Наш опыт бифуркационного стентирования коронарных артерий у больных ишемической болезнью сердца с помощью стентов с антипролиферативным покрытием
Закарян Н.В., Панков А.С., Давтян А.Г.
Введение.
Бифуркационные сужения коронарных артерий по праву считаются одним из серьезных вызовов в практике эндоваскулярных хирургов. Несмотря на значительный прогресс при вмешательствах на подобных поражениях, многие вопросы остаются нерешенными. Главной проблемой остается высокая частота рестенозов в отдаленном периоде после стентирования; при этом избыточная пролиферация клеток стенки артерий затрагивает как основную, так и боковую ветви бифуркационных стенозов (1, 2, 3, 8, 10).
В современных условиях большинство интервенционных хирургов придерживается стратегии провизионального (“provisional”) Т-стентирования бифуркационных поражений. Суть техники заключается в имплантации стента в основную ветвь коронарной артерии с последующей одномоментной ангиопластикой по технике “kissing balloons” основной и боковой ветвей. Дополнительный стент в боковую ветвь устанавливается только в случае субоптимального ангиографического результата после “kissing”-дилатации (наличие резидуальных сужений или диссекций в боковой ветви). Тем не менее, существуют анатомические варианты, при которых предпочтительнее выглядят другие эндоваскулярные методики. Так, в случае наличия крупной боковой ветви в сочетании с поражением проксимальной трети этой артерии, выходящего за пределы устья, рекомендовано стентирование обеих ветвей. Наиболее частыми техниками бифуркационных вмешательств в такой ситуации являются “crush-”, “V-”, “kissing stent” и “culotte” – стентирование. На рис. 2 показаны данные исследований, сравнивающие отдаленные результаты использования подобных методик с результатами провизионального стентирования.
В ряде исследований продемонстрировано, что использование стентов с антипролиферативным покрытием способствует снижению риска развития рестенозов, а также уменьшению частоты повторных реваскуляризаций и неблагоприятных кардиальных событий по сравнению с непокрытыми стентами. Так, в рандомизированном исследовании SCANDSTENT показано, что частота кардиальных осложнений в отдаленном периоде (на протяжениии 3 лет) после бифуркационного стентирования коронарных артерий составляет 19, 3% при использовании стентов, покрытых сиролимусом, и 36, 5% при применении непокрытых устройств (3).
В последние годы на рынке появилось много различных стентов с антипролиферативным покрытием. Все ли они эффективны при коррекции бифуркационных поражений? В работе Latib et al. (2008) проводилось сравнение двух наиболее распространенных типов стентов – покрытых сиролимусом (“Cypher”) и паклитакселем (“Taxus”) при вмешательствах на коронарных бифуркациях. В этой работе отмечено, что существенной разницы между этими видами стентов по частоте рестеноза, тромбоза и уровню кардиальных осложнений в отдаленном периоде (3 года) после выполнения операций нет. Так, частота рестеноза в группе стентов с сиролимусом составила 20, 9% против 25, 9% в группе стентов, покрытых паклитакселем; частота кардиальных осложнений – 26, 7% против 25%, частота повторной реваскуляризации стентированных артерий – 12, 9% и 15, 1% соответственно (4). Сходные результаты получены и в других работах (3, 5).
По данным большинства исследований, использование стентов с антипролиферативным покрытием эффективнее непокрытых стентов практически во всех случаях бифуркационного стентирования (2, 7, 9). Продолжают вызывать споры некоторые ситуации, при которых отчетливого превосходства стентов с покрытием не было получено:
1) при острых инфарктах миокарда с сопутствующим высоким риском последующего тромбоза стента;
2) у пациентов с противопоказаниями к продолжительной двойной антиагрегантной терапии;
3) в случае короткого по длине поражения в крупной основной ветви (при анатомическом варианте, когда бифуркация не является истинной)
В отечественной литературе встречаются лишь единичные работы, посвященные изучению эффективности эндоваскулярных вмешательств у больных с бифуркационными поражениями коронарных артерий. Таким образом, проблема выбора стратегии эндоваскулярного лечения при данной патологии является чрезвычайно актуальной и требует дальнейшего изучения.
Материал и методы.
С мая 2004 г. по май 2015 г. в отделении рентгенохирургических методов исследования и лечения ФГУ “Клиническая больница №1” УД Президента РФ было выполнено 362 стентирования бифуркационных поражений коронарных артерий у 351 больного ИБС. Средний возраст пациентов составил 63 + 18 года, 224 (63, 8%) больных были мужского пола, 127 (36, 2%) – женского. У 319 (90, 9%) пациентов до вмешательства наблюдалась стабильная стенокардия 1-4 ФК по классификации ССS, стентирование при остром коронарном синдроме проводились у 32 (9, 1%) больных. Длительность клиники стенокардии варьировала от 2 месяцев до 6, 5 лет, в среднем составив 4 + 2, 1 года. Наличие сахарного диабета в анамнезе было отмечено у 31 (8, 8%) больного. Пациентов с фракцией выброса левого желудочка менее 40% было 20 (5, 7%). В анамнезе у 35 (10%) пациентов имелись эндоваскулярные вмешательства на коронарных артериях; операции коронарного шунтирования ранее проводились 4 (1, 1%) пациентам. Признаки хронической сердечной недостаточности различных степеней были обнаружены у 243 (69, 2%) больных (по классификации Нью-Йоркской ассоциации сердца).
Чаще всего выполнялось стентирование бифуркационных поражений передней межжелудочковой ветви (ПМЖВ) и диагональной ветви (ДВ) левой коронарной артерии – всего 256 (70, 7%) из 362 случаев. Огибающая артерия (ОА) и ее ветви (ВТК, ЗБВ, ЗМЖВ) были стентированы в 42 (11, 6%) случаях, правая коронарная артерия (ПКА) и ее ветви (ЗБВ, ЗМЖВ, ВОК) – в 31 (8, 6%). Также нами было проведено стентирование 33 (9, 1%) бифуркационных поражений, локализованных в стволе ЛКА (в сочетании с устьевыми поражениями ПМЖВ, ОВ или а. intermedia). Согласно классификации Medina, 284 (78, 5%) бифуркационных сужений из 362 являлись истинными.
Провизиональное Т-стентирование выполнялось в 324 (89, 5%) случаях (в 310 случаях – стентирование только основной ветви, в 14 – имплантация еще одного стента в боковую ветвь). Причинами установки дополнительных стентов оказались диссекция боковой ветви у 5 пациентов и субоптимальный результат после “kissing”-дилатации в 9 случаях. Стентирование по технике “culottes” было проведено у 21 (5, 8%) больного, по методике “crush”- у 13 (3, 6%). Относительно редко (у 4 (1, 1%) пациентов) нами применялось “V”-стентирование. В 356 (98, 3%) случаях после всех типов бифуркационных стентирований нам удалось выполнить финальную “kissing”-дилатацию, что является достаточно высоким показателем даже по сравнению с опытом ведущих мировых клиник. В 6 (1, 7%) случаях воспользоваться данной методикой не представилось возможным, т. к. у 4-х пациентов не удалось провести проводник в боковую ветвь через ячейки раскрытого стента, еще у 2-х больных возникли затруднения с доставкой в боковую ветвь баллонного катетера.
Результаты и обсуждение.
Хороший непосредственный клинический результат (отсутствие или уменьшение функционального класса стенокардии) был достигнут у 345 (98, 3%) из 351 пациента. Госпитальная летальность составила 0, 6%. У одного больного после провизионального стентирования бифуркации ПМЖВ-ДВ через несколько часов в реанимационном отделении развился обширный инсульт, через неделю пациент скончался. Еще один пациент с острым инфарктом миокарда скончался на следующий день после операции ввиду исходно тяжелого состояния, несмотря на технически успешно проведенное стентирование бифуркации ПМЖВ-ДВ. Нефатальные осложнения были представлены пульсирующими гематомами в области пункции. Всего было зафиксировано 11 (3, 1%) подобных осложнений, все они были корригированы консервативно с помощью мануальной компрессии.
В отдаленном периоде в сроки от 6 до 52 месяцев коронарография выполнялась 74 (21, 1%) пациентам. Отсутствие рестеноза в области стентированных бифуркационных сегментов было зафиксировано у 51 (68, 9%) пациентов. Клинически незначимые рестенозы были выявлены у 8 (10, 8%) пациентов. Во всех случаях они развивались в области устьев боковых ветвей и не требовали повторных вмешательств. Рестенозы, которые вызывали возврат стенокардии, были обнаружены у 15 (20, 3%) обследованных пациентов. Всем этим больным выполнялись повторные эндоваскулярные вмешательства с хорошим ангиографическим и клиническим результатом. У 11 из этих пациентов были проведены повторные баллонные дилатации по методике “kissing” без имплантации стентов с хорошим итоговым результатом. У 4 пациентов возникла необходимость в имплантации дополнительного стента, также с хорошими итоговыми клиническими и ангиографическими результатами.
Частота острых тромбозов составила 0, 6%. У 1 пациента после классического Т-стентирования с имплантацией 2-х стентов через 20 дней развилась клиника нестабильной стенокардии. На контрольной коронарографии был выявлен тромбоз стента в ЗБВ ПКА, экстренно выполнена ТЛБАП ЗБВ и ЗМЖВ ПКА и имплантация дополнительного стента в дистальную треть ПКА. Больной выписался из клиники с отсутствием стенокардии. Через 52 месяца у этого же пациента при контрольной коронарографии выявлены “in-stent” рестенозы ЗМЖВ ПКА 85% и ЗБВ ПКА 75%, по поводу которых выполнена поочередная баллонная дилатация ЗБВ и ЗМЖВ ПКА баллонами высокого давления; ввиду сохранения резидуального стеноза в ЗМЖВ ПКА с переходом на д/3 ПКА имплантирован стент “Promus” с итоговой “kissing”-дилатацией и хорошим результатом. Еще один острый тромбоз развился на 3 сутки у пациента после “crush”- стентирования бифуркации ПМЖВ-ДВ. Больной был экстренно взят в рентгеноперационную, выполнена реканализация и ТЛБАП окклюзированной ПМЖВ с хорошим итоговым результатом.
Заключение.
В нашей работе удалось подтвердить высокую эффективность бифуркационного стентирования коронарных артерий при помощи стентов с антипролиферативным покрытием. Предпочтительной методикой, рекомендованной в большинстве случаев, является провизиональное стентирование основной ветви, в случае необходимости дополняемое стентированием боковой ветви. Используя данный вид вмешательств, мы добились относительно низкой частоты рестенозов в отдаленном периоде при помощи стентов с лекарственным покрытием. При ряде анатомических вариантов мы применяли “crush”, “culottes” и “V”-методики стентирования, которые также характеризовались вполне приемлемыми клиническими и ангиографическими результатами. Тем не менее, окончательное мнение о роли этих методик при стентировании бифуркационных поражений будет сформулировано в дальнейших крупных рандомизированных исследованиях.
Список литературы.
Автор статьи:
Панков Алексей Сергеевич
врач по рентгенэндоваскулярным диагностике и лечению, к.м.н.
Одномоментное хирургическое лечение пациента с сочетанным атеросклеротическим поражением брахиоцефальных и венечных артерий
Шевченко Ю.Л., Попов Л.В., Батрашов В.А., Зайниддинов Ф.А., Федотов П.А.
Цереброваскулярные осложнения являются одними из самых опасных последствий аортокоронарного шунтирования (АКШ), их частота варьирует от 2 до 6%. У 20% пациентов с плановым АКШ выявляется гемодинамически значимый стеноз сонных артерий. При наличии таких стенозов риск развития инсульта при АКШ увеличивается в 4-6 раз.
Своевременно выполненная одномоментная хирургическая реваскуляризация сердца и головного мозга позволяет избежать тяжелых последствий. Пациент И., 58 лет при поступлении предъявил жалобы на приступы давящих болей за грудиной, возникающие при незначительной физической нагрузке (подъем на 2 этаж), купирующиеся приемом нитроглицерина, одышку, головокружение. Из анамнеза известно, что в августе 2007 года пациент впервые отметил боли в области сердца, по этому поводу был госпитализирован с диагнозом «острый инфаркт миокарда».
При ангиографии артерий шеи и головы, стеноз этой артерии подтвержден (рис 4.) При ЭхоКГ: Систолическая функция ЛЖ сохранена, зон акинезии нет. Патологических изменений клапанного аппарата не выявлено. Учитывая наличие у больного гемодинамически значимого поражения двух артериальных бассейнов, принято решение о необходимости выполнения симультанной операции.
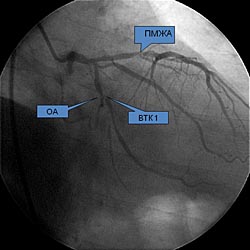 Рис. 1 | 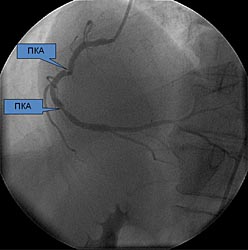 Рис. 2 |
 Рис. 3 | 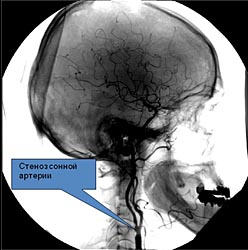 Рис. 4 |
Интраоперационно: просвет сонной артерии резко сужен за счет выраженных атеросклеротических изменений. Выполнена классическая каротидная эндартерэктомия, пластика общей и внутренней сонных артерий синтетической заплатой «Goretex» (рис. 5).
Вторым этапом выполнено аутовенозное АКШ ЗМЖВ ПКА, ОА, ПМЖВ в условиях ИК, тепловой кровяной кардиоплегии (рис 6).
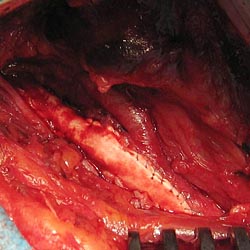 Рис. 5 | 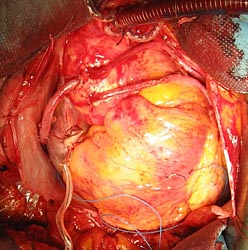 Рис. 6 |
Послеоперационный период протекал без неврологических и кардиологических осложнений, на 8-е сутки пациент выписан под наблюдение врача по месту жительства.
Таким образом, одномоментная хирургическая коррекция поражения венечного и каротидного русла позволяет добиться хорошего клинического эффекта и предотвратить развитие осложнений.
Медицинские интернет-конференции
Языки
Значимость степени стеноза ПМЖВ, обусловленного миокардиальным мостом, в клиническом исходе стентирования проксимального атеросклеротического поражения
Резюме
Ключевые слова
Статья
Введение. Мышечный мост (ММ), частично перекрывающий просвет коронарной артерии, является врожденным анатомическим вариантом и чаще встречается в ПМЖВ. ММ обусловливает развитие ИБС посредством двух независимых механизмов, зависящих от его анатомических особенностей (протяженность, толщина, локализация). Одним из механизмов является прямая механическая компрессия ПМЖВ в момент систолы, способствующая отсрочке диастолической релаксации артерии, снижает резерв кровотока и выраженность перфузии. Второй механизм – усиление прогрессии коронарного атеросклероза, обусловливающего стеноз ПМЖВ проксимальнее ММ, вследствие эндотелиального повреждения на фоне аномальной гемодинамики (ретроградный кровоток к устью ПМЖВ в систолу). Анатомические особенности ММ связаны с выбором тактики и исходом вмешательства у пациентов с ИБС. Так, в случаях стентирования по поводу атеросклеротической бляшки, расположенной проксимальнее ММ, возможно позиционирование части стента в области ММ, что увеличивает частоту отдаленных неблагоприятных исходов, обусловленных, в основном, нарушениями в области стентированного участка ММ. Т.о., анатомические особенности ММ необходимо учитывать при диагностике и выборе тактики лечения ИБС у пациентов, имеющих данную анатомическую особенность.
Цель исследования. Определить влияние степени систолической компресии ПМЖВ, обусловленной ММ, на частоту сердечно-сосудистых событий в ближайшем и отдаленном периоде после стентирования атеросклеротического поражения, расположенного проксимальнее ММ.
Материал и методы. В проспективное исследование было включено 17 пациентов с ИБС, которым в период с января 2012 по август 2013 года было выполнено стентирование ПМЖВ. Критериями включения явились: наличие ММ в средней трети ПМЖВ и стеноза, расположенного проксимальнее ММ. При позиционировании стентов использовалось ВСУЗИ с целью профилактики непреднамеренного стентирования части ММ. Ангиографическая эффективность стентирования оценивалась непосредственно после процедуры, а также по истечении 6 месяцев. Учитывали непосредственные результаты: развитие инфаркта миокарда (ИМ) в ближайшем периоде после стентирования, а также наличие и степень остаточного стеноза. В качестве отдаленных клинических результатов оценивались степень стеноза стента в зависимости от исходной степени систолической компрессией артерии, а также наличие осложнений (инфаркт миокарда, потребность в повторной реваскуляризации в данной локализации, летальные исходы). Наличие и степень остаточного стеноза определяли при контрольной ангиографии и ВСУЗИ непосредственно после стентирования и спустя 6 месяцев. В рамках настоящего исследования были использованы стенты только с лекарственным покрытием.
Неблагоприятных исходов в ближайшем периоде (острых нарушений коронарного кровообращения, диссекций артерии и проч.) в обеих группах зафиксировано не было.
На протяжении 6-месячного наблюдения у пациентов как I, так и II группы, не было отмечено острых коронарных событий или потребности в повторной реваскуляризации миокарда.
В отдаленном периоде частота рестенозов стентов не различалась в группах пациентов с разной степенью систолической компрессии артерии: так, в группе 1 рестеноз имел место у 2 пациентов, а в группе 2 – у 1 пациента (р(c 2 )= 0,55).
Выводы. Обязательным условием при стентировании ПМЖВ, имеющей дистально расположенный ММ, является использование ВСУЗИ для контроля позиционирования стента. Не было выявлено влияния степени систолической компрессии ПМЖВ (более или менее 50%), обусловленной миокардиальным мостом, на частоту неблагоприятных событий после выполнения коронарного стентирования в области проксимально расположенной атеросклеротической бляшки. Необходимо дальнейшее изучение соотношения анатомических параметров ММ и частоты рестенозов стентов, имплантированных по поводу проксимального атеросклеротического поражения ПМЖВ.
Современные методы диагностики и лечения окклюзирующих поражений коронарных артерий
АКТУАЛЬНОСТЬ
ЭТИОЛОГИЯ
ПАТОГЕНЕЗ И ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ
КЛАССИФИКАЦИЯ
ИНСТРУМЕНТАЛЬНАЯ ДИАГНОСТИКА ИБС
1. Электрокардиография
• Скрининговый метод определения наличия ишемии миокарда, очагов некроза и рубцевания, позволяет примерно локализовать зону поражения.
• Стандартная ЭКГ в 12-ти отведениях (чувствительность – 75%) – выявляет острую ишемию миокарда (приступ стенокардии или инфаркт), постинфарктный рубец и нарушения ритма.
• Суточное (холтеровское) мониторирование ( чувствительность – 90%) – фиксирует суточные транзиторные ишемические изменения и нарушения ритма.
• ЭКГ с физической нагрузкой: велоэргометрия и тердмил-тест (чувствительность 50-85%) – выявляет скрытую коронарную недостаточность.
• Чреспищеводная электрокардиостимуляция (чувствительность та же, что и у проб с физической нагрузкой) – альтернатива ЭКГ с физической нагрузкой у больных с хронической артериальной недостаточностью, сердечно-легочной недостаточностью.
• ЭКГ с фармакологическими пробами: нитроглицериновая – положительная динамика на ЭКГ после его приема подтверждает диагноз ИБС; проба с эргометрином в количестве до 0,5мг ступенчато в/в (провоцирует спазм коронаров) – выявляет ишемию миокарда, обусловленную коронароспазмом (спонтанная стенокардия покоя).
2. Ультразвуковая диагностика
• Позволяет диагностировать гипо- и дискинезию сегментов желудочков, толщину стенок и размеры полости желудочков.
• Позволяет диагностировать осложненные формы ИБС: аневризмы, недостаточность митрального клапана, ДМЖП.
• В последние годы разработаны способы ультразвуковой визуализации основного ствола ЛКА и проксимального отдела ПМЖА.
• Допплер-режим позволяет выявить турбулентный поток в полостях сердца при органическом поражении клапанного аппарата, ДМЖП, турбулентный поток крови по ЛКА И ПМЖА.
• Колор-кинезис – цветное картирование зон ишемии миокарда и кардиосклероза.
4. Изотопное сканирование (сцинтиграфия) миокарда.
• Сканирование с изотопом 201Талия (накапливается в капиллярах миокарда) – при ишемии и рубцовых изменениях способность к концентрации снижается.
• После внедрения методики колор-кинезиса отходит на второй план.
ХРОНИЧЕСКАЯ ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА
1. Клиника
• Основные клинические признаки хронической ишемии: периодически развивающийся ангинозный статус, аритмии, признаки сердечной недостаточности.
• Выделяют две формы хронической ИБС: стабильную стенокардию напряжения и спонтанную стенокардию покоя.
• При стабильной стенокардии напряжения ангинозный статус характеризуется загрудинной болью с иррадиацией в левую половину туловища, лица и шеи. Боль четко связана с физической нагрузкой и после ее прекращения проходит не позднее чем через 15 минут (чаще через 1-2 мин). Загрудинные боли легко купируются приемом нитроглицерина. Стабильная стенокардия напряжения характеризуется стабильной клинической картиной (одинаковая физическая нагрузка, одинаковая длительность и частота приступов, одинаковая субъективная характеристика приступов, идинаковые дозы нитроглицерина, необходимые для купирования приступа).
• Наиболее частые нарушения ритма у больных с ИБС: желудочковая экстрасистолия и нарушения проводимости, реже – мерцательная аритмия, пароксизмальная тахикардия.
• Функциональные классы стабильной стенокардии напряжения (Канадская ассоциация кардиологов): I – ангинозный статус возникает только при интенсивных физических нагрузках; II- при ходьбе на расстоянии более 500 м или при поъеме более чем на 1 этаж; III- при ходьбе на расстояние 100-500 метров или при подъеме менее чем на 1 этаж; IV – при ходьбе на расстояние менее 100 м, а также появлении стенокардии напряжения-покоя.
• Спонтанная стенокардия покоя характеризуется возникновением ангинозного статуса вне связи с физической нагрузкой. При этом толерантность к нагрузке или не изменена или даже повышена. Длительность приступа 5-15 минут (максимум до 30 минут). Спонтанная стенокардия обусловлена преходящим спазмом коронарных артерий. Достаточно редко встречается изолированно и в 90% сочетается со стенокардией напряжения (IV ФК). Спонтанная стенокардия, сопровождающая подъемом ST называется вариантной стенокардией (стенокардия Принметалла).
8. Трансмиокардиальная и эндомиокардиальная лазерная реваскуляризация.
• Принцип: с помощью «холодного» лазера создается 30-60 канальцев в миокарде либо трансмиокардиально (на работающем сердце), либо эндомиокардиально (катетером).
• Это альтернатива АКШ у больных с тяжелым поражением дистального русла и низкой фракцией выброса Лж.
НЕСТАБИЛЬНАЯ СТЕНОКАРДИЯ
1. Определение: это острое нарушение коронарного кровообращения без повреждения миокарда, связанное с нестабильностью атеросклеротической бляшки.
2. К нестабильной стенокардии относят:
• Изменение характера ангинозных приступов (особенно длительность свыше 15 минут и необходимость в использовании больших доз нитроглицерина для их купирования), в меньшей степени их частоты и интенсивности.
• Появление приступов стенокардии покоя на фоне имеющейся стенокардии напряжения;
• Впервые возникшая стенокардия (давность до 1 месяца).
• Стенокардия покоя в раннем периоде (первые 2 недели) после ИМ.
• Длительность нестабильной стенокардии – до 30 суток, после которых ее следует называть рефрактерной к консервативной терапии тяжелой стабильной стенокардией.
3. Патогенез
• Нестабильная стенокардия всегда связана с нестабильностью атеросклеротической бляшки. При этом происходит изъязвление, надрыв бляшки, кровоизлияние в бляшку. Все вышеперечисленное приводит к развитию пристеночного тромбообразования и длительного коронароспазма с резким уменьшением просвета коронарной артерии, а также к артериоартериальной эмболии сосудов дистального русла.
4. Диагностика
• Клиника. ЭКГ с обязательным холтеровским монитоированием.
• Нормальные уровни МВ-фракции КФК, АСТ, ЛДГ (в отличие от ИМ).
• Коронарография: выраженный коронароспазм, плохое контрастирование дистального русла, флотирующий тромб в просвете коронарной артерии.
5. Лечебная тактика
• При нестабильной стенокардии больной должен быть госпитализирован в отделение интенсивной терапии на 48 часов (острый период), где ему должна проводится в полном объеме интенсивная терапия как при ИМ. Она включает в/в введение 0,1% нитроглицерина (перлинганит), пероральный прием или в/в введение (изокет) пролонгированных форм нитратов, -адреноблокаторов, антагонистов кальция. Кроме этого должна проводится мощная антитромботическая терапия: гепарин в/в, аспирин или тиклид. При развитии острой сердечной недостаточности обязательно назначить сердечные гликозиды и диуретики. В тяжелых случаях следует подумать о внутриаортальной баллонной контрпульсации.
• Если эффект от лечения получен, то в последующем – плановая коронарография с последующим решением вопроса о возможном методе интервенционном методе лечения.
• Если эффект от лечения отсутствует, то выполняют экстренную коронарографию с последующими интракоронарной фибринолитической терапией и ангиопластикой (обычно на фоне ТАБК). При невозможности выполнить последнюю производится экстренное АКШ.
• Летальность при плановых операциях при НС – 4%, при экстренных – 10%.
ОСТРЫЙ ИНФАРКТ МИОКАРДА
1. Патогенез.
• В подавляющем большинстве случаев причиной ИМ является тромбоз коронарной артерии, меньшую роль отводят длительному коронароспазму и артериоартериальной эмболии.
• В течение первых двух часов (острейший период или период острой ишемии) возможен лизис тромба, тогда некроз миокарда не наступит. К концу первых суток (острый период) гистологически и макроскопически определяется зона некроза миокарда, начинаются процессы воспаления и лизиса некротизированных кардиомиоцитов, через 10 суток (подострый период) развиваются процессы рубцевания и мягкий рубец из грануляционной ткани формируются к концу 4-8 недели, к концу 6 месяца формируется плотный постинфарктный рубец.
• Площадь острой ишемии и некроза определяет возможность развития кардиогенного шока.
2. Клиника и диагностика
• Ангинозный статус более 30 минут, не купируемый приемом нитроглицерина и ненаркотическими анальгетиками.
• Признаки острой сердечной недостаточности (кардиогенный шок, отек легкого) и тяжелые нарушения ритма.
• ЭКГ: дислокация ST, инверсия зубца T, патологический зубец Q (патогномоничный признак), аритмии.
• Повышение МВ-фракции КФК, АСТ, ЛДГ1 и 5 с обязательной нормализацией к 2-3 суткам (КФК), к 4-5 суткам (АСТ и к 10-14 суткам (ЛДГ).
• Лихорадка и лейкоцитоз к концу первых суток и в течение первой недели, и в течение месяца – повышенная СОЭ.
• В постинфарктном периоде обычно развиваются нарушения ритма и хроническая сердечная недостаточность.
4. Лечебная тактика
• Консервативное лечение такое же как и при нестабильной стенокардии. Обязательны -алреноблокаторы и антагонисты кальция (сокращают зону ишемии), адекватное обезболивание наркотическими анальгетиками. При развитии кардиогенного шока – ТАБК. Период нахождения в отделении интенсивной терапии – 10 суток (опасность развития тяжелых осложнений).
• Экстренная интракоронарная фибринолитическая и антитромботическая терапия с последующей баллонной ангиопластикой эффективны если с момента ИМ прошло не более 6 часов.
• АКШ выполняют не ранее чем через 4 месяца после ИМ. Показаниями к экстренному АКШ являются: тромбоз КА во время ангиопластики или коронарографии, кардиогенный шок, трансмуральный ИМ давностью не более 6 часов, ранний рецидив стенокардии после ИМ.
• Летальность при АКШ в сроки до 6 часов – 5%, в более поздние сроки – 10%. 5-летняя выживаемость после ангиопластики и АКШ – 90%, при консервативном лечении – 80%.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ ИБС
1. Постинфарктная аневризма
• Образуется как в остром периоде инфаркта, так и отдаленные сроки. Частота – у каждого пятого после трансмурального инфаркта.
• В 85% формируется из передней или переднебоковой стенки Лж. 5-летняя выживаемость – 20% (смерть от разрыва аневризмы).
• Диагностика: ИМ в анамнезе, хроническая левожелудочковая недостаточность, стенокардия, систолический шум на верхушке, кардиомегалия, эхокардиоскопия, вентрикулография.
• Тактика: абсолютное показание к хирургическому лечению (обычно в сочетании с АКШ, которое предшествует резекции анеризмы). Методы – резекция анеризмы, анеризмораффия и аневризмопликация (при небольших анеризмах).
2. Постинфарктный ДМЖП
• Развивается обычно в остром периоде, при этом выживают 30% больных. Частота- до 2%.
• Диагностика – как врожденные ДМЖП, основной синдром – прогрессирующая сердечная недостаточность.
• Тактика – хирургическое лечение (пластика ДМЖП после АКШ).
3. Постинфарктная недостаточность митрального клапана.
• Развивается либо вследствие инфаркта сосочковых мышц с их последующим разрывом (острая митральная недостаточность), реже – вследствие ишемии сосочковой мышцы (хроническая митральная недостаточность).
• При разрыве сосочковых мышц развивается отек легких и кардиогенный шок, при хронической митральной недостаточности – хроническая левожелудочковая недостаточность.
• Тактика – экстренное или плановое АКШ + протезирование митрального клапана.










