что находится внутри пузырьков во время кипения
Из чего образуются пузыри при закипании воды?
Если вы когда-нибудь кипятили воду, то наверняка заметили, что при нагревании воды образуются очень маленькие пузырьки, которые поднимаются снизу вверх. Сначала пузырьки немногочисленны, но по мере нагревания воды начинает образовываться все больше пузырьков больших размеров. Дальнейшее повышение температуры приводит к появлению еще более крупных пузырьков, которые образуются довольно часто и сразу же поднимаются вверх. Эта эскалация достигает пика, когда вода начинает кипеть.
Но почему кипящая вода образует пузырьки?
Ответ на этот вопрос связан с химией самой воды. Точнее, это связано со всеми растворенными в воде веществами, а также с характером связи между молекулами воды.
Химические свойства молекул воды
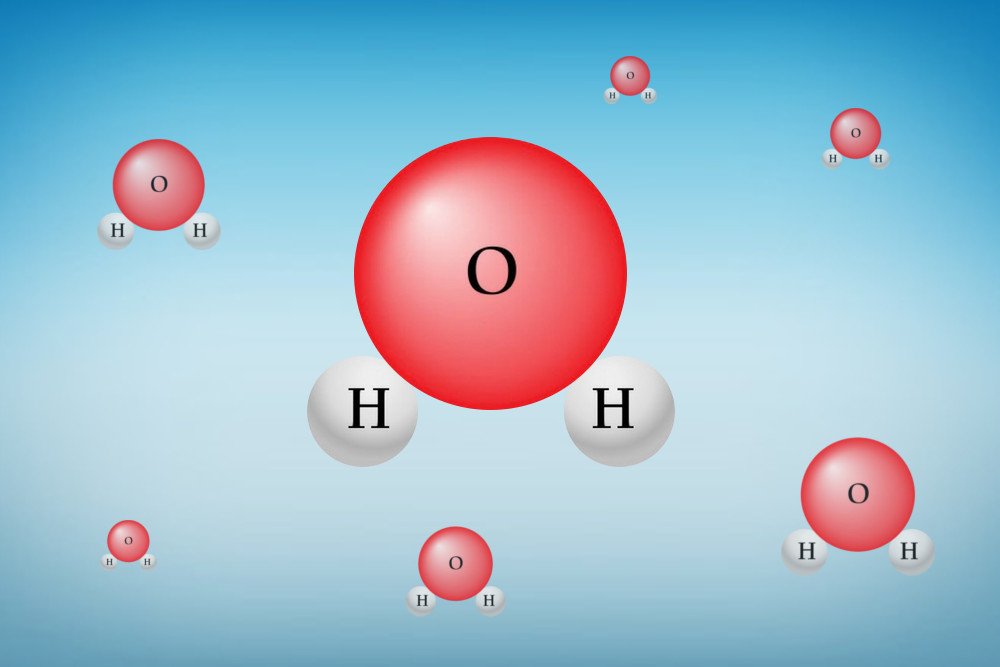
Каждая молекула воды состоит из двух атомов водорода (H) и одного атома кислорода (O). Оба атома H ковалентно связаны с единственным атомом O. Каждый элемент в природе стремится достичь состояния с минимально возможной энергией. Это состояние достигается путем потери или приобретения электронов для достижения ближайшей конфигурации инертного газа.
Иллюстрация молекулы воды
Атом кислорода имеет шесть электронов в своей валентной (внешней) оболочке. Ближайший инертный газ, неон, имеет восемь электронов в своей валентной оболочке. Таким образом, O имеет сильную тенденцию получить два электрона и достичь стабильной электронной конфигурации (перейти в состояние с наименьшей энергией). Водород имеет один электрон в своей валентной оболочке, в то время как ближайший благородный газ, гелий, имеет два электрона на своей валентной оболочке. Таким образом, H стремится получить один электрон, чтобы достичь стабильной электронной конфигурации.
Оба атома H делят по одному электрону с O, а O делит два электрона, по одному на каждый H. Это ковалентная связь. Кислород имеет сильную тенденцию притягивать к себе общие электроны благодаря свойству, называемому электроотрицательностью. Таким образом, электроны проводят больше времени возле атома O, чем возле атома H, что приводит к частичному отрицательному заряду на O и частичному положительному заряду на H.
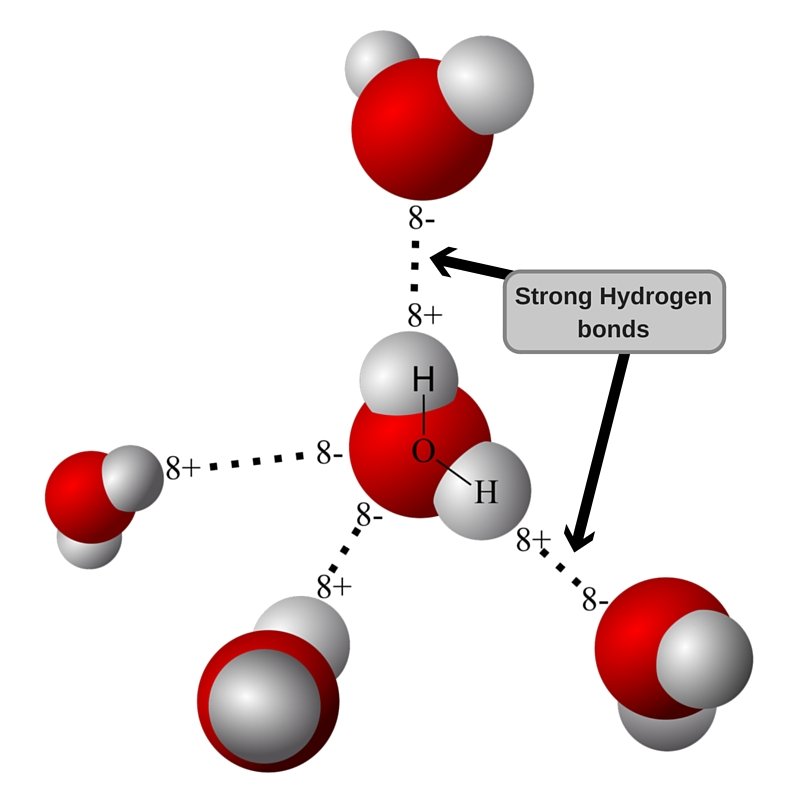
Геометрия молекулы воды такова, что заряды не компенсируются, и есть разделение центров заряда (поляризация). Когда две молекулы воды с небольшой поляризацией приближаются друг к другу, частично отрицательный O одной молекулы притягивает частично положительный H другой молекулы, образуя слабую межмолекулярную связь. Это называется водородной связью, и это сила, отвечающая за удержание молекул воды вместе.
Визуализация водородной связи.
Поскольку водородная связь слабая, вода остается жидкой при комнатной температуре, а при повышении температуры молекулы получают больше энергии для преодоления межмолекулярной водородной связи. При 100 °C энергии достаточно для того, чтобы молекулы вырвались на свободу.
Растворенные вещества в воде
Растворение одного вещества в другом возможно только при наличии взаимодействия между молекулами двух веществ. Подобным образом, некоторые газы, например, O2, CO2, N2, NH3 и SO2, растворяются в воде, потому что между молекулами воды и молекулами газа существует притягательное взаимодействие.
Есть два способа растворения газов в воде: ван-дер-ваальсова связь и водородная связь.
Гетероядерные молекулы (т.е. имеющие атомы из разных элементов), такие, как NH3 или CO2, имеют разницу в электроотрицательности между атомами. N и O более электроотрицательны, чем H и C, соответственно. Таким образом, N и O остаются частично отрицательными, а H и C становятся частично положительными. Это приводит к частичной поляризации молекул NH3 и CO2.
Отрицательные концы (N и O) притягиваются к частично положительному H воды; в то же время положительные концы (H и C) притягиваются к частично отрицательному O воды. Это и есть водородная связь. Чем больше поляризация газообразной молекулы, тем лучше она растворяется в воде.
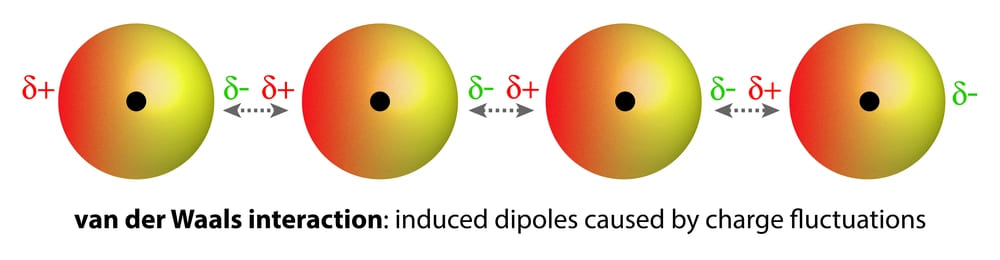
Гомоядерные молекулы (т.е. имеющие атомы одного и того же элемента), такие, как O2 и N2, неполярны и плохо растворимы (очень низкая растворимость) в воде. Слабые ван-дер-ваальсовы силы притяжения удерживают эти газы с молекулами воды. Они намного слабее, чем диполь-дипольные взаимодействия.
Слабые силы Ван-дер-Ваальса возникают из-за изменения распределения заряженных электронов вокруг атомов, что приводит к временной индуцированной поляризации.
Растворимость газов в воде уменьшается при повышении температуры.
Последовательность событий при кипении воды
Молекулы газа, вырывающиеся из воды.
Это бульканье продолжается до тех пор, пока не будет достигнута точка кипения воды. Нагревание воды происходит не совсем равномерно, то есть существуют области более высоких и более низких температур. При температуре выше 90 °С некоторые молекулы воды вблизи дна получают достаточно энергии для перехода в парообразную фазу. Образуются области газообразной воды, о чем свидетельствуют огромные пузыри, поднимающиеся со дна. Кроме того, из-за энергичного движения молекул конвективный нагрев еще больше повышает температуру. При температуре 100 °С почти все молекулы воды обладают достаточной кинетической энергией для перехода в парообразное состояние, и пузырьки водяного пара начинают стремительно подниматься вверх!
Молекулярная физика. Кипение жидкости.
Кипение — это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
В отличие от испарения, которое происходит при любой температуре жидкости, другой вид парообразования — кипение — возможен лишь при совершенно определенной (при данном давлении) температуре — температуре кипения.
При нагревании воды в открытом стеклянном сосуде можно увидеть, что по мере увеличения температуры стенки и дно сосуда покрываются мелкими пузырьками. Они образуются в результате расширения мельчайших пузырьков воздуха, которые существуют в углублениях и микротрещинах не полностью смачиваемых стенок сосуда.
Пары жидкости, которые находятся внутри пузырьков, являются насыщенными. С ростом температуры давление насыщенных паров возрастает, и пузырьки увеличиваются в размерах. С увеличением объема пузырьков растет и действующая на них выталкивающая (архимедова) сила. Под действием этой силы наиболее крупные пузырьки отрываются от стенок сосуда и поднимаются вверх. Если верхние слои воды еще не успели нагреться до 100 °С, то в такой (более холодной) воде часть водяного пара внутри пузырьков конденсируется и уходит в воду; пузырьки при этом сокращаются в размерах, и сила тяжести заставляет их снова опускаться вниз. Здесь они опять увеличиваются и вновь начинают всплывать вверх. Попеременное увеличение и уменьшение пузырьков внутри воды сопровождается возникновением в ней характерных звуковых волн: закипающая вода шумит.
Когда вся вода прогреется до 100 °С, поднявшиеся вверх пузырьки уже не сокращаются в размерах, а лопаются на поверхности воды, выбрасывая пар наружу. Возникает характерное бульканье — вода кипит.
Кипение начинается после того, как давление насыщенного пара внутри пузырьков сравнивается с давлением в окружающей жидкости.
Во время кипения температура жидкости и пара над ней не меняется. Она сохраняется неизменной до тех пор, пока вся жидкость не выкипит. Это происходит потому, что вся подводимая к жидкости энергия уходит на превращение ее в пар.
Температура, при которой кипит жидкость, называется температурой кипения.
Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости. Это объясняется зависимостью давления насыщенного пара от температуры. Пузырек пара растет, пока давление насыщенного пара внутри него немного превосходит давление в жидкости, которое складывается из внешнего давления и гидростатического давления столба жидкости.
Чем больше внешнее давление, тем больше температура кипения.
Всем известно, что вода кипит при температуре 100 ºC. Но не следует забывать, что это справедливо лишь при нормальном атмосферном давлении (примерно 101 кПа). При увеличении давления температура кипения воды возрастает. Так, например, в кастрюлях-скороварках пищу варят под давлением около 200 кПа. Температура кипения воды при этом достигает 120°С. В воде такой температуры процесс варки происходит значительно быстрее, чем в обычном кипятке. Этим и объясняется название «скороварка».
И наоборот, уменьшая внешнее давление, мы тем самым понижаем температуру кипения. Например, в горных районах (на высоте 3 км, где давление составляет 70 кПа) вода кипит при температуре 90 °С. Поэтому жителям этих районов, использующим такой кипяток, требуется значительно больше времени для приготовления пищи, чем жителям равнин. А сварить в этом кипятке, например, куриное яйцо вообще невозможно, так как при температуре ниже 100 °С белок не сворачивается.
У каждой жидкости своя температура кипения, которая зависит от давления насыщенного пара. Чем выше давление насыщенного пара, тем ниже температура кипения соответствующей жидкости, т. к. при меньших температурах давление насыщенного пара становится равным атмосферному. Например, при температуре кипения 100 °С давление насыщенных паров воды равно 101 325 Па (760 мм рт. ст.), а паров ртути — всего лишь 117 Па (0,88 мм рт. ст.). Кипит ртуть при 357°С при нормальном давлении.
Теплота парообразования.
Теплота парообразования (теплота испарения) — количество теплоты, которое необходимо сообщить веществу (при постоянном давлении и постоянной температуре) для полного превращения жидкого вещества в пар.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой r и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты, необходимое для парообразования (или выделяющееся при конденсации). Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования r умножить на массу m:
При конденсации пара происходит выделение такого же количества теплоты:
Учебники
Журнал «Квант»
Общие
Полякова Т., Заблоцкий В., Цыганенко О. Пузыри и вихри в кипящей жидкости //Квант. — 1996. — № 4. — С. 42-44.
По специальной договоренности с редколлегией и редакцией журнала «Квант»
Кипение жидкости — явление, которое мы можем наблюдать практически каждый день. И, казалось бы, увидеть что-либо новое и удивительное в кипении обычной воды невозможно. На самом же деле это довольно сложный и многообразный процесс, который и на сегодняшний день исследован далеко не в полной мере.
Если вы решили проделать этот опыт, но у вас ничего не получилось, не отчаивайтесь. Попробуйте еще раз, изменив интенсивность нагрева или высоту уровня воды в сосуде. Дело в том, что это явление очень капризно к условиям нагревания. (Опыт получается лучше, если нагревание производится при помощи газовой горелки.)
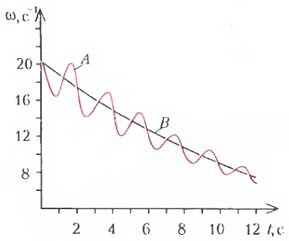
При сравнении кривых A и В возникает по меньшей мере два вопроса. 1) Почему, в отличие от некипящей жидкости, зависимость угловой скорости вращения кипящей жидкости от времени имеет осциллирующий характер? 2) Чем определяется период осцилляции угловой скорости? Чтобы ответить на эти вопросы и разобраться в физике наблюдаемого явления, прежде остановимся на основных закономерностях кипения жидкости, подогреваемой снизу.
Пусть жидкость вращается (целиком, как твердое тело) с угловой скоростью ω. Легко показать, что в этом случае ее свободная поверхность удовлетворяет уравнению
где g — ускорение свободного падения, z и r — обозначены на рисунке 2. Так как давление жидкости на дно сосуда равно \(
p = \rho gz\), из уравнения (1) найдем зависимость давления вблизи дна сосуда как функцию расстояния до оси вращения:
где p0 — давление в центре дна, ρ — плотность жидкости. Если во вращающейся жидкости образовался пузырек пара радиусом R, то он сможет расти только в том случае, когда давление внутри пузыря (pp) будет превосходить сумму внешнего давления (2) и добавочного давления под изогнутой поверхностью жидкости (лапласовского давления), равного \(
\frac<2 \sigma>
\rho \omega^2 rV\), где V — объем пузыря, и направленной к оси вращения, он будет двигаться к центру.
Мы пришли к выводу, что во вращающейся жидкости все пузырьки должны концентрироваться вблизи оси вращения. Поэтому рассмотрим более детально условие роста пузырька, который находится на оси вращения жидкости. Для характеристики степени завихренности течения жидкости (или газа) вводится специальная физическая величина — циркуляция скорости Γ. Вокруг нашего пузырька циркуляция скорости отлична от нуля и равна
\Gamma = 2 \pi \omega R^2.\)
Наличие такой циркуляции означает, что на пузырек (точнее на его «экватор») со стороны жидкости действует отрицательное давление, которое можно выразить через циркуляцию скорости:
Тогда условие роста пузыря будет выполненным, если pp ≥ p1, где
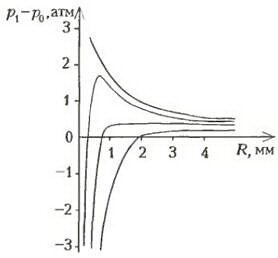
Если построить в соответствии с равенством (3) графики зависимостей p1 от R при различных значениях циркуляции, то получим кривые, приведенные на рисунке 3. Эти кривые показывают, что с возрастанием циркуляции скорости выполнение условия роста пузырька облегчается (условия смягчаются). (Интересно заметить, что давление жидкости, обусловленное ее вращением вокруг пузырька, играет роль, противоположную лапласовскому давлению. Например, для вращающейся воды роль лапласовского давления в процессе кипения будет сведена к нулю при значениях циркуляции Г > 1,5 см 2 /с. А это означает, в частности, что получить перегретую воду, в которой есть вихри с таким значением циркуляции, невозможно.)
Из предыдущих рассуждений и рисунка 3 можно заключить, что вихрь с любым значением циркуляции скорости представляет собой возможный центр образования пузырьков. Именно такие центры и возникают в нашем опыте с вращающейся водой. Поскольку температура воды в сосуде T0 0,1 см) в воде всплывают со скоростью υ ≈ 30 см/с. Поэтому время всплывания пузыря \(
t_1 \approx \frac
что находится в хорошем согласии с опытными данными.
В этой статье мы рассмотрели лишь некоторые аспекты пузырькового кипения жидкости, но и они позволили сделать несколько важных выводов, касающихся этого удивительного явления.
Физика. 10 класс
§ 9-1. Кипение жидкости
В 8-м классе вы узнали, что у жидкости может быть много значений температуры кипения. Дело в том, что в жидкости всегда имеется растворённый в ней газ, с которым тесно связано кипение ( рис. 60.1 ). Если нагревать на плите сосуд с водой, то у его стенок воздух начнёт выделяться в виде пузырьков. В эти пузырьки испаряется вода, поэтому в них в воздухе находится насыщенный водяной пар. С ростом температуры давление насыщенного пара увеличивается гораздо быстрее, чем давление остального газа. Поэтому можно считать, что давление внутри пузырьков в нагретой жидкости практически равно давлению насыщенного пара. На пузырьки, кроме силы тяжести их содержимого, действуют силы гидростатического давления воды и атмосферного давления воздуха. Однако если сосуд не слишком глубокий, то гидростатическое давление значительно меньше атмосферного и им можно пренебречь.
С ростом температуры объём пузырьков быстро увеличивается, что влечёт за собой увеличение выталкивающей силы. Когда сила Архимеда, действующая на пузырёк, становится больше силы тяжести его содержимого, он начинает всплывать ( рис. 60.2 ). Достигнув поверхности жидкости, пузырьки лопаются, поскольку давление насыщенного пара, которым они заполнены, немного превышает внешнее давление. Пар выходит наружу — жидкость кипит. Таким образом, жидкость начинает кипеть при такой температуре, при которой давление насыщенного пара равно (точнее, чуть больше) внешнему давлению.
Перегретую жидкость используют в пузырьковых камерах для визуализации треков заряженных частиц, движущихся со скоростями, близкими к скорости света.
С перегретой жидкостью необходимо обращаться очень осторожно. Любое возмущение (резкое перемещение сосуда, появление источника газа или какого-либо предмета в жидкости) может привести к её немедленному взрывообразному вскипанию.
1. Чем отличается кипение от испарения?
2. При каком условии происходит кипение жидкости?
3. Почему температура кипящей при определённом внешнем давлении жидкости остаётся постоянной?
18.1. Заполните пропуски в тексте.
Существует два способа парообразования: испарение и кипение. В отличие от испарения, кипение – это интенсивный переход жидкости в пар, сопровождающийся образованием пузырьков пара по всему объему жидкости. Температура, при которой жидкость кипит, называют температурой кипения этой жидкости.
18.2. Во время кипения в воде образуются пузырьки. Ответьте на вопросы.
Что находится в пузырьках? Пар
Откуда в пузырьки попадает воздух и водяной пар? Из воды
Какая сила заставляет пузырьки подниматься вверх? Архимедова
Почему возникает шум перед закипанием воды? Из-за попеременного увеличения и уменьшения пузырьков.
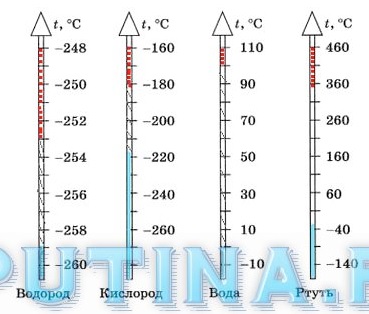
18.3. На каждой температурной шкале закрасьте синим цветом участки температур, при которых указанное вещество находится в твердом состоянии. Штриховкой покажите участок температур, при которых вещество находится в жидком состоянии; участок температур, при которых вещество находится в газообразном состоянии, отметьте точками. Для выполнения задания используйте таблицы 3 и 5 учебника.
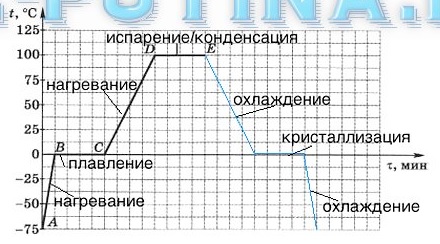
18.4. На рисунке представлен график зависимости температуры вещества от времени при его равномерном нагревании. Известно, что вначале вещество находилось в твердом состоянии.
а) Для каждого участка графика укажите, в каком агрегатном состоянии находится вещество, что с ним происходит и каким образом меняется его внутренняя энергия.
АВ: Вещество твердое; нагревание; внутренняя энергия увеличивается.
ВС: Вещество твердое/жидкое; плавление; внутренняя энергия увеличивается.
CD: Вещество жидкое; нагревание; внутренняя энергия увеличивается.
DE: Вещество жидкое/газообразное; испарение; внутренняя энергия увеличивается (далее возможна конденсация и уменьшение внутренней энергии).
б) Определите по графику, о каком веществе идет речь. Ответ обоснуйте.
Вода, т.к. ее температура плавления составляет 0°С, а испарения 100°С.
в) На рисунке синим цветом продолжите график зависимости температуры вещества от времени при его равномерном охлаждении после отключения нагревательного прибора. Рядом с каждым участком графика напишите название процесса.