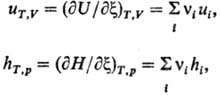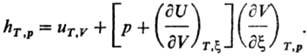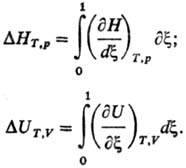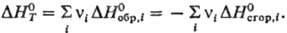что называется тепловым эффектом реакции
Урок №3. Тепловой эффект химических реакций. Экзо- и эндотермические реакции
I. Тепловой эффект химической реакции.
В каждом веществе запасено определенное количество энергии. С этим свойством веществ мы сталкиваемся уже за завтраком, обедом или ужином, так как продукты питания позволяют нашему организму использовать энергию самых разнообразных химических соединений, содержащихся в пище. В организме эта энергия преобразуется в движение, работу, идет на поддержание постоянной (и довольно высокой!) температуры тела.
2 H 2 (г) + O 2 (г) = 2 H 2 О(ж) + 572 кДж
2 H 2 (г) + O 2 (г) = 2 H 2 О(ж) + Q
Реакции протекающие с выделением энергии называются ЭКЗОТЕРМИЧЕСКИМИ (от латинского «экзо» – наружу). Например, горение метана:
CH 4 + 2O 2 = CO 2 + 2H 2 O + Q
C + H 2 O = CO + H 2 – Q
Тепловые эффекты химических реакций нужны для многих технических расчетов.
Тепловые эффекты химических реакций нужны для многих технических расчетов. Представьте себя на минуту конструктором мощной ракеты, способной выводить на орбиту космические корабли и другие полезные грузы (рис.).
Допустим, вам известна работа (в кДж), которую придется затратить для доставки ракеты с грузом с поверхности Земли до орбиты, известна также работа по преодолению сопротивления воздуха и другие затраты энергии во время полета. Как рассчитать необходимый запас водорода и кислорода, которые (в сжиженном состоянии) используются в этой ракете в качестве топлива и окислителя?
В химической промышленности тепловые эффекты нужны для расчета количества теплоты для нагревания реакторов, в которых идут эндотермические реакции. В энергетике с помощью теплот сгорания топлива рассчитывают выработку тепловой энергии.
I. Расчёты по термохимическим уравнениям (ТХУ)
§ 19. Тепловые эффекты химических реакций
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 19. Тепловые эффекты химических реакций |
| Напечатано:: | Гость |
| Дата: | Суббота, 11 Декабрь 2021, 10:17 |
Оглавление
Протекание химических реакций всегда сопровождается выделением или поглощением энергии.
Тепловой эффект реакции — это количество теплоты Q, выделяющейся или поглощающейся в ходе превращения, если количества реагентов (моль) соответствуют стехиометрическим коэффициентам уравнения реакции.
От чего зависит величина теплового эффекта химической реакции?
В качестве примера определим значение теплового эффекта реакции образования оксида азота(II) из простых веществ:
| Уравнение реакции | N2 | + | O2 | = | 2NO |
| Стехиометрическое количество | 1 моль | 1 моль | 2 моль | ||
| Энергия связи | 945 кДж/моль ∙ 1 моль | 494 кДж/моль ∙ 1 моль | 632 кДж/моль ∙ 2 моль | ||
| Изменение энергии | Затрачено на разрыв связей 1443 кДж | Выделилось при образовании связей 1264 кДж | |||
Общий тепловой эффект реакции Q равен сумме тепловых эффектов Q1 и Q2:
Отрицательное значение теплового эффекта показывает, что данная реакция является эндотермической и протекает в соответствии с термохимическим уравнением:
Термохимическими называют уравнения, в которых указаны значения тепловых эффектов.
Для осуществления эндотермических реакций необходимо постоянно передавать системе энергию в виде теплоты, электромагнитного излучения (свет, ультрафиолетовое излучение), электричества и др. Так, эндотермические реакции либо протекают при высоких температурах (например, разложение карбонатов, нитратов и гидроксидов щёлочноземельных металлов), либо требуют подведения электрической энергии (электролиз, образование NO в грозовом разряде) или энергии света (образование озона в атмосфере под действием ультрафиолетового излучения). Эндотермическим процессом является фотосинтез, в котором энергия солнечного света поглощается и запасается в виде химической энергии продуктов — кислорода и глюкозы:
Экзотермические реакции либо не требуют нагревания, либо для начала реакции нужно небольшое нагревание: например, водород со фтором реагирует мгновенно, а для взаимодействия водорода с кислородом смесь газов необходимо нагреть.
Величина теплового эффекта реакции определяется экспериментально в специальном приборе — калориметре, уже знакомом вам по урокам физики в 8-м классе. Результаты измерений приводят к определённым условиям. Обычно это давление 100 кПа и температура 25 °С ( 298,15 K ), что необходимо для сравнения и обобщения экспериментальных данных.
Рассмотрим примеры термохимических расчётов.
Пример 1. Рассчитайте количество теплоты, выделяющейся в результате полного сгорания в кислороде метана объёмом 6,72 м 3 ( н. у. ) в соответствии с термохимическим уравнением:
Тепловой эффект химической реакции
Тепловой эффект химической реакции или изменение энтальпии системы вследствие протекания химической реакции — отнесенное к изменению химической переменной количество теплоты, полученное системой, в которой прошла химическая реакция и продукты реакции приняли температуру реагентов.
Чтобы тепловой эффект являлся величиной, зависящей только от характера протекающей химической реакции, необходимо соблюдение следующих условий:
Содержание
Стандартная энтальпия образования (стандартная теплота образования)
Под стандартной теплотой образования понимают тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях.
Например, стандартная энтальпия образования 1 моль метана из углерода и водорода равна тепловому эффекту реакции:
Энтальпия образования простых веществ принимается равной нулю, причем нулевое значение энтальпии образования относится к агрегатному состоянию, устойчивому при T = 298 K. Например, для йода в кристаллическом состоянии ΔHI2(тв) 0 = 0 кДж/моль, а для жидкого йода ΔHI2(ж) 0 = 22 кДж/моль. Энтальпии образования простых веществ при стандартных условиях являются их основными энергетическими характеристиками.
Тепловой эффект любой реакции находится как разность между суммой теплот образования всех продуктов и суммой теплот образования всех реагентов в данной реакции (следствие закона Гесса):
Термохимические эффекты можно включать в химические реакции. Химические уравнения в которых указано количество выделившейся или поглощенной теплоты, называются термохимическими уравнениями. Реакции, сопровождающиеcя выделением тепла в окружающую среду имеют отрицательный тепловой эффект и называются экзотермическими. Реакции, сопровождающиеся поглощением тепла имеют положительный тепловой эффект и называются эндотермическими. Тепловой эффект обычно относится к одному молю прореагировавшего исходного вещества, стехиометрический коэффициент которого максимален.
Температурная зависимость теплового эффекта (энтальпии) реакции
Чтобы рассчитать температурную зависимость энтальпии реакции, необходимо знать мольные теплоемкости веществ, участвующих в реакции. Изменение энтальпии реакции при увеличении температуры от Т1 до Т2 рассчитывают по закону Кирхгофа (предполагается, что в данном интервале температур мольные теплоемкости не зависят от температуры и нет фазовых превращений):
Если в данном интервале температур происходят фазовые превращения, то при расчёте необходимо учесть теплоты соответствующих превращений, а также изменение температурной зависимости теплоемкости веществ, претерпевших такие превращения:
где ΔCp(T1,Tf) — изменение теплоемкости в интервале температур от Т1 до температуры фазового перехода; ΔCp(Tf,T2) — изменение теплоемкости в интервале температур от температуры фазового перехода до конечной температуры, и Tf — температура фазового перехода.
Стандартная энтальпия сгорания
Стандартная энтальпия растворения
Под энтальпией гидратации — ΔHгидр, понимается теплота, которая выделяется при переходе 1 моля ионов из вакуума в раствор.
Стандартная энтальпия нейтрализации
Стандартная энтальпия нейтрализации — ΔHнейтр о энтальпия реакции взаимодействия сильных кислот и оснований с образованием 1 моля воды при стандартных условиях:
HCl + NaOH = NaCl + H2O H + + OH − = H2O, ΔHнейтр° = −55,9 кДж/моль
Стандартная энтальпия нейтрализации для концентрированных растворов сильных электролитов зависит от концентрации ионов, вследствие изменения значения ΔHгидратации° ионов при разбавлении.
Химия. 11 класс
§ 19. Тепловые эффекты химических реакций
Протекание химических реакций всегда сопровождается выделением или поглощением энергии.
Тепловой эффект реакции — это количество теплоты Q, выделяющейся или поглощающейся в ходе превращения, если количества реагентов (моль) соответствуют стехиометрическим коэффициентам уравнения реакции.
От чего зависит величина теплового эффекта химической реакции?
В качестве примера определим значение теплового эффекта реакции образования оксида азота(II) из простых веществ:
| Уравнение реакции | N2 | + | O2 | = | 2NO |
| Стехиометрическое количество | 1 моль | 1 моль | 2 моль | ||
| Энергия связи | 945 кДж/моль ∙ 1 моль | 494 кДж/моль ∙ 1 моль | 632 кДж/моль ∙ 2 моль | ||
| Изменение энергии | Затрачено на разрыв связей 1443 кДж | Выделилось при образовании связей 1264 кДж | |||
Общий тепловой эффект реакции Q равен сумме тепловых эффектов Q1 и Q2:
Отрицательное значение теплового эффекта показывает, что данная реакция является эндотермической и протекает в соответствии с термохимическим уравнением:
Термохимическими называют уравнения, в которых указаны значения тепловых эффектов.
Для осуществления эндотермических реакций необходимо постоянно передавать системе энергию в виде теплоты, электромагнитного излучения (свет, ультрафиолетовое излучение), электричества и др. Так, эндотермические реакции либо протекают при высоких температурах (например, разложение карбонатов, нитратов и гидроксидов щёлочноземельных металлов), либо требуют подведения электрической энергии (электролиз, образование NO в грозовом разряде) или энергии света (образование озона в атмосфере под действием ультрафиолетового излучения). Эндотермическим процессом является фотосинтез, в котором энергия солнечного света поглощается и запасается в виде химической энергии продуктов — кислорода и глюкозы:
Экзотермические реакции либо не требуют нагревания, либо для начала реакции нужно небольшое нагревание: например, водород со фтором реагирует мгновенно, а для взаимодействия водорода с кислородом смесь газов необходимо нагреть.
Величина теплового эффекта реакции определяется экспериментально в специальном приборе — калориметре, уже знакомом вам по урокам физики в 8-м классе. Результаты измерений приводят к определённым условиям. Обычно это давление 100 кПа и температура 25 °С ( 298,15 K ), что необходимо для сравнения и обобщения экспериментальных данных.
Рассмотрим примеры термохимических расчётов.
Пример 1. Рассчитайте количество теплоты, выделяющейся в результате полного сгорания в кислороде метана объёмом 6,72 м 3 ( н. у. ) в соответствии с термохимическим уравнением:
ТЕПЛОВОЙ ЭФФЕКТ РЕАКЦИИ
теплота, выделенная или поглощенная термодинамич. системой при протекании в ней хим. р-ции. Определяется при условии, что система не совершает никакой работы (кроме возможной работы расширения), а т-ры реагентов и продуктов равны. Поскольку теплота не является ф-цией состояния, т. е. при переходе между состояниями зависит от пути перехода, то в общем случае Т. э. р. не может служить характеристикой конкретной р-ции. В двух случаях бесконечно малое кол-во теплоты (элементарная теплота) dQ совпадает с полным дифференциалом ф-ции состояния: при постоянстве объема dQ = = dU(U-внутр. энергия системы), а при постоянстве давления dQ = dH(H-энтальпия системы).
Практически важны два типа Т. э. р.-изотермо-изобар-ный (при постоянных т-ре Ти давлении р) и изотермо-изо-хорный (при постоянных Ти объеме V). Различают дифференциальный и интегральный Т. э. р. Дифференциальный Т. э. р. определяется выражениями:
Интегральный Т. э. р. в расчете на один пробег р-ции (изменение числа молей в-ва равно его стехиометрич. коэффициенту) измеряется в кДж и определяется ф-лами:
Если по условиям проведения р-ции i не зависят от состава (р-ции в неплотных газах, в разб. р-рах), дифференциальный и интегральный Т. э. р. численно совпадают. В противном случае отнесение измеренного Т. э. р. D T,p к изменению числа молей реагента или продукта дает средний Т. э. р. (кДж/моль).
Изучение Т. э. р. составляет важнейшую задачу термохимии. Осн. эксперим. метод -калориметрия. Совр. аппаратура позволяет изучать Т. э. р. в газовой, жидкой и твердой фазах, на границе раздела фаз, а также в сложных биол. системах. Диапазон типичных значений измеряемых Т. э. р. составляет от сотен Дж/моль до сотен кДж/моль. В табл. приводятся данные калориметрич. измерений Т. э. р. нек-рых р-ций. Измерение тепловых эффектов смешения, растворения, разведения, а также теплот фазовых переходов позволяет перейти от реально измеренных Т. э. р. к стандартным.
Важная роль принадлежит Т. э. р. двух типов-теп лотам образования соед. из простых в-в и теплотам сгорания в-в в чистом кислороде с образованием высших оксидов элементов, из к-рых состоит в-во. Эти Т. э. р. приводятся к стандартным условиям и табулируются. С их помощью легко рассчитать любой Т. э. р.; он равен алгебраич. сумме теплот образования или теплот сгорания всех участвующих в р-ции в-в:
Лит.: Мортимер К., Теплоты реакций и прочность связей, пер. с англ., М., 1964; Пригожин И., Дефэй Р., Химическая термодинамика, пер. с англ., Новосиб., 1966; Термические константы веществ. Справочник, под ред. В. П. Глушко, в. 1-10, 1965-82. См. также лит. при статьях Калориметрия, Термохимия. М. Ю. Панов.