с чем реагирует борная кислота
Борная кислота
| Борная кислота | |
|---|---|
 | |
 | |
| Систематическое наименование | Ортоборная кислота |
| Хим. формула | H3BO3 |
| Состояние | твёрдое |
| Молярная масса | 61,83 г/моль |
| Плотность | 1,435 (15 °C) |
| Т. плав. | 170.9 °C, 444 K, 340 °F |
| Т. кип. | 300 °C, 573 K, 572 °F °C |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | |
| ГОСТ | ГОСТ 9656-75 ГОСТ 18704-78 |
| Рег. номер CAS | 10043-35-3 |
| PubChem | 7628 |
| Рег. номер EINECS | 233-139-2 |
| SMILES | |
| Кодекс Алиментариус | E284 |
| RTECS | ED4550000 |
| ChEBI | 33118 |
| ChemSpider | 7346 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
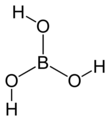
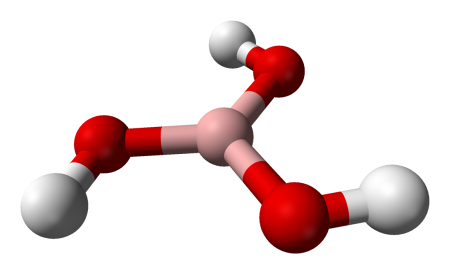
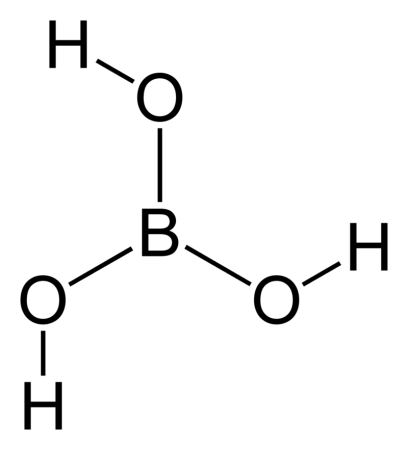
Борная кислота (ортоборная кислота или лат. acidum Boricum ) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
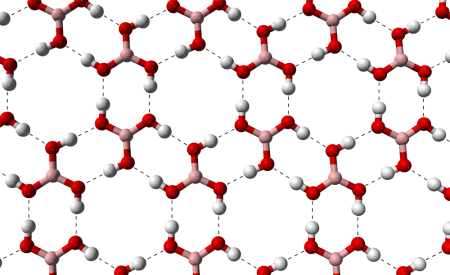
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272 пм. Расстояние между соседними слоями — 318 пм.
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-HBO2 с кубической решёткой, β-HBO2 с моноклинной решёткой и α-HBO2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы H3m-2nВmO3m-n. В природе встречается в виде минерала сассолина.
Содержание
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Получение
Борная кислота может быть получена путём смешения буры (Тетрабората натрия) с минеральной кислотой, например, соляной:
Также является продуктом гидролиза диборана или тригалогенидов бора:
B2H6 + 6H2O → 2H3BO3 + 6H2 BCl3 + 3H2O → H3BO3 + 3HCl 
Борная кислота ОСЧ
Свойства
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной H2B4O7, которая является значительно более сильной кислотой, чем ортоборная.
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведённым).
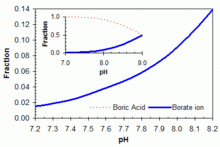
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
Образование борнометилового эфира В(OCH3)3 является качественной реакцией на H3BO3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Борная кислота в медицине
Борный спирт (лат. Solutio Acidi borici spirituosa ) — раствор борной кислоты в этиловом спирте (как правило, в 70 % этаноле).
Спиртовые растворы борной кислоты в концентрации 0,5 %, 1 %, 2 %, 3 %, 5 % готовятся на 70 % этиловом спирте и применяются в качестве антисептика и как противозудное средство при обтирании здоровых участков кожи вокруг очагов пиодермии, а также в качестве ушных капель.
Борная кислота применяется в медицине с 60-х годов XIX века как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
Использование борной кислоты в качестве антисептического средства для детей, а также беременных и кормящих женщин было запрещено 2 февраля 1987 года Министерством здравоохранения СССР по рекомендации Фармакологического комитета с формулировкой: «…запретить использование борной кислоты в качестве антисептического средства у детей грудного возраста, а также у женщин в период беременности и лактации в связи с её низкой активностью и высокой токсичностью».
4,72 г / 100 мл (20 ° C)
5,7 г / 100 мл (25 ° C)
19,10 г / 100 мл (80 ° C)
27,53 г / 100 мл (100 ° C)
умеренно растворим в пиридине,
очень мало растворим в ацетоне
СОДЕРЖАНИЕ
Вхождение
Подготовка
Он также образуется как побочный продукт гидролиза тригалогенидов бора и диборана :
Характеристики
Борная кислота растворима в кипящей воде. При нагревании выше 170 ° C он обезвоживается с образованием метаборной кислоты (HBO 2 ):
или, точнее говоря, в водном растворе:
Борная кислота вносит важный вклад в поглощение низкочастотных звуков в морской воде.
Реакции
Эта функция используется в аналитической химии для определения содержания бора в водном растворе потенциометрическим титрованием сильным основанием, например NaOH.
Борная кислота также растворяется в безводной серной кислоте:
Молекулярная и кристаллическая структура
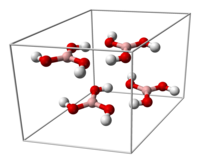 | 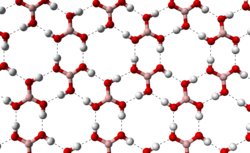 |
| Элементарная ячейка борной кислоты | водородная связь (пунктирные линии) позволяет молекулам борной кислоты образовывать параллельные слои в твердом состоянии |
Токсикология
Согласно отчету CLH по борной кислоте, опубликованному Бюро химических веществ Лодзи, Польша, борная кислота в высоких дозах проявляет значительную токсичность для развития и тератогенность у плодов кроликов, крыс и мышей, а также сердечно-сосудистые дефекты, изменения скелета и легкие почки. поражения. Вследствие этого в 30-м СПС к директиве ЕС 67/548 / EEC от августа 2008 года Европейская комиссия решила изменить свою классификацию как репротоксическую категорию 2 и применить фразы риска R60 (может ухудшить фертильность) и R61 (может нанести вред. будущему ребенку).
На заседании Европейской ассоциации производителей диагностических средств (EDMA) в 2010 году было обсуждено несколько новых дополнений к списку кандидатов на вещества, вызывающие очень большую озабоченность (SVHC) в связи с Правилами регистрации, оценки, авторизации и ограничения химических веществ 2007 года (REACH). После регистрации и проверки, завершенной в рамках REACH, классификация борной кислоты CAS 10043-35-3 / 11113-50-1 с 1 декабря 2010 года указана как H360FD (Может нанести ущерб фертильности. Может нанести вред нерожденному ребенку).
Использует
Промышленные
Борная кислота, смешанная с бурой ( декагидрат тетрабората натрия ) в массовом соотношении 4: 5, хорошо растворяется в воде, хотя по отдельности они не так растворимы. Раствор применяется как антипирен для древесины путем пропитки.
Медицинский
Растворы борной кислоты, используемые для промывания глаз или на истерзанной коже, являются токсичными, особенно для младенцев, особенно после многократного использования; это из-за его низкой скорости выведения.
Инсектицидный
Сохранение
В сочетании с использованием в качестве инсектицида борная кислота также предотвращает и уничтожает существующую влажную и сухую гниль в древесине. Его можно использовать в сочетании с носителем этиленгликоля для обработки внешней древесины от грибков и насекомых. Можно купить стержни, пропитанные боратом, для вставки в древесину через просверленные отверстия, где, как известно, влага и влага собираются и оседают. Он доступен в форме геля и в форме пасты для инъекций для обработки древесины, пораженной гнилью, без необходимости замены древесины. Концентраты препаратов на основе боратов можно использовать для предотвращения роста слизи, мицелия и водорослей даже в морской среде.
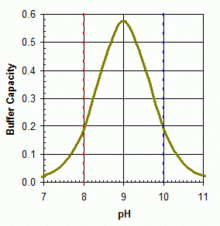
буфер pH
Смазка
Коллоидные суспензии наночастиц борной кислоты, растворенные в нефти или растительном масле, могут образовывать замечательную смазку на керамических или металлических поверхностях с коэффициентом трения скольжения, который уменьшается с увеличением давления до значений в диапазоне от 0,10 до 0,02. Самосмазывающиеся пленки H 3 BO 3 являются результатом спонтанной химической реакции между молекулами воды и покрытиями B 2 O 3 во влажной среде. В объемном масштабе существует обратная зависимость между коэффициентом трения и контактным давлением Герца, вызванным приложенной нагрузкой.
Атомная энергия
Пиротехника
Борная кислота может использоваться в качестве красителя, чтобы сделать огонь зеленым. Например, при растворении в метаноле он обычно используется жонглерами и прядильщиками огня для создания темно-зеленого пламени, намного более сильного, чем сульфат меди.
сельское хозяйство
Борная кислота используется для лечения или предотвращения дефицита бора в растениях. Он также используется для консервирования зерна, такого как рис и пшеница.
Борная кислота
| Борная кислота | |
 | |
 | |
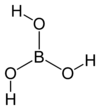 | |
| Общие | |
|---|---|
| Систематическое наименование | Ортоборная кислота |
| Химическая формула | H3BO3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Отн. молек. масса | 61,83 а. е. м. |
| Молярная масса | 61,83 г/моль |
| Плотность | 1,435 (15 °C) г/см³ |
| Термические свойства | |
| Температура плавления | 170.9 °C, 444 K, 340 °F °C |
| Температура кипения | 300 °C, 573 K, 572 °F °C |
| Химические свойства | |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | 2.52 (0 °C) |
4.72 (20 °C)
5,74 (25 °C)
19.10 (80 °C)
27.53 (100 °C)
г/100 мл
Бо́рная кислота́ (ортоборная кислота) — слабая кислота, имеющая химическую формулу H3BO3.
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решетку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями (d= 0,318 нм).
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трех модификациях — наиболее устойчивой γ-НВО2 с кубической решеткой, β-НВО2 с моноклинной решеткой и α-НВО2 с ромбической решеткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n.
Содержание
Свойства

Она легко вытесняется из растворов своих солей большинством других кислот. Соли ее, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная. Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.

Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведенным).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:

Наиболее распространенной солью борной кислоты является декагидрат тетрабората натрия Na2B4O7·10H2O (техническое название — бура).
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Применение
См. также
Примечания
Литература
Полезное
Смотреть что такое «Борная кислота» в других словарях:
борная кислота — В кулинарии применяется как средство против закисания молока, для сохранения свежести пива, мяса. Борная кислота входит в порошок галактофиль для сохранения молока (чайная ложка борной кислоты (сухой), 4 чайные ложки сахарной пудры). На 1 л… … Кулинарный словарь
БОРНАЯ КИСЛОТА — бесцветные, блестящие, чешуйчатые кристаллы; раствор. в воде, спирте и глицерине; употребл., как антисептическое средство. Словарь иностранных слов, вошедших в состав русского языка. Павленков Ф., 1907. БОРНАЯ КИСЛОТА минерал в виде блестящих… … Словарь иностранных слов русского языка
Борная кислота — (ортоборная кислота) (H3BO3) получается или при кислотном разложении природных боратов, или при физико химической обработке неочищенной борной кислоты. Она существует в виде порошка или мелких чешуек, слюдистых хлопьев или стекловидных кусков с… … Официальная терминология
Борная кислота — Действующее вещество ›› Борная кислота (Boric acid) … Словарь медицинских препаратов
БОРНАЯ КИСЛОТА — см. Борные кислоты … Большой Энциклопедический словарь
БОРНАЯ КИСЛОТА — (Н3ВО3), мягкое белое кристаллическое вещество, которое находят в природе в некоторых горячих источниках вулканического происхождения. Его используют в составе металлургических Флюсов как консервирующее, антисептическое средство, а также как… … Научно-технический энциклопедический словарь
борная кислота — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN boric acid … Справочник технического переводчика
БОРНАЯ КИСЛОТА — белый мелкокристаллический порошок. Хорошо растворяется в горячей воде. Обладает слабым дезинфицирующим и вяжущим действием. Применяется в 2 4 процентных водных растворах для полоскания рта, промывания глаз, для примочек и протирания кожи лица. В … Краткая энциклопедия домашнего хозяйства
Борная кислота — БОРНАЯ КИСЛОТА, H3BO3, кристаллы, tпл 170,9°C. Применяют борную кислоту для получения специального стекла, эмалей, цементов, флюсов, моющих и косметических средств, огнезащитных составов, как дезинфицирующее и консервирующее средство, антисептик … Иллюстрированный энциклопедический словарь
Борная кислота
Из Википедии — свободной энциклопедии
наименование

2,52 (0 °C)
4,72 (+20 °C)
5,74 (+25 °C)
19,10 (+80 °C)
27,53 (100 °C)
г/100 мл
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum ) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272 пм. Расстояние между соседними слоями — 318 пм.
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-НВО2 с кубической решёткой, β-НВО2 с моноклинной решёткой и α-НВО2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n. В природе встречается в виде минерала сассолина.