с чем реагирует бромоводородная кислота
Соединения брома
Бромоводород (НBr)
Способы получения бромоводорода
Химические свойства бромоводорода
НВr по физическим и химическим свойствам сходен с HCl, однако молекула НВr менее устойчива, чем HCl.
Восстановительные свойства галогеноводородов усиливаются в ряду HF – HCl – HBr – HI.
Кислородные кислоты и окислы брома
Бромноватистая кислота (HBrO)
HBrO — слабая неустойчивая кислота. В свободном виде не выделена. Максимально полученная концентрация HBrO в водном растворе — 30 %.
Ее соли и сложные эфиры называют гипобромитами.
Получение бромноватистой кислоты
HBrO получается при диспропорционировании брома в воде. Присутствие оксида ртути (II) смещает равновесие в сторону кислоты:
В полученном растворе концентрация бромноватистой кислоты не более 6 %.
Химические свойства бромноватистой кислоты
В темноте также при нагревании выше 60ºС:
3HBrO = HBrO3 + 2HBr
HBrO + NaOH = NaBrO + H2O
Бромистая кислота (HBrO2)
Бромистая кислота HBrO2 —неустойчивое соединение, существует только в водных растворах. Разлагается в течение 4 часов.
Образует соли — бромиты, например бромит бария Ba(BrO2)2•H2O.
Бромноватая кислота (HBrO3)
Бромноватая кислота HBrO3 — бесцветная (или слегка желтоватая) жидкость. В свободном состоянии не выделена, существует в растворе с максимальной концентрацией до 50%. Является сильной кислотой.
Получение бромноватой кислоты
Химические свойства бромноватой кислоты
Cоли бромноватой кислоты – броматы
Наиболее важными являются броматы калия и натрия – это белые вещества, хорошо растворимые в воде. Являются окислителями и слабыми восстановителями
Получение броматов
Химические свойства броматов
Бромная кислота (HBrO4)
Бромная кислота HBrO4 — сильная кислота. Cуществует только в водном растворе с максимальной концентрацией 83%. В свободном виде не выделена, устойчива в растворе с концентрацией менее 55%.
Соли кислоты — перброматы.
Получение бромной кислоты
NaBrO3 + F2 + 2NaOH = NaBrO4 + 2NaF + H2O
Химические свойства бромной кислоты
Соли бромной кислоты – перброматы
Наиболее выжный – пербромат калия. Белое вещество, умеренно растворимое в воде.
Получение перброматов
Химические свойства перброматов
Оксиды брома
Известны оксиды брома — Вr2O, ВrO2 и Вr3O8, которые крайне неустойчивы.
Ни одно из кислородных соединений брома не нашло важного практического применения
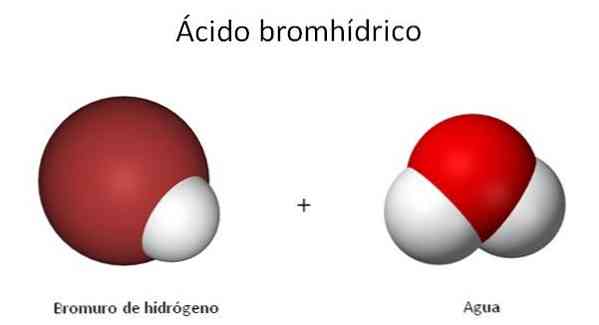
Бромистоводородная кислота — опасный, но важный химический реактив
Бромистоводородная кислота — сильная неорганическая кислота, ее формула HBr. 
В промышленных масштабах вещество получают химической реакцией водорода и брома в процессе нагревания, а так же как побочный продукт органического синтеза бромосодержащих соединений.
Свойства
Кислота хорошо растворяется в воде, спиртовой раствор образует электролит. Термически устойчива, даже при нагревании до 1000 °С на водород и бром разлагается не более полпроцента молекул вещества.
Водный раствор HBr — прозрачная бесцветная или слегка желтоватая жидкость. Желтый цвет раствору придают молекулы Br, образующиеся в процессе реакции вещества с кислородом воздуха. Реактив тяжелее воды, с резким запахом. С точки зрения химии — это одноосновная кислота с восстановительными свойствами. Считается одной из самых сильных кислот, по своей активности сопоставима с соляной кислотой. Реагирует с металлами, оксидами и щелочами с образованием бромидов. В реакции с металлами выделяет водород, который может воспламениться. Бромистоводородная кислота разрушает большинство металлов. Ее смесь с азотной кислотой способна растворять золото и платину.
Меры безопасности

Гост 2062-77 требует, чтобы работы с бромоводородом велись с использованием средств защиты лица, глаз, тела, органов дыхания, в вытяжном шкафу, с учетом правил противопожарной безопасности. Для нейтрализации пролитого реактива используют 10% раствор щелочи или большое количество воды. Для осаждения паров разлитой кислоты разбрызгивают воду. Газ тяжелее воздуха, поэтому при аварийных выбросах скапливается в нижней части помещения, в подвалах, в низинах.
HBr допускается перевозить любым транспортом с соответствующей маркировкой тары знаком опасности по ГОСТ 19433. Газообразная кислота транспортируется в баллонах под давлением 24 атм. Наиболее подходящая тара для хранения водной кислоты — пластиковые канистры.
Применение
— Бромистоводородная кислота, ее газообразная форма и водные растворы разной 
— Реактив используется как катализатор в реакциях алкилирования в органическом синтезе.
— Бромоводород востребован в аналитической химии и микробиологии, в нефтяной и химической индустрии.
В интернет-магазине реактивов и химического оборудования «ПраймКемикалс Групп» можно купить как бромистоводородную кислоту, так и пластиковую и стеклянную тару для нее, а также средства защиты для работы с агрессивными веществами.
Бромистоводородная кислота (HBr) структура, свойства, образование, использование
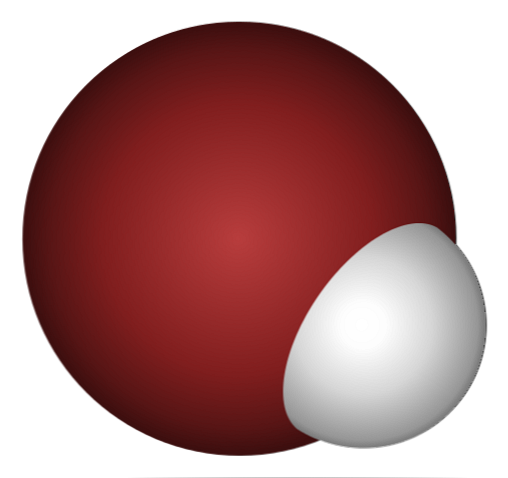
В химических уравнениях он должен быть записан как HBr (ac), чтобы указать, что это бромистоводородная кислота, а не газ. Эта кислота является одной из самых сильных, даже больше, чем соляная кислота, HCl. Объяснение этому кроется в природе его ковалентной связи.
Почему HBr такая кислота и еще больше растворяется в воде? Поскольку ковалентная связь H-Br очень слабая, из-за плохого перекрытия 1s-орбиталей H и 4p Br.
Это неудивительно, если вы внимательно посмотрите на изображение выше, где атом брома (коричневый) явно больше, чем атом водорода (белый).
Бромистоводородная кислота, после HI, является одним из самых сильных и полезных гидроцидов для расщепления определенных твердых образцов..
Структура бромистоводородной кислоты
На изображении показана структура H-Br, свойства и характеристики которого, даже газа, тесно связаны с его водными растворами. Вот почему наступает момент, когда вы вступаете в заблуждение относительно того, на какое из двух соединений намекают: HBr или HBr (ac).
Структура HBr (ac) отличается от структуры HBr, потому что теперь молекулы воды сольватируют эту двухатомную молекулу. Когда это достаточно близко, H передается + к молекуле Н2Или как указано в следующем химическом уравнении:
кислотность
Физико-химические свойства
Молекулярная формула
Молекулярный вес
Внешний вид
Бесцветная или бледно-желтая жидкость, которая будет зависеть от концентрации растворенного HBr. Чем оно более желтое, тем более концентрированным и опасным оно будет.
запах
Порог запаха
плотность
1,49 г / см 3 (водный раствор при 48% мас. / мас.). Эта величина, как и те, которые соответствуют точкам плавления и кипения, зависит от количества HBr, растворенного в воде.
Точка плавления
-11ºC (12ºF, 393ºK) (водный раствор при 49% мас. / Мас.).
Точка кипения
122 ° С (252 ° F, 393 ° К) при 700 мм рт. Ст. (Водный раствор 47-49% мас. / Мас.).
Растворимость в воде
-221 г / 100 мл (при 0 ºC).
-204 г / 100 мл (15 ºC).
-130 г / 100 мл (100 ºC).
Эти значения относятся к газообразному HBr, а не к бромистоводородной кислоте. Как видно, повышение температуры снижает растворимость HBr; поведение, которое является естественным в газах. Следовательно, если требуются концентрированные растворы HBr (ac), лучше работать с ними при низких температурах..
При работе при высоких температурах HBr будет выходить в виде газообразных двухатомных молекул, поэтому реактор должен быть герметично закрыт для предотвращения утечки.
Плотность пара
2,71 (по отношению к воздуху = 1).
Кислотность пКа
-9,0. Эта константа, столь отрицательная, свидетельствует о ее сильной кислотности.
Калорийность
Стандартная молярная энтальпия
198,7 кДж / моль (298 ºK).
Стандартная молярная энтропия
Точка зажигания
номенклатура
В то время как HBr (г), бромистый водород, является безводным; то есть у него нет воды. Поэтому он назван в соответствии с другими стандартами номенклатуры, что соответствует галогеноводородам.
Как это формируется?
Существует несколько синтетических методов приготовления бромистоводородной кислоты. Некоторые из них:
Смесь водорода и брома в воде
Без описания технических подробностей эту кислоту можно получить из прямой смеси водорода и брома в реакторе, заполненном водой..
Фосфор трибромид
В более сложном процессе смешивают песок, гидратированный красный фосфор и бром. Водяные ловушки помещаются в ледяные ванны, чтобы предотвратить выход HBr и образование вместо него бромистоводородной кислоты. Реакции:
Диоксид серы и брома
Это окислительно-восстановительная реакция. Br2 он уменьшает, он получает электроны, связываясь с атомами водорода; в то время как ТАК2 он окисляется, он теряет электроны, когда он образует больше ковалентных связей с другими атомами кислорода, как в серной кислоте.
приложений
Приготовление бромидов
Бромидные соли могут быть получены, если HBr (ac) реагирует с гидроксидом металла. Например, производство бромида кальция считается:
Другой пример для бромида натрия:
NaOH + HBr => NaBr + H2О
Таким образом, многие из неорганических бромидов могут быть получены.
Синтез алкилгалогенидов
А как насчет органических бромидов? Это броморганические соединения: RBr или ArBr.
Обезвоживание спиртов
Сырьем для их получения могут быть спирты. При протонировании кислотностью HBr они образуют воду, которая является хорошей исходящей группой, и вместо этого включается объемный атом Br, который становится ковалентно связанным с углеродом:
ROH + HBr => RBr + H2О
Добавление к алкенам и алкинам
Молекула HBr может быть добавлена из ее водного раствора к двойной или тройной связи алкена или алкина:
RC≡CR + HBr => RHC = CRBr
Можно получить несколько продуктов, но в простых условиях продукт сначала образуется там, где бром связан с вторичным, третичным или четвертичным углеродом (правило Марковникова)..
Эти галогениды вмешиваются в синтез других органических соединений, и диапазон их применения очень широк. Кроме того, некоторые из них могут даже использоваться в синтезе или разработке новых лекарств..
Эфирный кливаж
Из простых эфиров можно получить два алкилгалогенида одновременно, каждый из которых несет одну из двух боковых цепей R или R ‘исходного эфира R-O-R’. Случается что-то похожее на обезвоживание спиртов, но механизм его реакции другой.
Реакция может быть схематизирована с помощью следующего химического уравнения:
ROR ‘+ 2HBr => RBr + R’Br
И вода тоже выделяется.
катализатор
Бромоводородная кислота
Бромоводородная кислота
| Бромоводород | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | бромоводород |
| Химическая формула | HBr |
| Отн. молек. масса | 80,91 а. е. м. |
| Молярная масса | 80,91 г/моль |
| Физические свойства | |
| Плотность вещества | 3.307 г/л, газ (25°C) г/см³ |
| Состояние (ст. усл.) | бесцветный газ |
| Термические свойства | |
| Температура плавления | –86.80 °C |
| Температура кипения | –66.38 °C |
| Критическая точка | 51,4 °C |
| Энтальпия (ст. усл.) | -34,1 кДж/моль |
| Химические свойства | |
| pKa | ≈ –9 |
| Растворимость в воде | 193 (20°C) г/100 мл |
| Классификация | |
| номер CAS | [10035-10-6] |
Бромоводород НВr — соединение брома с водородом. Бесцветный газ, сильно дымит на воздухе. Образуется при взаимодействии паров брома с водородом при высокой температуре.
Хорошо растворим в воде, при растворении протекают следующие процессы:
В лаборатории обычно получают гидролизом бромида фосфора:
Применяют для приготовления бромидов, синтеза различных органических бромпроизводных.
При растворении в воде образуется сильная одноосновная бромоводородная кислота.
Полезное
Смотреть что такое «Бромоводородная кислота» в других словарях:
бромоводородная кислота — (HBr) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN hydrogen bromide … Справочник технического переводчика
бромоводородная кислота — (бромистоводородная кислота), раствор бромоводорода в воде, одна из самых сильных кислот (сильнее, чем соляная кислота). Чистая бромоводородная кислота бесцветная, на воздухе буреет (медленно окисляется, выделяя бром). Сильный восстановитель.… … Энциклопедический словарь
БРОМОВОДОРОДНАЯ КИСЛОТА — (бромистово дородная кислота), р р бромоводорода в воде, одна из самых сильных к т (сильнее, чем соляная кислота). Чистая Б. к. бесцветная, на воздухе буреет (медленно окисляется, выделяя бром). Сильный восстановитель. Соли Б. к. бромиды. Б. к.… … Естествознание. Энциклопедический словарь
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
бромистоводородная кислота — то же, что бромоводородная кислота … Энциклопедический словарь
БРОМИСТОВОДОРОДНАЯ КИСЛОТА — то же,что бромоводородная кислота … Естествознание. Энциклопедический словарь
Кислоты и ангидриды — Служебный список статей, созданный для координации работ по развитию темы. Данное предупреждение не устанавл … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Кислоты — У этого термина существуют и другие значения: Кислота (наркотик) Кислоты один из основных классов химических соединений. Они получили своё название из за кислого вкуса большинства кислот, таких, как азотная или серная. По определению кислота … … Википедия
Бромоводород
Бромоводород (HBr) — соединение брома с водородом. Бесцветный тяжёлый токсичный газ, образует туман в сыром воздухе.
Содержание
Получение
В промышленности бромоводород получают непосредственным взаимодействием простых веществ:
Также бромистый водород получается как побочный продукт при синтезе бромпроизводных органических соединений
В лаборатории получают гидролизом трибромида или пентабромида фосфора:
Восстановление брома несколькими способами:
Вытеснение из бромидов щелочных металлов разбавленной кислотой:
Физические свойства
Хорошо растворим в воде: 221 г/100 г воды при 0 °C (193 при 25°, 130 при 100 °C). Водный раствор образует азеотропную смесь с 47,63 % HBr, которая кипит при 124,3 °C.
Растворяется в этаноле, образуя слабый электролит.
При охлаждении водных растворов HBr можно получить кристаллогидраты:
Чистый HBr образует кристаллы орторомбической сингонии, пространственная группа F mmm, параметры при −173 °C a = 0,5640 нм, b = 0,6063 нм, c = 0,5555 нм, Z = 4.
Химические свойства
Водный раствор бромистого водорода образует сильную одноосновную кислоту:
Термически HBr очень устойчив, при температуре 1000 °C разлагаются около 0,5 % молекул:
Как кислота реагирует с металлами, их оксидами, основаниями:
Является восстановителем, медленно окисляется на воздухе, из-за чего водные растворы со временем окрашиваются в бурый цвет:
Применение
Применяют для приготовления бромидов, синтеза различных органических бромпроизводных и для реактивного ионного травления.
Транспортировка
Безводный HBr транспортируют в баллонах ёмкостью 6,8 и 68 кг под давлением 24 атм.
Токсичность
Бромистый водород — едкое, весьма токсичное вещество, обладающее удушающим действием. Предельно допустимая концентрация = 10 мг/м³, поражающая токсодоза = 2,4 мг/л·мин.