с чем взаимодействует пропионовая кислота
Применение пропионовой кислоты и ее взаимодействие с другими химическими соединениями
Для большинства потребителей добавка E280 ни о чем не говорит, но если копнуть глубже, то можно узнать, что за этим обозначением прячется пропионовая кислота. Она представляет собою бесцветную жидкость с резким запахом. Для этого химического соединения характерно универсальное применение, так как его применяют и в кулинарии, и в производстве пластмасс, и в производстве гербицидов, и даже в фармацевтике.
Особенности химических связей
Если рассматривать это вещество с точки зрения химии, то химическая формула пропионовой кислоты будет: C2H5COOH. Ее вывели с помощью нефти и процесса брожения углеводов. Саму кислоту производят бактерии с одноименным названием. Она выступает завершающим продуктом их жизнедеятельности.
Впервые данное вещество получили на производствах, где изготавливают уксус. Уксусная кислота и пропионовая кислота стали неотъемлемым понятием, потому что пропионовые соединения образуются во время изготовления уксуса.
Также ученые доказали тот факт, что пропионовая кислота может встречаться и на кожных покровах человека. Кроме того, ее обнаружили в желудках жвачных животных. В середине 19 века ее первооткрывателем стал ученый Йохан Готлиб. Получение пропионовой кислоты он обнаружил в процессе разложение сахара, но окончательно раскрыть все «секреты» этого вещества смог только француз Жан-Батист-Дюма. Он, к стати, и дал ее такое название.
Стоит отметить, что данная кислота имеет еще несколько названий, а именно:
В мировой классификации добавок она имеет значение E280.
Свойства кислоты
Чтобы понять – для чего ее добавляют в пищевые продукты, пластмассы или корма для животных, необходимо знать ее свойства. Поэтому ее ключевой характеристикой считается – препятствие размножения и роста различных видов плесени и бактерий.
Такое свойство ценится многими производителями хлебобулочных изделий, растворителей, пластмасс и лекарственных препаратов. Это химическое соединение считается консервантом.
Но, где и в каком количестве можно ее применять? Чтобы ответить на этот вопрос необходимо обращать внимание на законодательную базу той страны, где пропионовая кислота допускается в производственный процесс. Например, в Российской Федерации это вещество считается допустимым в определенном количестве, но в соседней Украине, это вещество запрещено на законодательном уровне.
Взаимодействие с другими химическими соединениями
Реакции пропионовой кислоты получаются в результате ее смешивания с водой или органическими растворителями. Самыми востребованными производными этой кислоты считаются пропионаты кальция и натрия. Пропионаты – это соли и эфиры пропионовой кислоты.
Самыми популярными реакциями взаимодействия пропионовой кислоты считаются:
1. Для получения пропионата кальция производят следующую реакцию:
2CH3CH2COOH + CaO → (CH3CH2COO)2Ca + H2O
2. Для получения пропионата натрия, необходимо провести реакцию пропионовой кислоты с гидроксидом натрия:
CH3CH2COOH + NaOH → CH3CH2COONa + H2O
Уравнение пропионовой кислоты с гидроксидом натрия показывает, что в результате этой реакции образовывается новое вещество – пропионат натрия.
Все эти реакции находят практическое применение в производстве, например, гербицида дихлорпрола и пропанола. Пропионовая кислота с гидроксидом натрия пагубно влияют на жизнедеятельность различных паразитарных растений и бурьянов. Они часто используются в сельском хозяйстве и аграрной сфере.
3. Также кроме реакций с калием и натрием, пропионовая кислота взаимодействует со спиртами. Реакция пропионовой кислоты с метиловым спиртом выражается следующим образом:
CH3CH2COOH + СН3OH = CH3CH2COOСН3 + Н2О
Полученное вещество называют метилпропионатом. Его применяют в качестве ароматизатора в пищевой промышленности, и в качестве растворителя олиф и целлюлозы.
4. Кроме метилового спирта эта кислота входит в реакцию и с этиловым спиртом. В результате получается этиловый эфир пропионовой кислоты: CH3CH2COOC2H5. Полученное вещество широко применяют в процессе производства искусственной кожи, а также с его помощью изготавливают растворители для пластмасс, целлюлозы, жира, воска. Этот продукт пропионовой кислоты считается сильнейшим ядом для насекомых.
5. Отдельного внимания требует частое использование муравьиной и пропионовой кислоты в производстве кормов для животных, в частности птиц. Муравьиная кислота помогает снизить уровень кислотности корма, что приводит к длительному хранению.
6. После реакции этанола с пропионовой кислотой получается этилпропионат. Это вещество считается неотъемлемой частью основных видов ароматизаторов, которые добавляют в пищевые продукты питания. Его также могут добавлять в качестве отдушки в парфюмерии.
7. Реакция, в которой участвуют пропанол и пропионовая кислота:
8. Реакция этанола с пропионовой кислотой:
С2Н5ОН + С2Н5СООН = С2Н5СООС2Н5 + Н2О
Вред от пропионовой кислоты
Если придерживаться всех мер безопасности и дозировки этого вещества, то никакой опасности не может быть. Но бывают случаи, когда из-за человеческого фактора и халатности, концентрация кислоты увеличивается. В таком случае, продукция может принести неисправимый вред организму. При повышенной концентрации в организме могут появляться язвы желудка, ожоги дыхательных и кожных покровов.
ПРИМЕНЕНИЕ ПРОПИОНОВОЙ КИСЛОТЫ И ЕЕ ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ХИМИЧЕСКИМИ СОЕДИНЕНИЯМИ
Для большинства потребителей добавка E280 ни о чем не говорит, но если копнуть глубже, то можно узнать, что за этим обозначением прячется пропионовая кислота.
Она представляет собою бесцветную жидкость с резким запахом. Для этого химического соединения характерно универсальное применение, так как его применяют и в кулинарии, и в производстве пластмасс, и в производстве гербицидов, и даже в фармацевтике.
ОСОБЕННОСТИ ХИМИЧЕСКИХ СВЯЗЕЙ
Если рассматривать это вещество с точки зрения химии, то химическая формула пропионовой кислоты будет: C2H5COOH. Ее вывели с помощью нефти и процесса брожения углеводов.
Саму кислоту производят бактерии с одноименным названием. Она выступает завершающим продуктом их жизнедеятельности.
Впервые данное вещество получили на производствах, где изготавливают уксус. Уксусная кислота и пропионовая кислота стали неотъемлемым понятием, потому что пропионовые соединения образуются во время изготовления уксуса
Также ученые доказали тот факт, что пропионовая кислота может встречаться и на кожных покровах человека.
Кроме того, ее обнаружили в желудках жвачных животных.
В середине 19 века ее первооткрывателем стал ученый Йохан Готлиб. Получение пропионовой кислоты он обнаружил в процессе разложение сахара, но окончательно раскрыть все «секреты» этого вещества смог только француз Жан-Батист-Дюма.
Он, к стати, и дал ее такое название.
Стоит отметить, что данная кислота имеет еще несколько названий, а именно:
В мировой классификации добавок она имеет значение E280.
СВОЙСТВА КИСЛОТЫ
Чтобы понять – для чего ее добавляют в пищевые продукты, пластмассы или корма для животных, необходимо знать ее свойства.
Поэтому ее ключевой характеристикой считается – препятствие размножения и роста различных видов плесени и бактерий.
Такое свойство ценится многими производителями хлебобулочных изделий, растворителей, пластмасс и лекарственных препаратов.
Это химическое соединение считается консервантом.
Но, где и в каком количестве можно ее применять? Чтобы ответить на этот вопрос необходимо обращать внимание на законодательную базу той страны, где пропионовая кислота допускается в производственный процесс.
Например, в Российской Федерации это вещество считается допустимым в определенном количестве, но в соседней Украине, это вещество запрещено на законодательном уровне.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ХИМИЧЕСКИМИ СОЕДИНЕНИЯМИ
Реакции пропионовой кислоты получаются в результате ее смешивания с водой или органическими растворителями. Самыми востребованными производными этой кислоты считаются пропионаты кальция и натрия.
Пропионаты – это соли и эфиры пропионовой кислоты.
Самыми популярными реакциями взаимодействия пропионовой кислоты считаются:
1. Для получения пропионата кальция производят следующую реакцию:
2CH3CH2COOH + CaO → (CH3CH2COO)2Ca + H2O
2. Для получения пропионата натрия, необходимо провести реакцию пропионовой кислоты с гидроксидом натрия:
CH3CH2COOH + NaOH → CH3CH2COONa + H2O
Уравнение пропионовой кислоты с гидроксидом натрия показывает, что в результате этой реакции образовывается новое вещество – пропионат натрия.
Все эти реакции находят практическое применение в производстве, например, гербицида дихлорпрола и пропанола. Пропионовая кислота с гидроксидом натрия пагубно влияют на жизнедеятельность различных паразитарных растений и бурьянов. Они часто используются в сельском хозяйстве и аграрной сфере.
3. Также кроме реакций с калием и натрием, пропионовая кислота взаимодействует со спиртами. Реакция пропионовой кислоты с метиловым спиртом выражается следующим образом:
CH3CH2COOH + СН3OH = CH3CH2COOСН3 + Н2О
Полученное вещество называют метилпропионатом. Его применяют в качестве ароматизатора в пищевой промышленности, и в качестве растворителя олиф и целлюлозы.
4. Кроме метилового спирта эта кислота входит в реакцию и с этиловым спиртом. В результате получается этиловый эфир пропионовой кислоты: CH3CH2COOC2H5. Полученное вещество широко применяют в процессе производства искусственной кожи, а также с его помощью изготавливают растворители для пластмасс, целлюлозы, жира, воска. Этот продукт пропионовой кислоты считается сильнейшим ядом для насекомых.
5. Отдельного внимания требует частое использование муравьиной и пропионовой кислоты в производстве кормов для животных, в частности птиц. Муравьиная кислота помогает снизить уровень кислотности корма, что приводит к длительному хранению.
6. После реакции этанола с пропионовой кислотой получается этилпропионат. Это вещество считается неотъемлемой частью основных видов ароматизаторов, которые добавляют в пищевые продукты питания. Его также могут добавлять в качестве отдушки в парфюмерии.
7. Реакция, в которой участвуют пропанол и пропионовая кислота:
8. Реакция этанола с пропионовой кислотой:
С2Н5ОН + С2Н5СООН = С2Н5СООС2Н5 + Н2О
ВРЕД ОТ ПРОПИОНОВОЙ КИСЛОТЫ
Если придерживаться всех мер безопасности и дозировки этого вещества, то никакой опасности не может быть.
Но бывают случаи, когда из-за человеческого фактора и халатности, концентрация кислоты увеличивается.
В таком случае, продукция может принести неисправимый вред организму
При повышенной концентрации в организме могут появляться язвы желудка, ожоги дыхательных и кожных покровов.
Пропионовая кислота
Пропионовая кислота (Пропановая кислота, Метилуксусная кислота) — одноосновная карбоновая кислота алифатического ряда, бесцветная едкая жидкость с резким запахом, имеющая формулу CH3CH2COOH.
Пропионовая кислота была открыта в 1844 году Йоханом Готлибом.
Содержание
[править] Физические свойства
Температура плавления = −20,8 °С, Температура кипения = 140,8 °С, температура самовоспламенения = 440 °C, плотность 0,993 г/см 3 (20 °С). Молярная масса = 74,08 г/моль.
[править] Химические свойства
Пропионовая кислота смешивается с водой и органическими растворителями.
Соли и эфиры пропионовой кислоты называются пропионатами. Например, пропионат натрия получают следующим образом:
Пропионат кальция получают следующим образом:
Пропионовая кислота, взаимодействуя со спиртами, образует эфир. Например, при реакции с метанолом CH3OH образуется метиловый эфир пропионовой кислоты:
Пропионовая кислота может взаимодействовать с галогенами, при этом происходит замещение в углеводородном радикале. Так, при реакции с хлором образуется α-хлорпропионовая кислота:
Пропионат аммония получают взаимодействием с NH4OH:
[править] Практическое применение
В промышленности пропионовую кислоту получают карбонилированием этилена по реакции Реппе; каталитическим окислением пропионового альдегида; как побочный продукт при парофазном окислении углеводородов С4-С10, например:
Пропионовая кислота и её производные применяются в производстве гербицидов (пропанол, дихлорпрол), лекарственных средств (ибупрофен, феноболин и др.), душистых веществ (бензил-, фенил-, геранил-, линалоил- пропионаты), пластмасс (поливинилпропионата и др.), растворителей (пропил-, бутил-, пентилпропионата и др.), винилпластификаторов и поверхностно-активных веществ (гликолевые эфиры).
Пропионовая кислота применяется в пищевой промышленности, так как препятствует росту плесени и патогенных бактерий. Поэтому эта кислота используется как консервант в продуктах, как потребляемых человеком, так и в кормах для животных (в последнем случае применяется пропионат аммония). В продуктах, потребляемых людьми, особенно в хлебобулочных изделиях, данная кислота используется как натриевая (пропионат натрия) или кальциевая (пропионат кальция) соли.
При работе с пропионовой кислоты необходимо соблюдать осторожность, так как её попадание на тело человека может вызвать химический ожог. При попадании внутрь данная кислота может теоретически вызвать язву желудка.
Пропионовая кислота
Пропионовая кислота — это общее название пропановой кислоты, карбоновой кислоты с резким запахом. Их соли и сложные эфиры называются пропионатами.
Химические свойства
Возникновение и получение
Пропионовая кислота естественным образом содержится в некоторых эфирных маслах. Ее получают в промышленных масштабах из этена, окиси углерода и воды. Есть также бактерии, которые производят пропионовую кислоту, например, бактерии, колонизирующие толстую кишку человека. Там они образуют кислоту из непереваренных углеводов.
Образование пропионовой кислоты определенными бактериями также важно при производстве сыров: бактерии пропионовой кислоты в сырном твороге формируют характерные отверстия и аромат твердых сыров, выделяя углекислый газ и пропионовую кислоту. Она также образуется во время процессов ферментации во время биологического разложения растительных или животных материалов.
Применение
Пропионовая кислота — важный синтетический строительный блок для производства пластмасс, гербицидов и фармацевтических препаратов. Пропионовая кислота (E280) и ее соли: пропионат натрия (Е281), пропионат кальция (Е282) и пропионат калия (E283) используются в качестве ингибиторов плесени.
Кислота и ее соли в основном используются в качестве консервантов против роста дрожжей и плесени. Ее часто используют при производстве хлебобулочных изделий, чтобы предотвратить рост бактериальной микрофлоры. Из-за резкого запаха и неприятного вкуса ее использование достаточно ограничено.
Кислоту часто добавляется в силос, где доля может составлять до 2% от сухого вещества, для предотвращения кетоацидоза у молочного скота.
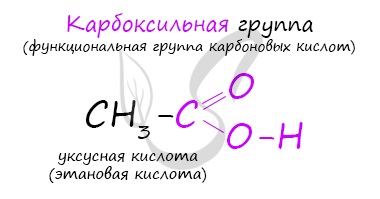
Карбоновые кислоты
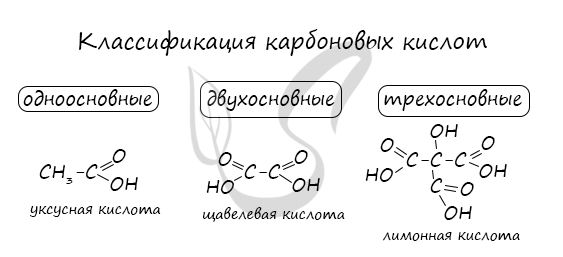
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
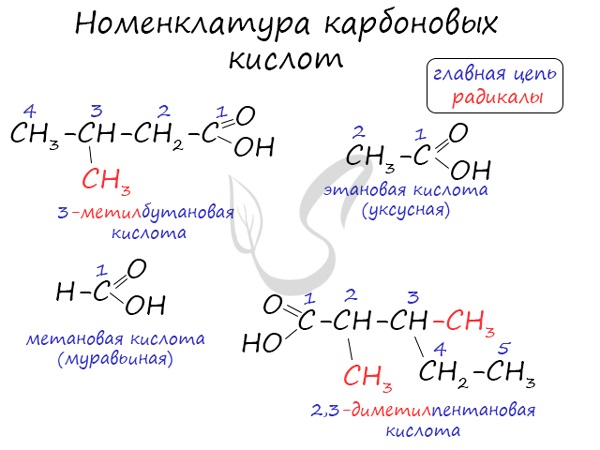
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
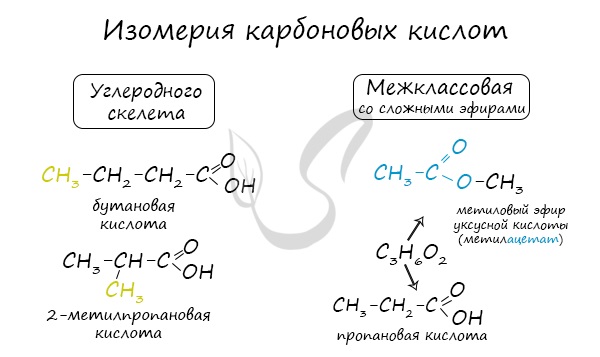
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
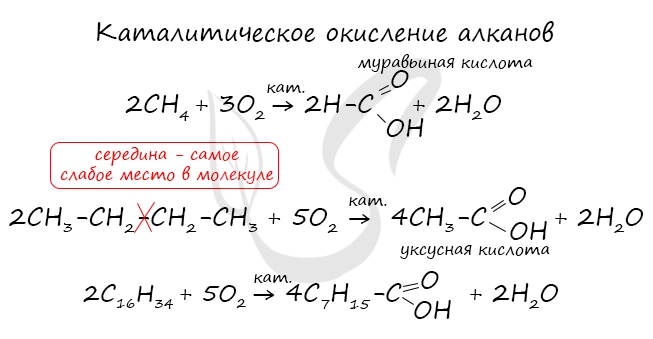
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
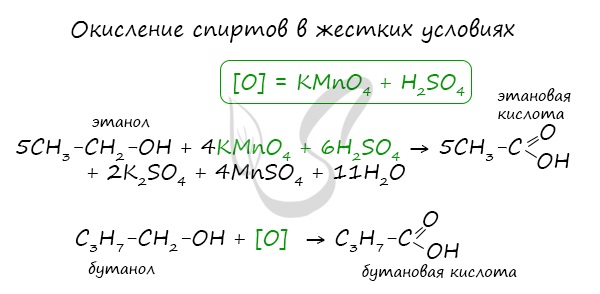
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
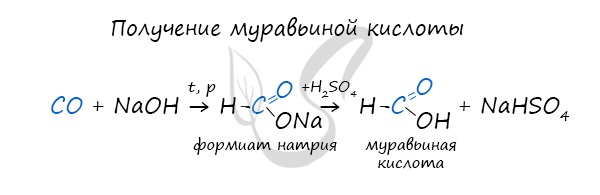
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
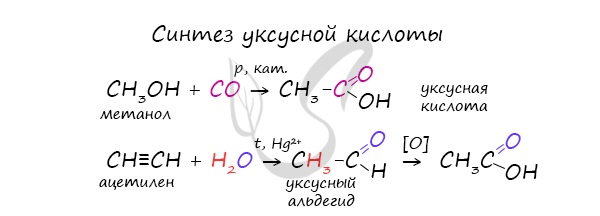
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
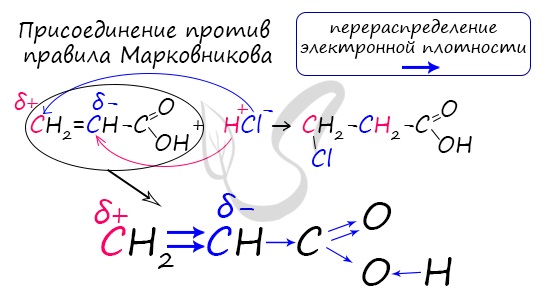
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
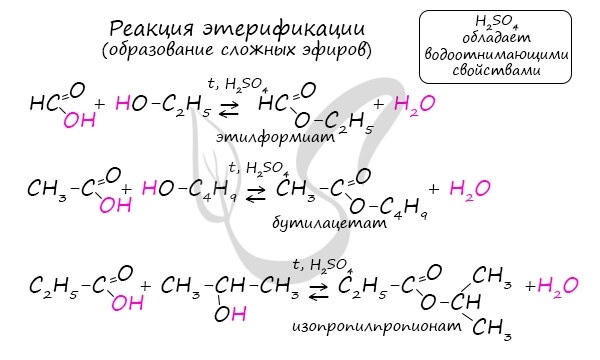
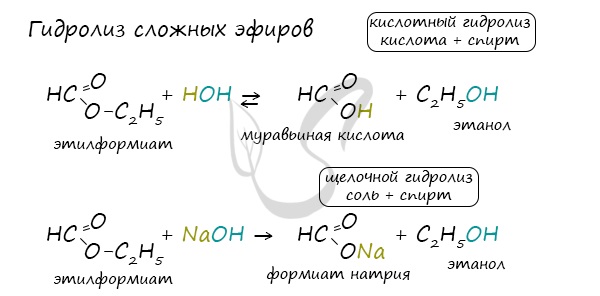
Сложные эфиры
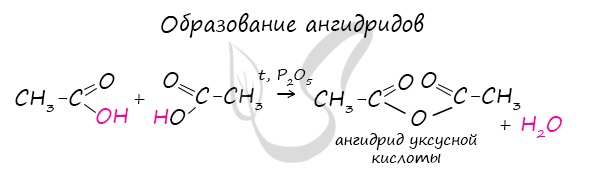
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
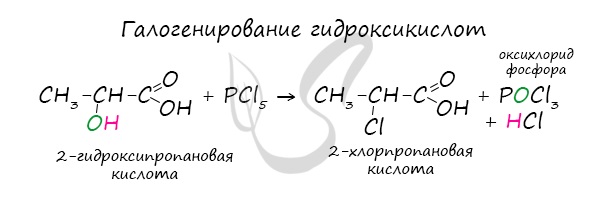
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.