саркопения у пожилых что это симптомы и лечение
Саркопения — новое имя старого недуга
Что такое саркопения и как поддерживать состояние костей и мышц в тонусе, рассказала Наталья Валерьевна Поленова, кандидат медицинских наук, кардиолог, диетолог, семейный врач GMS Clinic.
Что же такое саркопения? Слово явно нерусское и многим незнакомое.
Да, действительно, термин «саркопения» имеет греческое происхождение: sarx — «плоть», penia — недостаток, нехватка. Саркопения представляет собой патологическое состояние, особенно характерное для пожилых людей, при котором происходит уменьшение мышечной массы, а также ухудшение силы и функции мышц. Термин был предложен к использованию еще в 80-х годах прошлого века, однако статус официально признанного заболевания получил в прошлом, 2019 году. Такое внимание к проблеме саркопении было продиктовано растущей продолжительностью жизни в мире, увеличением количества пожилых и необходимостью формирования более точных подходов к диагностике и лечению данного состояния. Для системы здравоохранения любой развитой страны очевидно, что граждане зрелого возраста хотят быть не только здоровы, но физически и социально активными.
Чем опасна саркопения?
Саркопения опасна не только нарушениями двигательной активности пациентов, приводящими к заболеваниям опорно-двигательного аппарата: остеопорозу, артрозу, переломам и др. Саркопения на сегодняшний день признана значимым фактором риска развития и прогрессирования сердечно-сосудистых заболеваний, иммунодефицита, сахарного диабета, хронического неспецифического воспаления. Являясь одним из важнейших гериатрических синдромов, саркопения обуславливает инвалидность и смертность у больных пожилого и старческого возрастов наряду с такими известными врагами здоровья, как избыточная масса тела, недостаточное потребление овощей и фруктов, курение и гиподинамия.
Каковы причины возникновения этого заболевания?
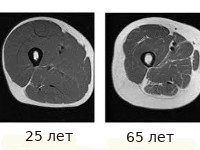
Основная причина развития саркопении банальна — возраст. В среднем к 65 годам человек теряет более 1/3 мышечной массы по сравнению с ее пиком, приходящимся на 20–30 лет. При снижении веса у пожилых людей до 1/4 потери массы тела приходится на мышечную массу, а набор веса происходит главным образом за счет жировой ткани. При быстрой потере массы тела могут происходить значительное снижение минеральной плотности костной ткани и повышение частоты переломов. Очень плохую службу здесь может оказать неправильное, несбалансированное похудение, особенно в зрелом возрасте. При сознательном снижении веса необходимо обязательно задаваться вопросом: «Не теряю ли я мышечную массу?» Чтобы этого не происходило, нужно поддерживать достаточную физическую активность и адекватное потребление белка в рационе.
Как понять, что процесс уже идет или приближается? Каковы симптомы?
Есть объективные, измеримые критерии диагностики саркопении, такие как кистевая динамометрия (измерения силы мышц кисти), тест 6-минутной ходьбы (какое расстояние пациент может пройти за 6 минут) и многие другие методы исследования, хорошо знакомые практикующим врачам. Однако особую важность представляет также субъективная оценка пациентом своих двигательных возможностей. Например, по неясным обстоятельствам привычные нагрузки стали восприниматься как более утомительные. Это очень важно, постарайтесь не пропустить момент, когда необходима помощь специалиста. Помимо физических проявлений (необъяснимая потеря массы тела, переутомление, выраженная слабость, медленная походка, низкая физическая активность) могут наблюдаться признаки снижения когнитивных функций и социальной активности. Все это не должно остаться незамеченным. Саркопения — обратимое состояние: чем раньше принять меры, тем эффективнее будет борьба с возрастными изменениями мышц.
Есть ли основные стадии развития этой болезни? И чем они характерны?
Да, эксперты разделяют течение саркопении на три стадии. Так, на первой стадии (пре-саркопения) отмечается только снижение мышечной массы без заметных клинических проявлений. На второй стадии снижение мышечной массы уже начинает вызывать тот или иной функциональный дефицит, то есть будет иметь место снижение мышечной силы или мышечной функции. На третьей стадии (тяжелая саркопения) имеют место все три проявления саркопении: снижены и масса мышц, и сила, и функция.
Как выявить и лечить саркопению, если она уже диагностирована?
Для оценки мышечной массы в клинической практике применяются двухэнергетическая рентгеновская абсорбциометрия, денситометрия (оценка плотности тканей организма), биоимпедансометрия (определение соотношения жировой и мышечной ткани), компьютерная или магнитно-резонансная томография.
Для оценки функции мышц специалистами применяются следующие методики: определение скорости ходьбы на короткое расстояние (4 метра), 5-кратное вставание со стула и возможность удержания равновесия в положении стоя в течение 10 секунд, 400 метров ходьбы на время или дальняя ходьба на время, лестничная проба, тест «встать и идти» (10 секунд), опросники, оценивающие устойчивость походки и частоту падений.
Каждый из указанных параметров «стоит» определенное число баллов. По итогам оценки доктор принимает решение о наличии диагноза «саркопения» у данного пациента.
Таблеток от саркопении пока нет. Рассматривается возможность применения витамина D, антагонистов гормона грелина, антицитокиновых препаратов, используемых в лечении ревматоидного артрита, однако это пока — скорее основание для проведения специально спланированных исследований. А вот что не подлежит сомнению, так это диета с достаточным содержанием белка (не менее 1–1,2 г/кг массы тела) и все виды физической активности: силовая, аэробная, упражнения на гибкость и равновесие. Все указанные виды физических упражнений в режиме умеренной, но регулярной активности способны помочь в борьбе с возрастным снижением мышечной массы и силы.
Возможно ли предотвратить эту болезнь? Что рекомендуется в качестве профилактических мер?
Не только возможно, но и очень желательно! Саркопению гораздо проще предотвратить, чем лечить. Диета с повышенным содержанием белка, а также регулярная физическая активность должны быть рекомендованы всем пациентам пожилого возраста с подтвержденным или предполагаемым диагнозом «саркопения». Чем раньше начать, тем дальше отодвинется развитие саркопении, проще говоря, старости как таковой. Все в наших руках!
Расскажите о необычных случаях из вашей практики.
На мой взгляд, заслуживают внимания случаи так называемого саркопенического ожирения. То есть общая масса тела в норме или даже превышена, а мышечной массы категорически не хватает. Более того, человек может сам придерживаться сомнительных рационов питания, как правило, жестких и несбалансированных по содержанию белка. Допустим, через месяц или два общая масса тела убывает, мы оцениваем состав тела и с сожалением отмечаем, что теряется не жировая масса, а мышечная. В связи с тем, что жировая масса практически инертна в отношении обмена веществ, такой пациент имеет риск вскоре набрать гораздо больше килограммов, чем он потерял, так называемый рикошетный набор веса. Поэтому очень важно худеть правильно, обратиться к специалисту и не потерять столь важную мышечную массу в попытке нормализовать массу тела.
У вас уже есть примеры исцеления или предотвращения болезни?
Конечно! Пожалуй, наиболее мне близкий и показательный пример — мой собственный дедушка, ему 91 год.
Очень отзывчивый пациент, следует практически всем рекомендациям в течение многих-многих лет. Ни одного его дня не проходит без утренней гимнастики, физическая и социальная активность — на запредельном уровне. Рацион иногда приходится корректировать, но в целом о пользе белка и овощей, а также о вреде быстрых углеводов он постоянно слышит от меня и, к моей радости, большую часть советов принимает. И хоть в рекомендациях по саркопении этого пункта нет, позволю добавить от дедушки и от себя: позитивный настрой очень важен в любом возрасте. В добром расположении духа физическая и социальная активность возрастают, а организм с благодарностью отвечает отменным здоровьем.
Саркопения
Саркопения – это патологическое состояние, ассоциированное с возрастом, характеризующееся снижением массы скелетной мускулатуры. Клинически проявляется уменьшением мышечной силы и функциональности. Может привести к проблемам с самообслуживанием, инвалидности и даже смерти. Диагноз саркопении ставится при помощи исследований, измеряющих мышечную силу и массу, а также специально разработанных тестов. В качестве лечения назначаются регулярные физические упражнения, коррекция питания (увеличение в рационе белковых продуктов), витамин Д. В тяжелых случаях применяют анаболические стероиды, гормон роста.
МКБ-10
Общие сведения
Саркопения (от греческого «sarx» — тело, плоть + «penia» — снижение) – дегенеративный процесс, при котором происходит постепенная потеря функциональных мышечных волокон. Использовать данный термин впервые предложил американский врач И. Розенберг в 1989 году. Атрофические изменения в мышцах, связанные с возрастом, известны очень давно. Однако саркопения только в 2016 году была выделена в самостоятельную нозологическую единицу и включена в международную классификацию болезней. В 2009 году была создана Европейская рабочая группа по саркопении у старых людей (EWGSOP). Распространенность патологии составляет 30% среди лиц 60-летнего возраста и около 50% среди населения старше 80 лет. Соотношение мужчин и женщин 1:1.
Причины саркопении
Данное состояние считается следствием инволютивных и нейродегенеративных явлений, происходящих при старении как во всем организме в целом, так и в скелетных мышцах. К ним относятся снижение способности к регенерации миосателлитных клеток, ухудшение функционирования нервно-мышечных синапсов и т. д. Немаловажную роль играет возрастная недостаточность гормонов, активирующих анаболические процессы в мышцах – тестостерона, соматотропина, инсулиноподобного фактора роста-1.
К предрасполагающим факторам, усугубляющим мышечную дистрофию, относятся низкая физическая активность, дефицит витамина Д. Неблагоприятное действие оказывает и недостаточное поступление белка с пищей, которое может быть вызвано как неправильным составлением своего рациона, так и патологиями желудочно-кишечного тракта, препятствующими нормальному усвоению аминокислот (хроническим панкреатитом, болезнью Крона, целиакией). К саркопении также приводят хронические заболевания – ревматоидный артрит, хроническая обструктивная болезнь легких, тяжелые болезни печени.
Патогенез
Механизм изменений в мышечной ткани при саркопении сложен. С одной стороны, присутствует напрямую связанное со старением физиологическое действие апоптоза (запрограммированной клеточной гибели), с другой ‒ влияние многочисленных факторов, ускоряющих апоптоз. Дефицит анаболических гормонов, витамина D, аминокислот сдвигает баланс между синтезом и распадом белков в мышцах в сторону последнего. Недостаточная физическая активность ухудшает кровообращение мышц, что нарушает биогенез митохондрий в мышечных клетках и запускает окислительный стресс, который повреждает клеточные мембраны.
Вырабатываемые медиаторы и цитокины (интерлейкин-6, С-реактивный белок, адипонектин) при хронических воспалительных заболеваниях также способствуют дисметаболизму в миоцитах. В последнее время ведущее патогенетическое значение отводится белку миостатину, тормозящему регенерацию мышечных волокон. Исходом этих процессов является уменьшение количества, объема миофибрилл, замещение их жировой и соединительной тканью.
Классификация
Традиционно саркопения считается болезнью пожилых и в подавляющем большинстве случаев встречается у людей старше 60 лет. Она часто сочетается со старческой астенией, кахексией. Вместе с тем, выделяют первичную саркопению, сопровождающую старение, и вторичную, которая развивается при некоторых хронических болезнях (печеночной недостаточности, ревматоидном артрите). Также существуют следующие фенотипические формы:
Представленные фенотипы характерны как для первичной, так и для вторичной формы. В зависимости от тяжести состояния пациента и количества имеющихся диагностических критериев различают:
Симптомы саркопении
Клиническая симптоматика развивается медленно. При минимальных атрофических изменениях в мышцах человек начинает плохо переносить привычную для него физическую нагрузку (быстро наступает усталость, требуется большее время для отдыха). При прогрессировании патологических процессов пациенту становится трудно подниматься по лестнице, нести даже небольшой груз (2-3 кг), расчесывать волосы на голове.
Из-за выраженной слабости мышц у больного подкашиваются ноги при ходьбе по прямой поверхности, нарушается равновесие, возникают частые падения. Поражение диафрагмы и межреберных мышц сопровождается смешанной одышкой. Когда преобладающее количество мышечных волокон замещено соединительной и жировой тканью, больной не может сам себя обслуживать, ему нужна помощь, чтобы встать с кровати.
Осложнения
Саркопения является тяжелым заболеванием, приводящим к временной или стойкой утрате трудоспособности и инвалидности по причине критичной мышечной слабости. Самые опасные для жизни состояния возникают из-за функциональной неполноценности дыхательной мускулатуры – это аспирационная пневмония и дыхательная недостаточность. Наиболее частые осложнения (переломы длинных трубчатых костей) вызваны постоянными падениями. При вторичной саркопении неблагоприятные последствия связаны с основным заболеванием (например, кровотечение при печеночной недостаточности). Также саркопения ввиду повышения инсулинорезистентности может ухудшить течение сахарного диабета 2 типа. Саркопеническое ожирение усугубляет ишемическую болезнь сердца и хроническую сердечную недостаточность.
Диагностика
Курацией пациентов с саркопенией занимаются врачи-гериатры. Для выявления клинических признаков патологии пользуются опросником SARC-F. В опроснике нужно ответить на такие вопросы, как «насколько сложно вам совершать прогулки вокруг дома?», «испытываете ли вы трудности при подъеме по лестнице?», «как часто вы падали за последний год?». Европейской рабочей группой был разработан специальный диагностический алгоритм, позволяющий определить мышечную силу, массу и функцию. Если человек, отвечая на вопросы SARC-F, набирает большое количество баллов, целесообразно проведение следующих исследований:
Саркопению необходимо дифференцировать с мышечными дистрофиями, дермато- и полимиозитом, неврологическими заболеваниями (миастения, синдром Гийена-Барре). Тяжелые формы требуют обязательного исключения злокачественных новообразований и ВИЧ-инфекции. В дифференциальной диагностике принимают участие неврологи, онкологи.
Лечение саркопении
Из лекарственных средств применяются нативные препараты витамина Д; при наличии остеопороза назначаются активные формы витамина. При выраженных признаках мышечной атрофии используются анаболические стероиды (нандролона деканоат). При их неэффективности прибегают к аналогам гормона роста (соматотропин). В настоящее время ведутся клинические исследования новых перспективных лекарственных препаратов – ингибиторов миостатина, агонистов грелина и селективных модуляторов андрогенных рецепторов. Терапия вторичной формы дополнительно включает лечение основного заболевания.
Профилактика и прогноз
Саркопения является тяжелой патологией, снижающей работоспособность, приводящей пациентов к инвалидности, лишающей их способности к самообслуживанию. Риск летального исхода составляет около 5-10%. Основные причины смерти – дыхательная недостаточность, сердечно-сосудистая патология, кахексия. Саркопения снижает продолжительность жизни у больных с циррозом печени и другими сопутствующими заболеваниями. Профилактика заключается в регулярном выполнении физических нагрузок, полноценном питании (нормальном потреблении белка), приеме превентивных доз витамина D.
Саркопения глазами эндокринолога
Полный текст:
Аннотация
Одним из синдромов, существенно влияющим на состояние здоровья и жизнь пациента, является саркопения. Саркопения – это мультиэтиологичный синдром со сложным, недостаточно изученным патогенезом, в котором эндокринные факторы играют одну из ведущих ролей. Коморбидность пожилых пациентов создает трудности дифференциальной диагностики имеющейся патологии. Сочетание саркопении с различными эндокринными патологиями, такими как ожирение, остеопороз, гипотиреоз, гипопаратиреоз, дефицит витамина D, приводит к более тяжелому течению заболеваний и худшему прогнозу для качества и продолжительности жизни пациента. При этом вторичный генез саркопении в ряде ситуаций может позволить улучшить состояние пациента путем оценки патогенетических причин и их устранения.
Таким образом, эндокринологу следует уделять более пристальное внимание синдрому саркопении и его коррекции, а также мерам его профилактики на самых ранних стадиях.
Ключевые слова
Для цитирования:
Мокрышева Н.Г., Крупинова Ю.А., Володичева В.Л., Мирная С.С., Мельниченко Г.А. Саркопения глазами эндокринолога. Ожирение и метаболизм. 2018;15(3):21-27. https://doi.org/10.14341/omet9792
For citation:
Mokrysheva N.G., Krupinova J.A., Volodicheva V.L., Mirnaya S.S., Melnichenko G.A. A view at sarcopenia by endocrinologist. Obesity and metabolism. 2018;15(3):21-27. (In Russ.) https://doi.org/10.14341/omet9792
Эпидемиология
Распространенность саркопении в популяции по разным источникам варьирует от 4,3% до 73,3% и зависит от возрастных критериев включения и особенностей исследуемых групп (пациенты, получающие амбулаторную помощь, и жители домов престарелых имеют значимые отличия). Чаще встречаются данные о распространенности в диапазоне 5–13% среди лиц 60–70 лет и на уровне 50% – в группе старше 80 лет [3, 4]. В российской популяции частота составила 13% у пациентов старше 85 лет [5].
Этиология
Этиологически саркопению разделяют на первичную и вторичную. Первичную саркопению рассматривают в рамках возрастных изменений мышечной ткани, вторичную – как следствие других заболеваний и патологических состояний (онкологической патологии, сахарного диабета (СД) 2 типа, хронической сердечной недостаточности, гиподинамии и прочего, а также вследствие приема некоторых лекарственных препаратов).
Также обсуждается и генетическая предрасположенность к саркопении. Например, доказана связь генов ACE (кодирует ангиотензинпревращающий фермент), ACTN3 (кодирует альфаактинин 3), MSTN (кодирует миостатин), CNTF (кодирует цилиарный нейротрофический фактор), IGF1 (кодирует ИФР-1), IL-6 (кодирует интерлейкин 6) и VDR (кодирует рецептор витамина D) с силой и/или массой мышечной ткани. Особый интерес для изучения представляют такие гены-кандидаты, как GREM1 (кодирует Gremlin1), TRHR (кодирует рецептор тиреотропин-рилизинг гормона), ACVR1B (кодирует рецептор активина 1B). В ряде двойных слепых исследований продемонстрировано, что наследуемость некоторых показателей мышечной массы и силы достигает 80% [6, 7].
Патогенез
Саркопения – это мультиэтиологичный синдром со сложным патогенезом, в котором эндокринные факторы играют одну из ведущих ролей. Патогенез данного состояния изучен недостаточно, однако уже известно, что на развитие саркопении значимое влияние оказывает снижение уровня гормона роста (ГР), инсулиноподобного фактора роста-1 (ИФР-1), половых гормонов, витамина D, инсулинорезистентность. В то же время активно изучаются такие факторы, способствующие развитию саркопении, как особенности образа жизни (качество питания, физическая активность, иммобилизация) и пищевой статус. Снижение последнего приводит к недостаточному синтезу белка, развитию дегенеративных процессов, митохондриальной дисфункции и атрофии мышечных волокон, вследствие чего происходит потеря мышечной массы и силы [8]. На развитие саркопении также может влиять течение гестационного периода матери, окружающая среда в раннем детском возрасте, вес тела при рождении и в младенчестве, который прямо связан с мышечной массой и ее функциональными возможностями в старшем возрасте [6].
В основе патогенеза саркопении лежит утрата мышечной массы. Зрелые мышечные волокна состоят из многоядерных клеток, неспособных к делению, поэтому рост и регенерация мышц происходят за счет пролиферации клеток-сателлитов. При саркопении в первую очередь снижается количество клеток-сателлитов и волокон II типа, приводя к невозможности совершения пациентом быстрых движений [9]. Будучи ключевым звеном большинства клеточных процессов (обеспечение энергией, регуляция внутриклеточного гомеостаза кальция, активация клеточной пролиферации), митохондриальная дисфункция и дальнейшая потеря целостности митохондрий в миоцитах приводят к снижению окислительной способности, нарастанию уровня оксидативного стресса, повреждению клеток и развитию атрофии мышечных волокон (рис. 1).
Рис. 1. Этиология и патогенез саркопении.
Значительную роль играют системное воспаление, трансформация митохондрий и их взаимное усиление дегенеративного влияния на мышцы. В скелетных мышцах происходит повреждение транспортной цепи электронов, которое может определяться фокально в миоцитах или в дискретных областях отдельной клетки, и приводит к снижению активности цитохрома С-оксидазы и повышению активности сукцинатдегидрогеназы (СДГ) [10].
Доказательства, подтверждающие ключевую роль мутаций митохондриальной ДНК (мтДНК) в патогенезе старения, были получены в эксперименте на животных моделях, у которых имела место ошибка считывания в мтДНК-полимеразе γ (PolG), что проявлялось преждевременным старением, характеризующимся алопецией, кифозом, потерей слуха, остеопорозом, саркопенией и сокращением продолжительности жизни. У этих мышей накапливались соматические мутации мтДНК и демонстрировали системную дисфункцию митохондрий, включая снижение функции дыхательной цепи, ускоренный апоптоз в постмитотических тканях, при этом повышенного уровня окислительного стресса у них не наблюдалось. Интересно, что делеции мтДНК локализуются совместно с мутациями транспортной цепи электронов и при повышении определенного порога значений приводят к нарушению ее активности. В целом эти данные подтверждают гипотезу о том, что делеции мтДНК, накапливаясь в мышечных волокнах, компрометируют митохондриальную биоэнергетику и способствуют развитию атрофии мышц [10].
Другой путь, регулирующий метаболизм митохондрий во время старения, включает ИФР-1. Этот путь осуществляется путем фосфорилирования АТФ-цитрат-лиазы, фермента, катализирующего митохондриальное производное цитрат в оксалоацетат и ацетил-КоА. Предполагается, что возрастное снижение уровня ИФР-1 может нарушать митохондриальную активность посредством снижения АТФ-цитрат-лиазы, способствуя развитию саркопении [10].
Наличие воспалительной реакции также тесно связано с риском развития саркопении. Повышение фактора некроза опухоли-α способствует развитию воспаления через активацию ядерного фактора k-B, что приводит к потере мышечной массы (см. рис. 1) [11].
Таким образом, ИФР-1, механизмы контроля качества митохондрий и воспалительный путь являются основными звеньями, контролирующими мышечную массу.
Повреждения на любом уровне контроля состояния митохондрий сохраняются на протяжении их жизни, таким образом накапливаются поврежденные органеллы. Как следствие, увеличение отношения AMФ/ATФ и оксидативный стресс активируют катаболический путь, который приводит к атрофии мышц. Этот путь включает в себя как посредников, связанных с аутофагами, так и индукторов мышечного катаболизма (MuRF-1, атрогин), приводящих к деградации митохондрий и белка для обеспечения альтернативных источников энергии [11].
В исследовании, изучавшем взаимосвязь скелетной мышечной массы с сохранностью капиллярной сети при старении, сравнивались данные гистологического исследования мышечной ткани между группами молодых здоровых лиц (средний возраст – 22 года, мужчины (n=14), женщины (n=5)) и пожилых лиц (средний возраст – 74 года, мужчины (n=22), женщины (n=6)). Степень мышечной капилляризации и распределения капилляров определяли методом капиллярных доменов. Окислительную способность мышечных волокон оценивали с помощью количественной гистохимии. Обеспечение капиллярами волокон определялось главным образом размером волокна и лишь в малой степени окислительной способностью. Несмотря на атрофию волокон II типа на 18% (p=0,019) и снижение количества капилляров на одну клетку на 23% (р 10,75 кг/м²
Вместе с тем биоимпедансный метод исследования недостаточно точен, особенно у пациентов с заболеваниями, проявляющимися отечным синдромом (хроническая сердечная недостаточность, почечная недостаточность и лимфедема). Антропометрические измерения, такие как окружность икроножной мышцы или толщина кожной складки, неточны главным образом потому, что ожирение, отеки, а также изменения в жировой ткани и потеря эластичности кожи, связанные с возрастом, снижают специфичность метода в оценке мышечной массы. Они не рекомендуются для использования в целях диагностики саркопении, но могут быть альтернативными в случае отсутствия других методов [16, 18]. Антропометрический метод недостаточно информативен и при саркопеническом ожирении, включающем критерии саркопении и увеличение объема подкожной жировой клетчатки у мужчин ≥25%, у женщин ≥35%. При данном состоянии наблюдается жировое перерождение клеток-сателлитов, жировая инфильтрация мышц, которые способствуют снижению силы нижних конечностей и гиподинамии – возникает порочный круг. Однако на данный момент невозможно оценить, что развивается первично: саркопения или ожирение, так как при ожирении наблюдается хроническое воспаление, которое, в свою очередь, приводит к снижению мышечной массы и силы [16].
Остеосаркопения
Остеосаркопения – это относительно новое понятие, включающее в себя сочетание низкой мышечной массы и сниженной минеральной плотности костной ткани (МПК), связанное со старением и общим патогенезом [19]. Учитывая повышение риска развития как саркопении, так и остеопороза у пожилых лиц, требуется оценка состояния мышечной ткани у таких пациентов [20].
Состав тела пациентов с остеосаркопенией характеризуется снижением мышечной массы, МПК, ИМТ и индекса общего жира по сравнению с пациентами с изолированным остеопорозом или саркопенией. Клинические проявления остеосаркопении характеризуются слабостью, низкой скоростью ходьбы, потерей подвижности. В настоящее время отсутствуют специфические маркеры остеосаркопении, однако отмечено, что у пациентов с данной патологией уровень тестостерона, витамина D и гемоглобина ниже, чем у пациентов с изолированным остеопорозом или саркопенией.
Помимо возраста, существует ряд других факторов, которые способствуют развитию остеосаркопении. Генетические полиморфизмы GLYAT, METTL21C, MSTN, ACTN3 PGC-1α и MEF-2C связаны с потерей костной и мышечной ткани. Эндокринные заболевания (в основном СД, нарушение функции щитовидной железы и низкий уровень витамина D, половых гормонов, ГР, ИФР-1), алиментарная недостаточность, ожирение и прием кортикостероидов также влияют на развитие остеосаркопении [19]. Отмечено, что саркопения и мышечная слабость, так же как и частота переломов, встречаются чаще у пациентов с СД 2 типа, чем у здоровых людей [21].
Жировая инфильтрация мышц у пожилых вносит свой вклад в развитие остеосаркопении, что, возможно, связано с отрицательным воздействием продукции воспалительных цитокинов костным мозгом и жировой тканью. Установлено, что пациенты с саркопенией и остеопенией имеют высокие концентрации воспалительных цитокинов, преобладание интерлейкина-6 (IL-6) и фактора некроза опухолей альфа (ФНО-α), которые связаны как с системной, так и с локальной липотоксичностью. Кроме того, изменения в костном мозге тесно ассоциированы с изменениями мышечной массы. Скелетная и мышечная ткань взаимодействуют механически, физически, а также биохимически посредством паракринных и эндокринных факторов. В этом процессе существует много возможных путей, которые могут объяснить развитие и прогрессирование остеосаркопении. Один из них включает остеокальцин, который стимулирует пролиферацию β-клеток, секрецию инсулина и действует непосредственно на скелетную мышцу, коррелируя с мышечной силой. Другим внутренним механизмом, связывающим мышцы и кость, является секреция сосудистого эндотелиального фактора роста (VEGF) с помощью мезенхимальных стромальных клеток костного мозга, что стимулирует пролиферацию миобластов. Мышцы также секретируют несколько гормонов и активных веществ, влияющих на кость, таких как ИФР-1, остеоглицин, ирисин, остеонектин, фактор роста фибробластов-2, IL-6, IL-15 и миостатин. Миостатин является членом надсемейства бета-трансформирующего фактора роста, экспрессируемого в основном в скелетных мышцах. Изучен его эффект на рост мышц и влияние на кость. Дефицит гена MSTN и системное введение ACVR2B-Fc (inhibitor of the Activin Receptor 2B – блокатора рецептора активина 2B) приводят к гипертрофии мышечной ткани и увеличению костной массы [18]. Мышечная ткань также секретирует декорин, который, связывая миостатин, способствует росту мышечной ткани. Обнаружен и его противоопухолевый эффект. При изучении генетически модифицированных животных с выключенным геном DCN, кодирующим декорин, зафиксирован спонтанный рост опухолей. Однако влияние этого белка на физиологию человека изучено недостаточно.
Постменопаузальная остеосаркопения, развитие которой обусловлено генетическими факторами, изменением состава тела, низкой физической активностью, дефицитом эстрогенов и витамина D, приводит к снижению мышечной массы, силы, функциональных возможностей, а также к снижению МПК, что в сочетании с коморбидностью пожилых пациентов реализуется в увеличении частоты переломов, инвалидизации и смертности [20].
Также существует такое понятие как остеосаркопеническое ожирение, критериями которого являются снижение МПК по Т-критерию ≤-1,0 SD по данным DXA, снижение ИТМ 1 (для андроидного типа ожирения) или 2,34 мг/дл), гликемии (>112 мг/дл), а также более высокий риск переломов (FRAX>15%, r=0,316; p 30 нг/мл (50 нмоль/л) [18]. Баланс между витамином D и паратиреоидным гормоном (ПТГ) является ключевым регулятором мышечной силы: ПТГ способен модулировать работу мышечной ткани через увеличение внутриклеточного кальция.
Лечение и профилактика саркопении
В настоящее время отсутствует специфическое лечение саркопении, первичной является профилактика. Физические упражнения, особенно постепенно увеличивающиеся силовые нагрузки, являются стимулом для синтеза мышечного белка. Выполнение физических упражнений в течение минимум 20 минут в неделю значительно повышает мышечную и костную массу, силу, снижает функциональные ограничения, предотвращает падения и переломы у пожилых людей. Однако у пациентов с тяжелыми сопутствующими заболеваниями (такими как нейрокогнитивные и сердечные-сосудистые патологии) могут возникнуть сложности в достижении рекомендуемого уровня физической активности [18].
В ходе мета-анализа, включившего 37 исследований, 34 рандомизированных клинических исследования, оценивали влияние физических упражнений на мышечную массу у пожилых людей (почти в 80% случаев мышечная масса увеличилась с помощью физических упражнений). Влияние дополнительного питания на мышечную массу было зафиксировано только в 23,5% случаев. Мышечная сила увеличилась в 82,8% исследований после повышения физической активности, а пищевые добавки показали дополнительные преимущества только в небольшом количестве исследований (22,8%). Таким образом, физические упражнения оказывают положительное влияние на мышечную массу и силу или физическую работоспособность у здоровых лиц в возрасте от 60 лет и старше [24].
Белок пищи оказывает косвенное влияние на ключевые регуляторные белки и факторы роста, связанные со здоровьем мышц и костей, за счет увеличения абсорбции кальция, подавления ПТГ и увеличения секреции ИФР-I (костного и мышечного анаболического стимулятора). Потребление белка более 0,8 мг/кг массы тела в день, в основном животного происхождения, усиливает анаболизм мышечного белка наряду с защитой от возрастной потери мышц и костной ткани. У пациентов в возрасте 70–79 лет содержание белка в пище в количестве 1,1 г/кг массы тела в день приводит к отсутствию мышечной потери при 3-летнем наблюдении.
ESCEO рекомендует потребление белка с пищей от 1,0 до 1,2 г/кг массы тела в день, минимум 20–25 г чистого белка в каждой порции. Европейское общество клинического питания и обмена веществ (ESPEN) и Исследовательская группа PROT-AGE рекомендуют такое же потребление белка для здоровых людей старшего возраста, от 1,2 до 1,5 г/кг массы тела в день, а для пациентов с тяжелыми заболеваниями и недостаточным питанием – свыше 2 г/кг в сутки [18]. Пациенты с хронической болезнью почек (ХБП) додиализных стадий для профилактики саркопении должны снизить потребление белка до 0,2–0,5 г/кг в сутки (при СКФ <20 мл/мин/1,73 м²) вследствие возможного развития метаболического ацидоза [25]. Кроме того, потребление белка совместно с физическими упражнениями улучшает синтез мышечного белка и положительно влияет на состав тела, способствуя снижению жировой массы, увеличению или поддержанию мышечной ткани и сохранению кости [18] (табл. 2).
Таблица 2. Рекомендуемое количество потребления белка в сутки различным группам людей
Количество потребляемого белка в сутки, г/кг массы тела