синдром шая дрейджера что это
Синдром шая дрейджера что это
В 1960 г. Шай и Дрейджер опубликовали результаты клинико-морфологического обследования двух больных, в клинической картине которых преобладали симптомы паркинсонизма и ортостатической гипотензии. Заболевание относится к числу редких, хотя в последние годы юно неоднократно описывалось в ряде работ; мы также имели возможность наблюдать несколько таких больных.
Вполне вероятно, что синдром Шая—Дрейджера встречается гораздо чаще, чем распознается. Обычно эти пациенты фигурируют в медицинской документации как больные паркинсонизмом.
Развернутая клиническая картина синдрома Шая—Дрейджера складывается в основном из умеренно выраженного акинетикоригидного синдрома с проявлениями гипокинезии, ахейрокинезом, пластической ригидностью и тремором, а также из выраженной ортостатической гипотензии. К числу характерных признаков относят также ангидроз, атонию мочевого пузыря, иногда с признаками недержания мочи, фиксированный сердечный ритм и (иногда) снижение тонуса ректального сфинктера.
В неврологическом статусе нередко находят клинические (и электромиографические) указания на вовлечение в патологический процесс клеток передних рогов спинного мозга. Возможны атрофия дистальных отделов конечностей, фасцикуляции. Реже определяют мозжечковые симптомы в виде более или менее выраженного интенционного тремора, адиадохокинеза и пр. Могут встречаться парезы наружных глазных мышц, атрофия радужной оболочки глаз.
Мужчины больше подвержены этому заболеванию. Болезнь дебютирует в возрасте 50—60 лет и быстро прогрессирует. Заболевание часто начинается с жалоб на утомляемость, слабость в конечностях, головокружения и непереносимость тепла (ангидроз). Затем появляются повторные синкопальные атаки, с которых иногда и начинается болезнь. Наиболее тягостным для больных является склонность к обморокам, которые в выраженных случаях могут наблюдаться даже в сидячем положении больного.
Головокружения и обмороки плохо поддаются обычной симптоматической терапии.
При перемене положения тела наблюдаются выраженные колебания артериального давления; Шай и Дрейджер приводят собственное наблюдение, в котором у больного систолическое давление снижалось со 170 в положении лежа до 40 мм рт. ст. в положении стоя. Характерным является незначительное изменение пульса при перемене положения тела.
Атония мочевого пузыря может сопровождаться учащенным мочеиспусканием и недостаточным произвольным управлением сфинктером. Некоторые авторы описывают при этом заболевании и другие симптомы, факультативно присутствующие в отдельных наблюдениях (сухожильная гиперрефлексия, симптом Бабинского, уменьшенное слезо- и слюноотделение, импотенция и др.).
Патоморфологические описания указывают на гибель нейронов в структурах вегетативной нервной системы, патологические изменения в кортико-нуклеарных и кортико-спинальных трактах, базальных ганглиях, мозжечковых связях. Морфологические находки указывают на нозологическую самостоятельность данного заболевания, сущность которого заключается в прогрессирующей знцефаломиелопатии неизвестной этиологии. Заболевание рассматривается как дегенеративное.
ШАЯ-ДРЕЙДЖЕРА СИНДРОМ
Шая-Дрейджера синдром (G. М. Shy, американский невропатолог, 1919—1967; G. A. Drager, американский невропатолог, родился в 1917 году) — дегенеративное поражение центральной нервной системы неясной этиологии, проявляющееся ортостатической артериальной гипотензией в сочетании на разных этапах болезни с симптомами паркинсонизма, нарушением потоотделения (ангидрозом), расстройством функции тазовых органов и другими неврологическими нарушениями. Заболевание встречается редко.
Еще до описания Шая—Дрейджера синдрома было известно редкое заболевание — идиопатическая ортостатическая гипотензия, ведущим проявлением которого является постуральное падение АД неясного генеза с тяжелыми ортостатическими расстройствами кровообращения. В 1960 году Шай и Дрейджер описали два случая такой гипотензии, обратив внимание на сочетание ее с симптомами распространенного органического поражения центральной нервной системы — ригидностью и дрожанием конечностей, потерей координации движений, атонией сфинктеров тазовых органов, нарушениями потоотделения. Так как эти нарушения предшествовали выраженной ортостатической гипотензии, Шай и Дрейджер предположили, что органические изменения центральной нервной системы при этом заболевании первичны, а не обусловлены ортостатическими расстройствами кровоснабжения мозга (см. Ортостатические изменения кровообращения). Однако перемежающаяся гипоксия мозга может приобретать дополнительное патогенетическое значение по мере развития болезни. В настоящее время идиопатическую ортостатическую гипотензию и Шая—Дрейджера синдром рассматривают как варианты проявления единой патологии и оба термина нередко употребляют как синонимы.
Содержание
Этиология
Этиология не известна. Токсическая природа дегенерации нервных структур маловероятна, хотя изменения, наблюдаемые при этом заболевании, сходны с изменениями, возникающими при хроническом отравлении некоторыми металлами. Имеется наблюдение семейной формы Шая—Дрейджера синдрома с доминантным типом наследования. Описано развитие синдрома Шая — Дрейджера при раке миндалины как (предположительно) паранеопластического процесса (см. Паранеопластические синдромы), что не исключает возможной роли в его происхождении аутоиммунных нарушений.
Патогенез
Патогенез изучен недостаточно. Морфологическим субстратом паркинсонизма при Шая-Дрейджера синдроме являются дегенеративные изменения клеток черной субстанции. Аминофф (М. J. Aminoff, 1973) и др. полагают, что в основе их формирования при Шая-Дрейджера синдроме лежат преимущественно стриарные и паллидарные поражения. Однако патогенез паркинсонизма при Шая-Дрейджера синдроме остается неясным и отличается от такового при болезни Паркинсона (см. Дрожательный паралич). Холинолитические вещества (см.) не ослабляют проявлений паркинсонизма при этом синдроме, а L-ДОФА в ряде случаев даже ухудшает соматические неврологические расстройства.
Относительно ясен генез ортостатической гипотензии, связь которой с выпадением симпатической регуляции гемодинамики доказывается не только патологоанатомическими данными, но и сведениями о концентрации норадреналина в крови больных. У здоровых лиц при переходе из горизонтального положения в вертикальное содержание норадреналина в крови возрастает в среднем почти в 1-2 раза и обусловлено ортостатической активацией тонуса симпатических нервов. У больных с Шая-Дрейджера синдромом такого прироста концентрации норадреналина в ортостазе не наблюдается (она даже снижается), в то время как при горизонтальном положении тела она близка к нормальной (лишь в некоторых случаях обнаруживается снижение концентрации норадреналина в крови и цереброспинальной жидкости). Гемодинамика и тонус периферических сосудов в горизонтальном положении у больных существенно не отличаются от нормы, но в вертикальном положении не происходит наблюдаемого у здоровых учащения сердцебиений (так называемый фиксированный темп) и резко снижены или отсутствуют сосудистые реакции, наиболее зависимые от симпатической регуляции (см. Ортостатические изменения кровообращения). Это приводит к снижению сердечного выброса, не компенсируемому ростом периферического сосудистого сопротивления, в результате чего у больных с синдромом Шая — Дрейджера при переходе из горизонтального положения в вертикальное круто падает и систолическое, и диастолическое АД, снижается приток крови к головному мозгу и вследствие его диффузной ишемии развивается обморок.
Снижение тонуса симпатических нервов проявляется гипофункцией потовых желез, ослаблением потоотделения при повышении температуры, а также значительным повышением чувствительности альфа-адренорецепторов кровеносных сосудов к нор-адреналину. Последнее проявляется тяжелыми гипертензивными реакциями даже при весьма медленном внутривенном введении больным норадреналина (со скоростью всего 0,5 или даже 0,1 мкг/кг в 1 минуту). Поскольку L-ДОФА у больных с Шая-Дрейджера синдромом не оказывает центрального гипотензивного действия, нередко повышая АД (периферическое действие), можно сделать вывод о разобщении симпатических связей между головным мозгом и периферией.
Сведения о патогенезе других неврологических нарушений ограничены указанием на их связь с расстройствами соматической и вегетативной иннервации, дегенерацией клеток в разных структурах центральной нервной системы, включая дорсальное ядро блуждающего нерва, а также в симпатических ганглиях.
Патологическая анатомия
При патологоанатомическом исследовании изменения, специфичные для Шая-Дрейджера синдрома, макроскопически не выявляются. В некоторых случаях отмечается гипоплазия надпочечников с очаговой гиперплазией коркового вещества в виде мелких аденом.
Основные изменения обнаруживают в центральной нервной системе. Гистологически выявляются дегенерация нейронов скорлупы, черной субстанции, нижних олив, хвостатого ядра, дегенеративные изменения в мозжечке, варолиевом мосту, стрионигральном, стриатопаллидарном и оливопонтоцеребеллярных трактах, межуточном мозге, значительное уменьшение числа клеток Пуркинье, патологические изменения клеток вентрального столба, интермедиолатеральной субстанции спинного мозга и клеток столбов Кларка, изменения нейронов вегетативных ганглиев. Выражена глиальная реакция, но признаки воспаления отсутствуют. С наибольшим постоянством выявляется уменьшение клеток в интрамедиолатеральной субстанции спинного мозга. По данным Потье (J. С. Potier, 1969), дегенерация в боковых рогах спинного мозга более выражена, чем в симпатических ганглиях.
Клиническая картина. Шая-Дрейджера синдром наблюдается у лиц обоего пола, чаще всего в возрасте 50—70 лет. Первые обращения к врачу связаны, как правило, с появлением ортостатических гемодинамических расстройств. Вначале больные жалуются на слабость, утомляемость, неустойчивость походки. В последующем длительное стояние становится невозможным из-за «головокружений», потемнения в глазах, предчувствия потери сознания. Затем тяжесть ортостатических нарушений быстро прогрессирует, часто возникают ортостатические обмороки, которые становятся доминирующими и определяют тяжесть состояния больного независимо от степени сопутствующих неврологических нарушений. В течение нескольких месяцев интервал времени от момента перехода больного из горизонтального положения в вертикальное до возникновения обморока сокращается до нескольких минут, в последующем — до 1 минуты и менее. В тяжелых случаях обморок (см.) может возникнуть даже в положении сидя в постели, пассивный перевод больного в вертикальное положение угрожает развитием глубокого обморока с тяжелой ишемией мозга.
В анамнезе у таких больных нередко выявляют предшествующие (за несколько месяцев или за 1—3 года до появления ортостатических нарушений) другие симптомы болезни — чаще всего снижение либидо у женщин, импотенция у мужчин, вегетативные расстройства (дизурия, нарушения потоотделения, функции кишечника). У некоторых больных проявления болезни в течение нескольких лет ограничиваются описанными выше прогрессирующими ортостатическими гемодинамическими расстройствами без других отклонений в неврологическом статусе. В большинстве же случаев через несколько месяцев после возникновения ортостатических гемодинамических нарушений или одновременно с их появлением (реже раньше) обнаруживаются ригидность и дрожание мышц конечностей, расстройства координации.
ЭЭГ у больных с синдромом Шая — Дрейджера не имеет специфических особенностей; обычно выявляется диффузная дизритмия, иногда медленная активность.
При отсутствии мозжечковой атаксии (см.) больные часто пытаются адаптировать походку и позы тела к ортостатическим изменениям гемодинамики. Они передвигаются широкими, направленными чуть в сторону быстрыми шагами на слегка согнутых в коленях ногах, низко наклонив туловище вперед и опустив голову (поза конькобежца). Чтобы продлить время пребывания в вертикальном положении, больные принимают напряженные, иногда причудливые позы — нередко скрещивают ноги, сдавливая сильным напряжением мышц вены голеней и бедер, что увеличивает венозный возврат крови к сердцу.
При обследовании больных в горизонтальном положении существенных изменений деятельности внутренних органов (кроме связанных с сопутствующими заболеваниями, осложнениями или обусловленных расстройствами нервной регуляции) не отмечается: АД нормальное, иногда повышено или умеренно снижено; характерна его нестабильность при почасовом и ежесуточном измерении. При проведении ортостатических проб (см.) реакция АД и пульса соответствует асимпатико-тоническому типу нарушений ортостатической регуляции — быстро падает как систолическое, так и диастолическое АД при отсутствии изменений частоты пульса или незначительном его учащении, возникает и быстро прогрессирует «алебастровая» бледность кожи головы, лица, шеи, верхней половины туловища, взор больного становится нефиксированным, наступает обморок и при отсутствии посторонней помощи больной может упасть. В положении больного лежа сознание постепенно возвращается, и в течение нескольких часов после этого больной отмечает выраженную слабость, утомляемость, сонливость.
Осложнения, наблюдаемые при Шая-Дрейджера синдроме, наиболее часто связаны с ортостатическими гемодинамическими расстройствами: возможны травмы вследствие падения при обмороке, расстройства психики и интеллекта в результате перемежающейся ишемии коры головного мозга, у лиц пожилого возраста иногда развиваются ишемические инсульты. Нарушения функции органов мочевой системы часто осложняются циститом, пиелитом.
Диагноз
Диагноз при раннем развитии ортостатических гемо динамических расстройств, обусловленных дефицитом симпатической активности, не вызывает затруднений. Иногда возникает необходимость в исключении органической окклюзии внутренней сонной артерии (см. Сонные артерии) и синдрома каротидного синуса. В случаях, когда ортостатическая артериальная гипотензия появляется уже на фоне выраженных соматических неврологических нарушений, ранняя диагностика трудна.
Дифференциальный диагноз в зависимости от синдрома неврологических расстройств проводят с болезнью Паркинсона, последствиями энцефалита, вторичными дегенеративными изменениями центральной нервной системы при различных заболеваниях и интоксикациях. Развивающиеся при паркинсонизме вегетативные расстройства (ангидроз, энурез, атония сфинктера прямой кишки) возникают позже, чем при Шая-Дрейджера синдроме и значительно менее выражены. Для постэнцефалитического паркинсонизма характерны гиперсаливация (см. Слюноотделение), гипергидроз (см.), блефароспазм (см.), замедление и инертность психических процессов. Дифференциальный диагноз с дегенеративными изменениями центральной нервной системы токсического генеза основывается на тщательном токсикологичском анамнезе и выявлении признаков поражения периферических нервов, которое не свойственно синдрому Шая — Дрейджера.
Лечение
Лечение заключается в коррекции наиболее тяжелых проявлений болезни — ортостатических расстройств гемодинамики и паркинсонизма. Для ограничения скорости развития ортостатической артериальной гипотензии применяют тугое бинтование конечностей, тазового пояса и живота. Из фармакологических средств чаще других эффективны синтетические фторсодержащие кортикостероиды, механизм действия которых не ясен (эффект не совпадает с увеличением объема крови и задержкой солей), и дигидрированные алкалоиды спорыньи (дигидроэрготамин или дигидроэрготоксин внутрь или в виде внутримышечных инъекций). Применение альфа-адреномиметиков менее эффективно и сопряжено с возникновением артериальной гипертензии в горизонтальном положении больного и опасностью развития осложнений. В отдельных случаях несколько улучшают переносимость вертикального положения ингибиторы МАО, тирамин, обогащенная солью диета; описан положительный результат применения индометацина. Мосс (A. J. Moss) и др. (1980) сообщили о значительном улучшении состояния больного после имплантации кардиостимулятора, задающего частоту сокращений предсердий 100 в 1 минуту.
Паркинсонизм при Шая-Дрейджера синдроме резистентен к применению L-ДОФА и с трудом поддается коррекции. Имеются сообщения об эффективности сочетанного применения циклодола и дибензипина.
Прогноз
Обычно болезнь быстро прогрессирует. В редких случаях наблюдается относительная стабилизация проявлений Шая-Дрейджера синдрома на 3—5 лет. Летальный исход у большинства больных может наступить через 7—8 лет после появления первых симптомов.
Синдром шая дрейджера что это
2. Спорадическая оливопонтоцеребеллярная атрофия (ОПЦА). При ОПЦА преобладает мозжечковая симптоматика (особенно атаксия и дизартрия), хотя редко бывает изолированной. Другими сопутствующими проявлениями могут быть паралич взора, гиперрефлексия, патологические стопные знаки и, что особенно важно, признаки паркинсонизма.
3. Синдром Шая-Дрейджера (Shy-Drager). При синдроме Шая-Дрейджера наблюдается дисфункция вегетативной нервной системы, что проявляется ортостатической гипотензией, нарушением функций тазовых органов, импотенцией.
Неясен вопрос о том, являются ли эти нарушения различными по сущности или только клиническими вариантами одного патологического состояния. Однако они обычно наблюдаются одновременно и имеют схожую патологическую картину. С диагностической точки зрения синдром МСА должен быть заподозрен у пациентов с гипокинезией, недостаточным эффектом леводопы при наличии значительных вегетативных или мозжечковых отклонений.
Методы нейровизуализации. МРТ головного мозга выявляет гипоинтенсивность в области скорлупы при СНД, вероятно, вследствие избыточного накопления железа в этой структуре. При ОПЦА можно наблюдать атрофию мозжечка.
Патоморфология. Общим признаком всех синдромов МСА является наличие характерных глиальных цитоплазматических включений. В дополнение к этому при синдроме Шая-Дрейджера обнаруживаются утрата нейронов и глиоз в двигательных ядрах блуждающего нерва и структурах спинного мозга, ответственных за вегетативную регуляцию.
4. Синдромы деменции. Болезнь Альцгеймера, болезнь Пика и болезнь с диффузными тельцами Леви —¦ это дегенеративные поражения ЦНС с преобладанием в клинической картине признаков деменции. Хотя дегенеративный процесс при этих заболеваниях затрагивает преимущественно некоторые области коры, могут быть вовлечены и подкорковые структуры, что приводит к развитию экстрапирамидных нарушений, включая паркинсонизм. Ключ к идентификации первичных дементных нарушений как причины паркинсонизма — это раннее появление признаков деменции, предшествующее развитию гипокинезии или ригидности.
Нейродегенеративные заболевания
Болезнь Вильсона — это аутосомно-рецессивное состояние, которое связано с нарушением экскреции меди, что приводит к накоплению ее в различных органах и системах, включая ЦНС, печень (цирроз), роговицу (кольца Кайзера-Флейшера), сердце и почки.
Болезнь Вильсона может начинаться в широком возрастном диапазоне — от 5 до 50 лет, но чаще всего в возрасте 8—16 лет. Неврологические расстройства присутствуют в начале заболевания примерно у 40 % больных. Такие экстрапирамидные симптомы, как дистония, ригидность и брадикинезия наиболее часто встречаются у детей, в то время как у взрослых более вероятно появление тремора и дизартрии. При болезни Вильсона могут наблюдаться разнообразные психические расстройства. Чрезвычайно важным для установления правильного диагноза является наличие печеночных расстройств (цирроз или хронический активный гепатит), особенно у молодых пациентов. Комбинация брадикинезии и тремора у этих больных позволяет предполагать болезнь Паркинсона. Однако слишком молодой возраст пациентов при появлении первых признаков заболевания, наличие психических расстройств, нарушений функций печени или дистонии являются основанием для поиска лабораторного подтверждения болезни Вильсона. Поскольку последствия этого заболевания предотвратимы при условии раннего назначения специфического лечения, возможность его наличия должна всегда учитываться при дифференциальном диагнозе вариантов атипичного паркинсонизма, особенно у людей моложе 50 лет.
Методы нейровизуализации. МРТ головного мозга выявляет расширение желудочков, а также атрофию в области коры и стволовых отделов. Базальные ганглии, особенно скорлупа, могут иметь гипо- или гиперинтенсивный характер в Т2-режиме исследования и гиподенсивный при КТ.
Иногда эти изменения в срезах среднего мозга при МРТ выглядят как «лицо гигантской панды».
Патоморфология. Наблюдается генерализованная атрофия мозгового вещества. Скорлупа, бледный шар и хвостатое ядро содержат кавитации и коричневый пигмент, что отражает накопление меди. d. Другие тесты. Наиболее информативный лабораторный тест —определение церулоплазмина плазмы, который обычно ниже 20 мг/дЛ (норма — 25—45 мг/дЛ). Уровень меди й плазме снижается, а выведение меди с мочой увеличивается. Исследование роговицы в свете щелевой лампы позволяет обнаружить кольца Кайзера-Флейшера почти у всех пациентов с неврологическими расстройствами, что является высокоспецифической, но не патогномоничной находкой. Если один или более из данных тестов в норме и диагноз вызывает сомнения, его следует подтвердить с помощью биопсии печени, которая позволяет констатировать увеличение содержания меди.
— Вернуться в оглавление раздела «Неврология.»
Лечение мультисистемной атрофии
Мультисистемная атрофия – прогрессирующее дегенеративное заболевание, которое поражает сразу несколько отделов нервной системы. Заболевание встречается редко и обычно возникает у лиц старше 40 лет. Врачи Юсуповской больницы проведут диагностику, назначат эффективную терапию и подберут индивидуальную программу реабилитации.
Виды мультисистемной атрофии
В зависимости от характера клинической картины выделяют три варианта мультисистемной атрофии:
При мультисистемной атрофии поражается вегетативная нервная система, регулирующая деятельность внутренних органов (например, артериальное давление или тазовые функции). Данные нарушения проявляются ортостатической гипотензией (слабость, головокружение, потери сознания), перебоями в работе сердца, запорами, недержанием мочи, изменением потоотделения и эректильной дисфункцией.
Синдром паркинсонизма: симптомы
При этом заболевании также выявляется синдром паркинсонизма, который включает замедленность движений, мышечную ригидность, тремор. Отличительной чертой данного вида паркинсонизма является раннее развитие изменений позы и неустойчивости, частые падения и отсутствие стойкой реакции на препараты леводопы (эффективен при болезни Паркинсона).
При мозжечковой форме наблюдаются нарушения равновесия и координации. Могут выявляться изменения речи, трудности с глотанием и аномальные движения глаз.
Диагностика и лечение мультисистемной атрофии
Диагностика мультисистемной атрофии является комплексной в связи с неспецифическими симптомами. Первым этапом является тщательный сбор жалоб и анамнеза и неврологический осмотр. Далее проводится магнитно-резонансная томография головного мозга, пробы на выявление нарушений артериального давления, консультации уролога и кардиолога.
Лечение мультисистемной атрофии является симптоматическом, так как не существует препаратов, изменяющих течение заболевания. Медикаментозная терапия включает применение лекарственных средств, улучшающих двигательную активность, а также препаратов, купирующих вегетативные симптомы. Пациентам необходимо проведение реабилитационных мероприятий: физической, физиотерапевтической, логопедической, психологической терапии.
Высококвалифицированные специалисты Юсуповской больницы проведут полную диагностику в случае подозрения на мультисистемную атрофию, а также назначат необходимую терапию и программу реабилитации, которая позволит значительно улучшить качество жизни пациентов.
Остались вопросы? Мы вам перезвоним
Мы с радостью проконсультируем вас и ответим на все интересующие вопросы.
PsyAndNeuro.ru
Методы диагностики МСА на ранних стадиях
Мультисистемная атрофия (МСА) – это спорадическое фатальное нейродегенеративное заболевание с началом во взрослом возрасте, характеризующееся прогрессирующей вегетативной недостаточностью, паркинсонизмом, мозжечковым и пирамидным синдромами в различных комбинациях. МСА считается редким заболеванием (см. www.orpha.net ) : оно встречается в 3,4 – 4,9 случаях на 100 000 населения, но для группы старше 40 лет – 7,8.
Аутопсическим индикатором становится большое скопление α-синуклеина в олигодендроцитах вкупе со стриатонигральной дегенерацией или оливопонтоцеребеллярной атаксией.
МСА выделилась в отдельную нозологическую форму в 1969 г., обобщив три ранее отдельных диагноза. До начала XX века заболевание существовало под разными названиями: стриатонигральная дегенерация (СНД), оливомостомозжечковая атрофия (ОПЦА) и синдром Шая-Дрейджера (по имени исследователей Джорджа Милтона Шая и Глена Алберта Дрейджера).Термин МСА служит отныне отдельной клинико-патоморфической единицей для разнообразных сочетаний симптомов МСА. Термин «синдром Шая-Дрейджера» более не используется.
На данный момент заболевание имеет два подкласса: МСА-п (паркинсонического типа, или стратонигральная дегенерация, MSA-p – англ.) и МСА-ц (оливопонтоцеребеллярная атрофия, MSA-c – англ.). Различие двух типов становится ярче по мере прогрессирования заболевания.
Диагностика МСА очень затруднительна. Как правило, начало болезни приходится на шестой десяток жизни пациента. Продолжительность жизни варьируется от 6 до 15 лет после постановки диагноза.
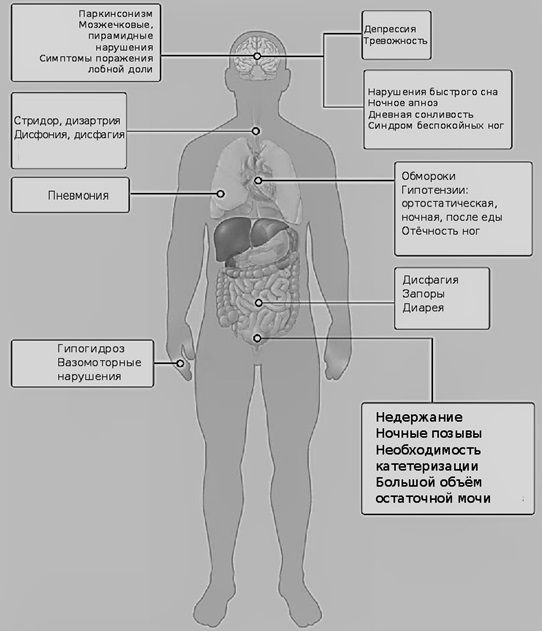
Симптоматика носит смешанный характер: помимо паркинсонизма, мозжечковой атаксии, двигательной атаксии, ортостатического коллапса , выявляются проблемы вегетативной системы (см. Табл. 1, и рис.1). Преобладание паркинсонизма или же мозжечковой атаксии предопределяет возможность (possible) или вероятность заболевания (probable, definite) и выбор подтипа.
Рис. 1 Мультидисциплинарное проявление МСА. Перевод на русский язык. Источник: Fanciulli, Alessandra, and Gregor K. Wenning. “Multiple-system atrophy.” New England Journal of Medicine 372.3 (2015): 249-263
В ходе лечения на первых порах можно отметить реакцию на леводопосодержащие медикаменты, но со временем их эффективность снижается. Для обоих типов МСА характерно драматически быстрое развитие болезни. Потеря автономности пациента сопровождается трудностями пищеварения, дыхания (стридор может вести к необходимости трахеостомии). По статистике, приведённой A. Фанчулли и Г. Веннингом, во время сна у 40% пациентов замечено ночное апноэ. На поздних стадиях заболевания следует избегать условий для развития пневмонии. Кроме того, МСА сопутствует гипертензия в позе лёжа. Во время сна у пациентов отмечается нарушение движений глазных яблок во время быстрого сна [5]. Также замечено уменьшение потоотделения, недержание (в т.ч. ночной полиурией), у мужчин – эректильная дисфункция. При этом следует учитывать, что последние два из перечисленных симптомов могут быть не связаны с МСА. Но в любом случае требуется превентивное и постоянное лечение инфекций мочевыводящих путей.
На более развитых стадиях болезни у 50% пациентов по статистике Фанчулли и Веннинга испытывают парализующую боль. Характерным условием для развития этого симптома была дистония. Симптом чаще наблюдается у женщин.
В обыденной жизни пациенты сталкиваются не только с ограничениями медицинского характера, но и с каждодневными трудностями, которые накладывает болезнь. Внешние проявления болезни выражаются в необычной походке, положении головы. Из-за спазмов на лице больных МСА иногда появляется “сардоническая улыбка”. При МСА-п непроизвольно происходит сильный наклон или вытягивание головы вперёд. Скованность и замедленность движений затрудняют выполнение рутинных задач.
Редкое заболевание известно далеко не всем, и порой вызывает непонимание окружающих. Поэтому в публичных местах из-за физических ограничений пациенты испытывают стресс, ограничивают себя в социализации, избегают людных мест, что создаёт дополнительные факторы для усугубления сопутствующей депрессии и психологического дискомфорта (см. «нейропсихологические проявления», Табл. 1).
Урология
2. Увеличенный объём остаточной мочи, недержание
Жалобы на хронический запор
Преобладает при МСА-п
4. Тремор покоя или движения
Преобладает при МСА-ц
Заметна скованность движений
2. Гиперрефлексия
5. Дневная сонливость (17%)
6. Неприятные ощущения в нижних конечностях (синдром беспокойных ног)
*Клинические проявления МСА среди 437 пациентов, EMSA-registry.
Карло Колозимо предлагает синтетическую таблицу основных и дополнительных критериев диагностики МСА (Таблица 3.5, глава “Multiple system atrophy”, Carlo Colosimo, David E. Riley, Gregor K. Wenning, Handbook of Atypical Parkinsonism, Cambridge University Press, 2011, P. 36.)
Основные критерии:
Дополнительные симптомы
Диагностика заболевания, как уже было сказано, затруднена. Нет единого критерия или сочетания симптомов, которые могли бы однозначно указать на МСА с самого начала болезни. Выход на финальный диагноз проводится методом исключения по мере её развития. При всех общих неизвестных, первостепенным аргументом для подтверждения МСА остаётся снимок МРТ (как минимум 1,5 тесла). Но анализ МРТ на начальных стадиях не даёт точной уверенности, поэтому как правило первоначальным диагнозом становится болезнь Паркинсона (БП). Более достоверное выявление потери нейронов возможно на снимках ПЭТ (PET, позитронно-эмиссионная томография) или ОЭМТ (SPECT,однофотонная эмиссионная компьютерная томография).
Подтипы МСА изображены на фиг. 1 и 2. [1]
Фиг. 1 А : двусторонняя атрофия в области скорлупы, гиперинтенсивность края (отмечено стрелочками). В-С : гиперинтенсивность двустороннего кортикопинального тракта в кортикальной и подкорковой предцентральной извилине и за пределом тракта (С).
Фиг. 2 A : “крест” в области варолиевого моста (“hot cross bun” (англ.) – по внешней схожести с пасхальным хлебом “мазанецем”, “крестовой булочкой”), B-C : гиперинтенсивность в области двустороннего кортикопинального тракта в подкорковой предцентральной извилине и за пределом тракта (С).
При МСА-п (паркинсонического типа, MSA-p)(характерный снимок-см. Фиг. 1) заметны проявления брадикинезии и ригидности; гипокинетической дизартрии; постуральная неустойчивость; часто – тремор покоя.
На 2003 г. случаи паркинсонического подтипа встречались вдвое-вчетверо раз чаще, чем МСА-ц в западном полушарии. Однако МСА-ц чаще встречается в Японии. По собранной на данный момент статистике МСА-п начинает уступать по частоте МСА-ц.
МСА-ц (оливоцеребеллярная атрофия, MSA-c)(характерный снимок – см. Фиг. 2) характеризуется прежде всего мозжечковой атаксией; постепенным, но неуклонным затруднением движения, речи и походки, а также движения глазных яблок и работы верхних век. У пациентов с МСА-ц чаще наблюдается тремор действия, например, при доставании предметов. Мышечная слабость при МСА-ц может привести к невнятной речи и попёрхиванию при глотании. Яркие проявления обнаруживаются среди ортостатических расстройств кровообращения: у пациента могут быть обмороки, слабость с головокружнием, тошнота, дрожь, боль области шеи и плеч. Мозжечковая дисфункция проявляется на более ранних стадиях и сочетается более заметным затруднением дыхания во время сна.
В статье французской исследовательской группы из Тулузы MRI Supervised and Unsupervised Classification of Parkinson’s Disease and Multiple System Atrophy приводится предварительный вывод многостороннего анализа снимков МРТ пациентов обоих подтипов МСА. На развитой стадии МСА (начало болезни наблюдаемых варьировалось между 5 и 7 годами) с высокой степенью вероятности можно отличить МСА от БП, опираясь только на МРТ-данные. Изменения отображаются на снимках в области:
1) лучистого венца верхнего отдела пирамидного пути (обе стороны),
2) верхней извилины лобной доли.
Для МСА-п характерны сокращение фракционной анизотропии в скорлупе, дополнительной моторной области и лучистом венце верхнего отдела пирамидного пути. Исходя из снимков МРТ, труднее отличить от бП МСА церебеллярного типа [7].
С помощью фтордеоксиглюкозы на снимках ПЭТ видны гипометаболизм в стриатуме, в основном в путамене, также стволе головного мозга и мозжечке при МСА-п. При МСА-ц – в основном в путамене, а также может быть заметна потеря допаминергических нейронов нигростриарного пути.
| Тест | Типичный результат |
| Кардиоваскулярные тесты | Ортостатическая гипотензия Низкий коэфициент при пробе Вальсавы Слабое выделение норадреналина в лимфе, слабое сосудосужение |
| Определение уровня глюкозы | Слабый релизинг гормона роста (спорный результат) |
| Тест терморегуляции и количественный тест вызванного судомоторного аксон-рефлекса | Судомоторная дисфункция, проявляющаяся гипо- ангидрозом |
| Электрофизиологические исследования (sympathetic skin response) | Кожный симпатический потенциал либо отсутвует, либо аномальный |
| Тест цереброспинальной жидкости | Повышенный уровень нейрофиламентов |
| Электромиография наружного сфинктера заднего прохода | Либо денервация, либо раздражение (нерелевантные результаты) |
| Транскраниальная сонография | Гиперэхогенность чечевицеобразного ядра и нормальная эхогенность чёрной субстанции |
| Компьютерная томография | Не дала результатов |
| МРТ на 1,5 тесла | Аномалии в базальных ганглиях, «крест» в области варолиевого моста, атрофия мозжечка или ствола мозга |
| ДВИ (диффузно-взвешенное изображение) | Диффузность в области путамена, варолиева моста и средней ножки мозжечка |
| Волюметрия | Потеря объёма в путамене при МСА-п, потеря объёма в стволе и мозжечке при МСА-ц |
| Cканирование с радиоактивным изотопом-метайодобензилгуанидином MIBG | В норме |
| Сканирование переносчиков Иофлупаном I123 (123I-FP-CIT SPECT imaging) | Недостаток транспортёров дофамина в полосатом теле |
| Сканирование переносчиков йодобензамидом I123 123I-IBZM-SPECT | Недостаток транспортёров дофаминового рецептора D2 в полосатом теле |
| ПЭТ с флуородопой | Недостаток захвата флуорисцентной леводопы |
| ПЭТ с раклопридом | Недостаток транспортёров дофаминового рецептора D2 в полосатом теле |
| ПЭТ с изохинолиновым карбоксамидом PK-11195 | Микроглиальная активация в области базальных ганглий и ствола мозга |
| ПЭТ с использованием радиофармпрепарата фтордеоксиглюкозы | Замедленный метаболизм |
Благодаря дополнительным тестам на данный момент выявлены несколько направлений, в которых будет развиваться диагностика. Они базируются не только на исключении других болезней или изучении снимков ПЭТ (см. Табл. 3, Типичные результаты дополнительных тестов.), но и на анализе офтальмологических особенностей МСА, терморегуляции, дисфункции вегетативной системы. Остановимся на результатах некоторых из них.
Офтальмологические особенности МСА
Целевое ретроспективное наблюдение больных МСА в клинике Мэйо (Рочестер, Миннесота, США) позволило выявить основные аномалии зрения, сопутствующие заболеванию. Из 285 рассмотренных случаев были отобраны 39 пациентов с подтверждённым диагнозом. Среди пациентов с МСА-п 14 человек жаловались преимущественно на синдром сухого глаза, у 13-ти были выявлены асинхронность глазных движений. У 7-х было отмечено смещение или ограничение движения глазного яблока, у одного пациента наблюдалась монокулярная диплопия (двоение изображения для одного глаза) из-за аномального роста ресниц. Единичными случаями стали двусторонняя атрофия зрительного нерва и синдром Холмса – Эйди (парасимпатическая денервация зрачка, проявляющаяся мидриазом со снижением, а иногда и полным исчезновением способности зрачка сужаться, реагируя на свет ).
Следует различать аномалии, которые по независимым причинам сопровождают МСА, и те, которые проистекают из заболевания. К последним относятся, по предположению учёных, атрофия глазного нерва и рубцевание конъюнктивы (рубцовый пемфогоид).
Среди наблюдаемых с МСА-ц офтальмологические особенности чаще всего проявляются в асинхронности движения и смещении глазного яблока. Особо выделена корреляция длительности жизни пациентов после установления диагноза и зрительными аномалиями, за исключением синдрома “сухого глаза”. В связи с этими наблюдениям медики призывают пациентов с МСА регулярно проходить офтальмологическое обследование с целью раннего выявления аномалий и предупреждения несчастных случаев по причине плохого зрения [2].
Особенности ортостатического давления и пульса при МСА
Среди критериев, указывающих на вероятное развитие болезни, отмечено падение ортостатического давления. Ортостатическая проба заключается в замере давления стоя. За три минуты в стоячем положении систолическое давление падает как минимум на 20-30 мм.рт.ст., а диастолическое – на 10-15 мм.рт.ст. при заниженном сердцебиении. Поэтому пациентам с МСА желательно носить абдоминальный бандаж, компрессионное бельё, увеличить частоту потребления воды и соли, а также медикаментов для повышения артериального давления.
Признаки тахикардии с гипотонией являются характерной особенностью пациентов с вегетативными нарушениями. Но диапазон нарушений пока ещё не изучен. В статье Orthostatic Heart Rate Changes in Patients with Autonomic Failure caused by Neurodegenerative Synucleinopathies сообщается о диапазоне ортостатических изменений сердечного ритма у пациентов с вегетативной недостаточностью, в том числе и при МСА.
При МСА речь идёт о вегетативной нервной системе. Ортостатическая гипотензия вызвана нарушением активации симпатических вазоконстрикторных нейронов. Сердечный пульс значительно выше у пациентов с МСА в отличие от других пациентов с заболеваниями, связанными с образованием телец Леви, и в частности БП. Заметное повышение сердечного ритма при МСА объясняется тем, что постганглионарные волокна и их аксоны остаются почти незатронутыми, однако при этом констатируется потеря вегетативных нейронов головного и спинного мозга [3]. Это, например, проявляется в том, что у пациентов с МСА очень низкая температура конечностей: холодные ладони и ступни [4].
Потоотделение при МСА
У пациентов с МСА, по сравнению с БП, значительно ниже показатели потоотделения ладоней и особенно ступней. Гипогидроз (пониженная потливость) или вовсе отсутствие потоотделения при МСА считается связанными с дегенерацией центральных предганлиев [6].
Изучение МСА затруднено редкостью заболевания, затруднённой диагностикой на начальной стадии и тем, что до сих пор не найдены способы эффективного торможения болезни. Интерес к разносторонним проявлениям болезни может в будущем привести к раннему выявлению заболевания, улучшенному лечению и повышению качества жизни пациентов.
Термины:
Проба Вальсальвы (напряжение по Вальсальве) — это форсированное выдыхание при закрытом носе и рте.
Гипокинетическая дизартрия — вид экстрапирамидной дизартрии, возникающий при поражении подкорковых узлов и их нервных связей.
Стриатонигральная дегенерация — спорадическое прогрессирующее нейродегенеративное расстройство, которое представляет собой одно из проявлений МСА. Проявляется, как правило, в снижении численности нейронов и глиозом в скорлупе, черной субстанции, стволе и мозжечке, а также в дегенерации клеток боковых рогов спинного мозга.
Оливопонтоцеребеллярные дегенерации — наследственные дегенеративные заболевания ЦНС, объединенные сходной локализацией патологического процесса в мозжечке, нижних оливах и мосте головного мозга.
Глазной рубцовый пемфигоид — заболевание, при котором происходит рубцевание конъюнктивы у пациентов пожилого возраста.
Монокулярная диплопия — ви́дение одним глазом двух или более изображений предмета.
Подготовила: Мартемьянова Е.О.
Помощь в редакции: Оськин С.
Carlo Colosimo, David E. Riley, Gregor K. WenningHandbook of Atypical Parkinsonism, Cambridge University Press (2011).
Fanciulli, Alessandra, and Gregor K. Wenning. “Multiple-system atrophy.” New England Journal of Medicine 372.3 (2015): 249-263.