синтез простагландинов что это
Синтез простагландинов что это
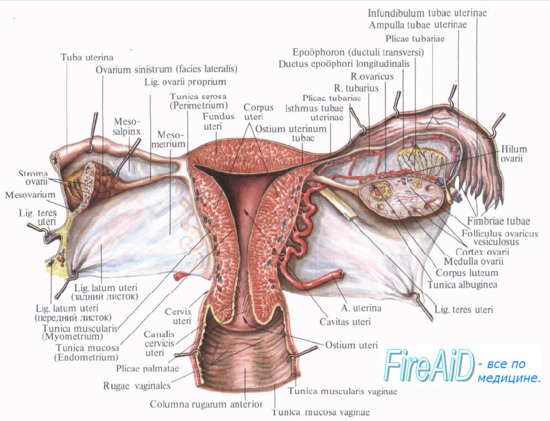
Простагландины ( ПГ ) представляют собой ненасыщенные жирные кислоты с 20 углеродными атомами, окружающими скелет молекулы простаноевой кислоты. Различают четыре серии натуральных простагландинов: Е, F, А и В. Особый интерес в репродуктивной физиологии представляют соединения серии Е и F.
Синтез простагландинов F2 и Е2 из ненасыщенных жирных кислот был осуществлен S. Bergstrom ct al. (1964) и DA Van Dorpet al. (1964), после чего эти вещества начали использоваться в клинике. Позже S. Bergstrom et al. были удостоены Нобелевской премии за синтез простагландинов и фундаментальные исследования в этой области.
Источником образования простагландинов является арахидоновая кислота. Знание механизма синтеза простагландинов в тканях является источником для понимания процесса родов. Биосинтез простагландинов осуществляется в различных тканях: простациклин ПЦ2 синтезируется в миометрии, Е2 — в амнионе и хорионе, ПГF2a — в децидуальной ткани.
Нет четких доказательств увеличения скорости образования ПГ во внутриматочных тканях до начала родов. Тогда как в родах имеется резкое возрастание концентрации ПГ Е2 и ПГ F2 амниотической жидкости. Возрастает также концентрация метаболитов ПГ F2, а именно 13-14 дсгидро-15 кето-ПГ F2 амниотической жидкости, крови и моче. С другой стороны нет четкого доказательства возрастания уровня ПГЕ2 (или метаболитов) в материнской крови (Mitchell M. D., 1988).
ПГ F2 может продуцироваться в децидуальной оболочке и в миометрии, по не в плодных оболочках, однако возрастание концентрации ПГ F2 и его метаболитов во время родов отмечено в амниотической жидкости, крови матери и моче.
Важно подчеркнуть, что амниотическая жидкость способствует сохранению простагландинов. Так, период полураспада ПГ F2 и Е2 в крови составляет 6- 8 мин, тогда как в амниотической жидкости он колеблется от 4 до 6 часов. Существует гипотеза, что децидуальная активность синхронна с началом родов. Во время родов в амниотической жидкости аккумулируются биологически активные вещества, а именно, арахидоновая кислота, простагландины, цитокины.
Концентрация арахидоновой кислоты в амниотической жидкости в родах возрастает в 5-10 раз.
Действие простагландинов осуществляется через фосфолипазу А2 или аденилатциклазпую систему, увеличивается количество рецепторов к ПГ Е2 и ПГ F2, а также возрастают концентрации гликозаминглнканов. Установлено, что ПГ Е2 в 10 раз активнее, чем ПГ F2a, что обусловлено количеством рецепторов,
В возникновении родовой деятельности простагландины Е и F играют важную роль. Механизм действия их на сократительную деятельность матки изучен недостаточно. Полагают, что механизм стимулирующего действия на матку реализуется деполяризацией клеточных мембран и освобождением ионов кальция (Са2+), что ведет к активации киназой легкой цепи миозина, фосфорилироваиию миозина и взаимодействию фосфорилированного миозина и актина (Carsten M.E., Miller J.D., 1983), а возможно, их прямым стимулирующим влиянием на гипофиз, в результате усиливается синтез окситоцина (Gillespie Л., 1973). Установлено, что при сочетанном применении ПГЕ2 или ПГ F2 с окситоцином эффективность действия смеси выше, чем одного простагландина.
Установлено, что манипуляции с плодными оболочками при влагалищном исследовании (отслаивание, введение баллона), амниотомия, манипуляции с шейкой матки способствуют выработке ПГ F2 и его метаболитов (Mitchell M.D., 197G; Mortimer G. et al., 1985; Mc Colgin S.W. et al., 1993)
Синтез простагландинов увеличивается и при прижатии плодных оболочек головкой плода. Их концентрация в передних водах выше, чем в задних.
Синтез простагландинов что это
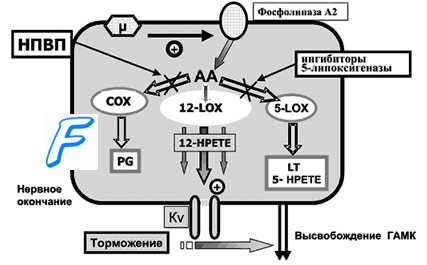
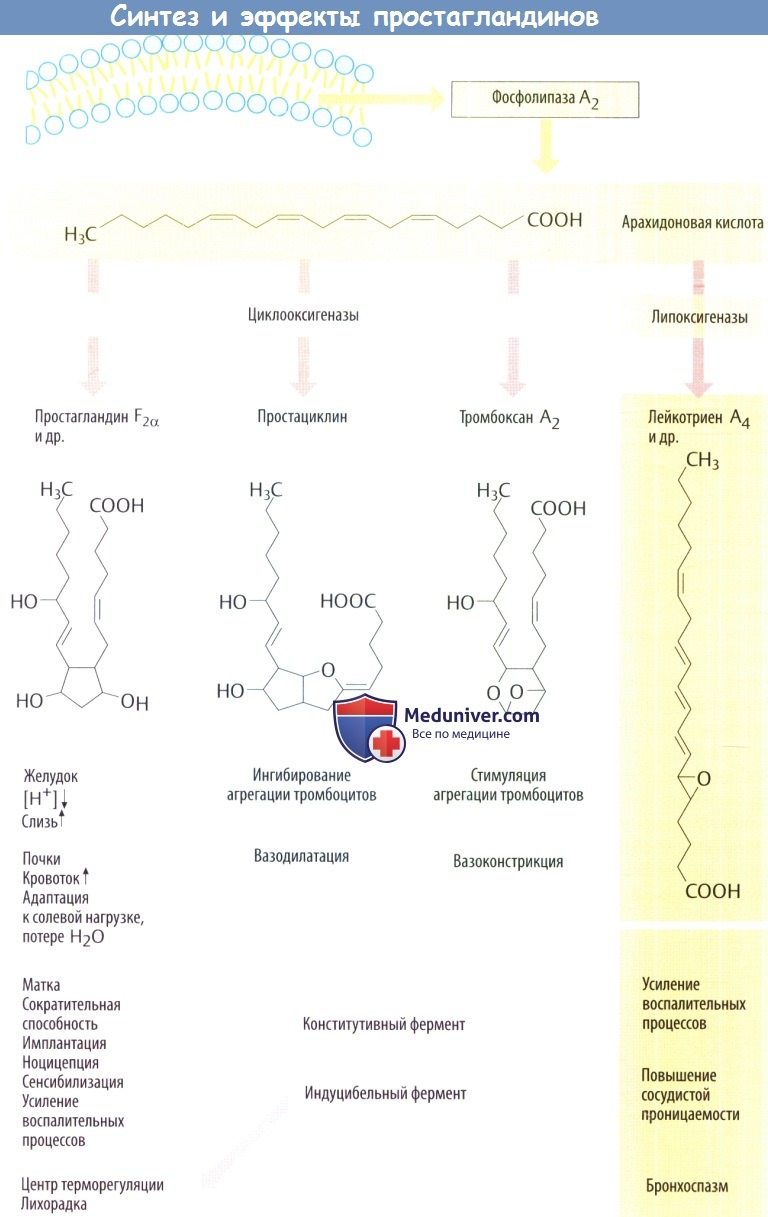
Под действием циклооксигеназ (ЦОГ-1, ЦОГ-2 и их сплайс-вариантов) растянутая молекула арахидоновой кислоты (эйкозатетраеновая кислота) превращается в соединения, содержащие центральное кольцо с двумя длинными заместителями: простагландины, простациклин и тромбоксаны.
Под действием липоксигеназы из арахидоновой кислоты синтезируются лейкотриены, которые в центре структуры не имеют кольца. Продукты, образованные из арахидоновой кислоты, действуют как местные гормоны и быстро инактивируются. В группы простагландинов и лейкотриенов входит большое количество близкородственных соединений. В данном разделе рассматриваются только наиболее важные простагландины и их основные эффекты.
а) Простагландин (PG) Е2 ингибирует секрецию желудочного сока и повышает выработку слизи, что защищает слизистую оболочку. PGF2α стимулирует сокращение матки. PGI2 (простациклин) вызывает расширение сосудов и способствует экскреции Na + в почках.
Кроме того, простагландины, синтезируемые ЦОГ-2, участвуют в воспалительных процессах, повышая чувствительность ноцицепторов, что снижает болевой порог, способствуя развитию воспалительной реакции за счет выделения медиаторов, таких как интерлейкин-1 и фактор некроза опухолей-α, и повышая температуру тела.
б) Простациклин синтезируется в эндотелии сосудов и участвует в регуляции кровотока. Он вызывает расширение сосудов и предотвращает агрегацию тромбоцитов, т. е. это функциональный антагонист тромбоксана.
Тромбоксан А2 —местный гормон, синтезируется в тромбоцитах и способствует их агрегации. Образование тромбоксана происходит при небольших дефектах в сосудистой или капиллярной стенке.
Лейкотриены образуются в основном в лейкоцитах и тучных клетках. Недавно установлено, что лейкотриены могут связываться с глутатионом. От этого комплекса отщепляется глутамин и глицин в результате чего образуется большее количество локальных гормонов. Лейкотриены обладают провоспалительным свойством; они стимулируют миграцию лейкоцитов и повышают их активность.
При анафилактических реакциях лейкотриены обусловливают расширение сосудов, повышение их проницаемости, а также могут вызывать сужение кровеносных сосудов.
Терапевтическое применение синтетических эйкозаноидов. Усилия по синтезу стабильных производных простагландинов для терапевтического применения пока не увенчались успехом. Динопростон (PGE2), гемепрост и сульпростан используются как стимуляторы сокращения матки. Мизопростон предназначен для защиты слизистой оболочки желудка, но характеризуется выраженными системными побочными эффектами. Все эти препараты не обладают органоспецифичностью.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Простагландины – универсальные биорегуляторы в организме человека (обзор литературы)
Авторы
Ключевые слова:
Аннотация
В последнее время учеными разных отраслей уделяется огромное внимание проблеме простагландинов.
Цель работы – на основе анализа данных отечественной и зарубежной литературы изучить и систематизировать основные вопросы структуры, биологического действия, метаболизма простагландинов в организме человека и применение их аналогов в фармации.
Простагландины – биологически активные вещества, близкие по своему действию к гормонам, но, в отличие от гормонов, они синтезируются не в эндокринных железах, а в клетках различных тканей организма. Простагландины как универсальные клеточные медиаторы широко распространены в организме, синтезируются в минимальных количествах практически во всех тканях, имеют как местное, так и системное воздействие. Для каждого простагландина существует свой орган-мишень. По химическому строению они небольшие молекулы, относящихся к эйкозаноидам – группе жироподобных веществ (липидов). В зависимости от химической структуры простагландины делятся на серии (A, B, C, D, E, F, G, H, I и J) и три группы (1–3); изомеры типа F обозначаются дополнительно буквами α и β.
Простагландины обладают чрезвычайно широким спектром физиологических эффектов, относятся к самым активным биогенных веществам, выполняют в организме три основные функции: поддерживающую, молекулярную, медиаторную. Большинство простагландинов взаимодействуют со специфическими рецепторами цитоплазматических мембран, однако некоторые простагландины (группа А) могут действовать нерецепторно. Запас простагландинов в организме отсутствует, жизненный цикл их короткий, они быстро образуются в ответ на воздействие биологических стимуляторов, проявляют свое действие в чрезвычайно скудных количествах и быстро инактивируются, попадая в кровь. В связи с чрезвычайно быстрым распадом в организме простагландины действуют в основном вблизи места их секреции. Препараты простагландинов и их производных используют в экспериментальной и клинической медицине для прерывания беременности и стимуляции родовой деятельности, терапии язвы желудка, бронхиальной астмы, некоторых сердечно-сосудистых заболеваний, врожденных пороков сердца у новорожденных, глаукомы, атеросклероза, ревматических, неврологических заболеваний, болезнях почек, сахарном диабете, коррекции гемостаза, как антикоагулянты при операциях с искусственным кровообращением, а также при гемодиализе.
Выводы. Простагландины – самые активные универсальные биогенные вещества в организме человека с чрезвычайно широким спектром физиологических эффектов. Они имеют как местное, так и системное воздействие, реализуют свое действие различными путями, их рецепторы содержатся практически во всех органах организма, для каждого простагландина существует свой орган-мишень. Указанные свойства простагландинов отражаются в их широком применении в медицине и фармации. Несмотря на активные исследования в данном направлении, у ученых остается много вопросов относительно механизмов действия, функций простагландинов и их аналогов в организме человека.
Библиографические ссылки
Bondarenko, O. A. (2012). Riven prostahlandyniv ta tsyklichnykh nukleotydiv u syrovattsi krovi khvorykh na khronichnyi pankreatyt, spoluchenyi z ozhyrinniam v dynamitsi zahalnopryiniatoho likuvannia [The level of prostaglandinums and cyclic nucleotides in serum blood of the patients with chronic pancreatitis, combined with obesity]. Ukrainskyi medychnyi almanakh, 15(2), 31–34 [in Ukrainian].
Victorov, О. P., Deyak, S. I., Bazyka, O. Y., Kashuba, O. V., & Matveyeva, О.V. (2011). Efektyvne ta bezpechne medychne zastosuvannia analhetykiv-antypiretykiv (pohliad na problemu) [Effective and safe analgetics-antipyretics use (problem view)]. Ukrainskyi medychnyi chasopys, 6(86), 90–93. [in Ukrainian].
Zharkova, T. S. (2015). Klinichne znachennia prostahlandyniv u formuvanni variantiv perebihu bakterialnykh kyshkovykh infektsii u ditei [Clinical significance of prostaglandins in the formation of courses of bacterial intestinal infections in children]. Zdorov’e rebenka, 62, 120–122. [in Ukrainian].
Zhuk, S. I., Khoroshaeva, N. E., & Salnikov, S. N. (2012). Dosvid dopolohovoi pidhotovky shyiky matky preparatamy, shcho mistiat promestryn [Experience of prenatal preparation of the cervix with drugs containing promestrin]. Reproduktivnaya e’ndokrinologiya, 4(6), 70–73 [in Ukrainian].
Ilkiv, I. I., Panasiuk, N. B., Biletska, L. P., & Skliarov, O. Ya. (2014). Zminy pokaznykiv systemy NO-syntaza/arhinaza za umov poiednanoi dii hostroho stresu ta blokuvannia tsyklooksyhenazy/lipooksyhenazy u tonkii kyshtsi [Changes indicators of NO-synthase/arginase under conditions combined effects of acute stress and blocking cyclooxygenase/lipooksyhenazе in the small intestine]. Eksperymentalna ta klinichna fiziolohiia i biokhimiia, 4, 19–25 [in Ukrainian].
Kuznietsov, S. V., & Zharkova, T. S. (2010). Rol prostahlandyniv u formuvanni klinichnoho variantu perebihu shyhelozu u ditei [The role of prostaglandins in the formation of the clinical alternative course of shigellosis in children]. Sovremennaya pediatriya, 3(31), 58–60 [in Ukrainian].
Pertseva, T. O., & Sanina, N. A. (2012). Rol systemnykh zapalnykh protsesiv u patohenezi khronichnoho obstruktyvnoho zakhvoriuvannia lehen [The role of systemic inflammation in the pathogenesis of chronic obstructive pulmonary disease]. Ukrainskyi pulmonolohichnyi zhurnal, 4, 48–50. [in Ukrainian].
Svintsitskyi, A. S., Kozak, N. P., & Antonenko, A. V. (2011). Adaptatsiia slyzovoi obolonky shlunka do dii nesteroidnykh protyzapalnykh preparativ [Adaptation of gastric mucosa to nonsteroidal anti-inflammatory drugs]. Ukrainskyi revmatolohichnyi zhurnal, 46(4), 1–3 [in Ukrainian].
Austin, S. C., Sanchez-Ramos, L., & Adair, C. D. (2010) Labor induction with intravaginal misoprostol compared with the dinoprostone vaginal insert: a systematic review and metaanalysis. Am J Obstet Gynecol, 202, 624.e1-9. doi: 10.1016/j.ajog.2010.03.014.
Brenneis, C., Coste, O., Altenrath, K., Angioni, C., Schmidt, H., Schuh, C. D., et al. (2011) Anti-inflammatory role of microsomal prostaglandin E synthase-1 in a model of neuroinflammation. J Biol Chem, 286(3), 2331–42. doi: 10.1074/jbc.M110.157362.
Brock, J. S., Hamberg, M., Balagunaseelan, N., Goodman, M., Morgenstern, R., Strandback, E., et al. (2016) A dynamic Asp-Arg interaction is essential for catalysis in microsomal prostaglandin E2 synthase. Proc Natl Acad Sci,113(4), 972–977. doi: 10.1073/pnas.1522891113.
Diakowska, D., Markocka-Mączka, K., Nienartowicz, M., Lewandowski, A., & Grabowski, K. (2014) Increased level of serum prostaglandin-2 in early stage of esophageal squamous cell carcinoma. Arch Med Sci., 10(5), 956–961. doi: 10.5114/aoms.2013.34985.
Facchinetti, F., Fontanesi, F., & Del Giovane, C. (2012) Pre-induction of labour: comparing dinoprostone vaginal insert to repeated prostaglandin administration: a systematic review and meta-analysis. J Matern Fetal Neonatal Med., 25, 1965–9. doi: 10.3109/14767058.2012.668584.
Hui, Y., Ricciotti, E., Crichton, I., Yu, Z., Wang, D., Stubbe, J., et al. (2010) Targeted deletions of cyclooxygenase-2 and atherogenesis in mice. Circulation, 121, 2654–2660. doi: 10.1161/CIRCULATIONAHA.109.910687.
Johansson, J. U., Woodling, N. S., Wang, Q., Panchal, M., Liang, X., Trueba-Saiz, A., et al. (2015) Prostaglandin signaling suppresses beneficial microglial function in Alzheimer’s disease models. J Clin Invest., 125(1), 350–364. doi: 10.1172/JCI77487.
Legler, D. F., Bruckne, M., Uetz-von Allmen, E., & Krause, P. (2010) Prostaglandin E2 at new glance: Novel insights in functional diversity offer therapeutic chances. Int J Biochem Cell Biol., 42, 198–201. doi: 10.1016/j.biocel.2009.09.015.
Rania, N., Ramzi, H., & Hébert, R. L. (2014) Chronic kidney disease: targeting prostaglandin E2 receptors. Am J Physiol Renal Physiol, 307, 243–250. doi: 10.1152/ajprenal.00224.2014.
Regner, K. R. (2012) Dual Role of Microsomal Prostaglandin E Synthase 1 in Chronic Kidney Disease. Hypertension, 59(1), 12–14. doi: 10.1161/HYPERTENSIONAHA.111.180034.
Ricciotti, E., & FitzGerald, G. A. (2011) Prostaglandins and Inflammation. Arterioscler Thromb Vasc Biol., 31(5), 986–1000. doi: 10.1161/ATVBAHA.110.207449.
Rooney Thompson, M., Towers, C. V., Howard, B. C., Hennessy, M. D., Wolfe, L., & Heitzman, C. (2015) The use of prostaglandin E1 in peripartum patients with asthma. Am J Obstet Gynecol, 212, 392.e1-3. doi: 10.1016/j.ajog.2014.11.042.
Samuelsson, B., Morgenstern, R., & Jakobsson, P. J. (2007) Membrane prostaglandin E synthase-1: a novel therapeutic target. Pharmacol Rev., 59, 207–24. doi: 10.1124/pr.59.3.1.
Satoh, H., Amagase, K., Ebara, S., Akiba, Y., & Takeuchi, K. (2013) Cyclooxygenase (COX)-1 and COX-2 both play an important role in the protection of the duodenal mucosa in cats. J. Pharmacol. Ther., 344(1), 189–195. doi: 10.1124/jpet.112.199182.
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
Основные закономерности метаболических процессов в организме человека. Часть 2.
Рассматривая обмен веществ в условиях нормального функционирования организма, следует остановиться на безусловно взаимосвязанных, но в то же время достаточно специфичных составляющих метаболизма, а именно на углеводном, белковом, липидном и водно-электролитном обмене.
Очевидно, что основная роль углеводов в метаболизме определяется их энергетической функцией. Именно глюкоза крови вследствие наличия простого и быстрого пути гликолитической диссимиляции и последующего окисления в цикле трикарбоновых кислот, а также возможности максимально быстрого извлечения ее из депо гликогена, обеспечивающей экстренную мобилизацию энергетических ресурсов, является наиболее востребованным источником энергии в организме. Использование циркулирующей в плазме глюкозы разными органами неодинаково: мозг задерживает 12% глюкозы, кишечник— 9%, мышцы — 7%, почки — 5%. При этом уровень глюкозы плазмы крови является одной из важнейших гомеостатических констант организма, составляя 3, 3—5, 5 ммоль/л. Как известно снижение уровня глюкозы ниже допустимого передела имеет своим незамедлительным следствием дискоординацию деятельности ЦНС, проявляющуюся соответствующей клинической симптоматикой: головной мозг содержит небольшие резервы углеводов и нуждается в постоянном поступлении глюкозы, поскольку энергетические расходы мозга покрываются исключительно за счет углеводов. Глюкоза в тканях мозга преимущественно окисляется, а небольшая часть ее превращается в молочную кислоту.
При полном отсутствии углеводов в пище они образуются в организме из продуктов трансформации жиров и белков. В печени возможно новообразование углеводов как из собственных продуктов их распада (пировиноградной или молочной кислоты), так и из продуктов диссимиляции жиров и белков (кетокислот и аминокислот), что обозначается как глюконеогенез. В результате трансформации аминокислот образуется пировиноградная кислота, при окислении жирных кислот — ацетилкоэнзим А, который может превращаться в пировиноградную кислоту — предшественник глюкозы. Это наиболее важный общий путь биосинтеза углеводов. Между двумя основными источниками энергии — углеводами и жирами — существует тесная физиологическая взаимосвязь. Повышение содержания глюкозы в крови увеличивает биосинтез триглицеридов и уменьшает распад жиров в жировой ткани. Поступление в кровь свободных жирных кислот уменьшается. В случае возникновения гипогликемии процесс синтеза триглицеридов тормозится, ускоряется распад жиров и в кровь в большом количестве поступают свободные жирные кислоты. Гликогенез, гликогенолиз и глюконеогенез являются тесно взаимосвязанными процессами, обеспечивающими оптимальный уровень глюкозы крови сообразно степени функционального напряжения организма.
Центральным звеном регуляции углеводного и других видов обмена и местом формирования сигналов, управляющих уровнем глюкозы, является гипоталамус. Отсюда регулирующие влияния реализуются вегетативными нервами и гуморальным путем, включающим эндокринные железы. Единственным гормоном, снижающим уровень гликемии, является инсулин — гормон, вырабатываемый β-клетками островков Ланхгерганса. Снижение гликемии происходит за счет усиления инсулином синтеза гликогена в печени и мышцах и повышения потребления глюкозы тканями организма. Увеличение уровня глюкозы в крови возникает при действии нескольких гормонов. Это глюкагон, продуцируемый α-клетками островков Ланхгерганса, адреналин — гормон мозгового слоя надпочечников, глюкокортикоиды — гормоны коркового слоя надпочечников, соматотропный гормон гипофиза, тироксин и трийодтиронин — гормоны щитовидной железы. Данные гормоны в связи с однонаправленностью их влияния на углеводный обмен и функциональным антагонизмом по отношению к эффектам инсулина часто объединяют понятием «контринсулярные гормоны».
Таким образом биологическая роль углеводов для организма человека определяется прежде всего их энергетической функцией. Обладая энергетической ценностью в 16, 7 кДж (4, 0 ккал) на 1 грамм вещества, углеводы являются основным источником энергии для всех клеток организма, при этом выполняя еще пластическую и опорную функции. Суточная потребность взрослого человека в углеводах составляет около 500 г.
— пластическая (структурная) функция заключается в том, что белки являются главной составной частью всех клеточных и межклеточных структур тканей;
— ферментная (каталитическая, энзимная) функция состоит в обеспечении всех химических реакций, протекающих в ходе обмена веществ в организме (дыхание, пищеварение, выделение), деятельностью ферментов, являющихся по своей структуре белками;
— транспортная функция белков заключается в их способности к соединению с целым рядом метаболитов и переносе последних в связанном состоянии в межтканевой жидкости и плазме крови к области их утилизации;
— защитная функция белков проявляется реализацией иммунного ответа образованием иммуноглобулинов (антител) и системы комплемента при поступлении в организм чужеродного белка, а также способностью к непосредственному связыванию экзогенных токсинов; белки системы гемостаза обеспечивают свертывание крови и остановку кровотечения при повреждении кровеносных сосудов;
— регуляторная функция, направленная на сохранение гомеостаза с поддержанием биологических констатнт организма, реализуется буферными свойствами молекулы протеинов, белковой структурой клеточных рецепторов, активируемых в свою очередь регуляторными полипептидами и гормонами, также имеющими белковую структуру;
— двигательная функция, обеспечивается взаимодействием сократительных белков мышечной ткани актина и миозина;
— энергетическая роль белков состоит в обеспечении организма энергией, образующейся при диссимиляции белковых молекул; при окислении 1 г белка в среднем освобождается энергия, равная 16, 7 кДж (4, 0 ккал).
При катаболизме почти все природные аминокислоты сначала передают аминогруппу на а-кетоглутарат в реакции трансаминирования с образованием глутамата и соответствующей кетокислоты. Затем глутамат подвергается прямому окислительному дезаминированию под действием глутаматдегидрогеназы, в результате чего получаются а-кетоглутарат и аммиак. При необходимости синтеза аминокислот и наличии необходимых а-кетокислот обе стадии непрямого дезаминирования протекают в обратном направлении. В результате восстановительного аминирования а-кетоглутарата образуется глутамат, который вступает в трансаминирование с соответствующей а-кетокислотой, что приводит к синтезу новой аминокислоты. В случае использования белков в качестве источника энергии большинство аминокислот окисляются в конечном счёте через цикл лимонной кислоты до углекислого газа и воды. Прежде, чем эти вещества вовлекаются в заключительный этап катаболизма, их углеродный скелет превращается в двухуглеродный фрагмент в форме ацетил-КоА. Именно в этой форме большая часть молекул аминокислот включается в цикл лимонной кислоты.
Таблица 1. 1. Аминокислоты, входящие в состав белков человека.
1. Незаменимые
2. Частично заменимые
3. Условно заменимые
4. Заменимые
Таблица 1. 2. Классификация липидов организма человека.
1. Гликолипиды.
Содержат углеводный компонент.
2. Жиры.
3. Минорные липиды.
4. Стероиды.
А. Стерины (спирты).
Наиболее важен холестерин.
В. Стериды.
Эфиры стеринов и высших жирных кислот. Наиболее распространены эфиры холестерина.
5. Фосфолипипы.
Одним из продуктов катаболизма жиров, имеющем важное значения для метаболизма в целом являются кетоновые тела. Кетоновые тела — группа органических соединений, являющихся промежуточными продуктами жирового, углеводного и белкового обменов. К кетоновым телам относят β-оксимасляную и ацетоуксусную кислоты и ацетон, имеющие сходное строение и способные к взаимопревращениям. Главным путем синтеза кетоновых тел, происходящего в основном в печени, считается реакция конденсации между двумя молекулами ацетил-КоА, образовавшегося при β-окислении жирных кислот или при окислительном декарбоксилировании пирувата (пировиноградной кислоты) в процессе обмена глюкозы и ряда аминокислот. Данный путь синтеза кетоновых тел более других зависит от характера питания и в большей степени страдает при патологических нарушениях обмена веществ. Из печени кетоновые тела поступают в кровь и с нею во все остальные органы и ткани, где они включаются в универсальный энергообразующий цикл — цикл трикарбоновых кислот, в котором окисляются до углекислоты и воды. Кетоновые тела используются также для синтеза холестерина, высших жирных кислот, фосфолипидов и заменимых аминокислот. При голодании, однообразном безуглеводистом питании и при недостаточной секреции инсулина использование ацетил-КоА в цикле трикарбоновых кислот подавляется, так как все метаболически доступные ресурсы организма превращаются в глюкозу крови. В этих условиях увеличивается синтез кетоновых тел. Следует подчеркнуть важную роль кетоновых тел в поддержании энергетического баланса. Кетоновые тела – поставщики «топлива» для мышц, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала.
Процесс образования, отложения и мобилизации из депо жира регулируется нервной и эндокринной системами, а также тканевыми механизмами и тесно связаны с углеводным обменом. Так, повышение концентрации глюкозы в крови уменьшает распад триглицеридов и активизирует их синтез. Понижение концентрации глюкозы в крови, наоборот, тормозит синтез триглицеридов и усиливает их расщепление. Таким образом, взаимосвязь жирового и углеводного обменов направлена на обеспечение энергетических потребностей организма. При избытке углеводов в пище триглицериды депонируются в жировой ткани, при нехватке углеводов происходит расщепление триглицеридов с образованием неэтерифицнрованных жирных кислот, служащих источником энергии. В обмене жиров одна из важнейших ролей принадлежит печени. Печень — основной орган, в котором происходит образование кетоновых тел (бета-оксимасляная, ацетоуксусная кислоты, ацетон), используемых как альтернативный глюкозе источник энергии.
Как указывалось выше метаболизм жиров контролируется нервной и эндокринной системами. Мобилизация жиров из депо происходит под влиянием гормонов мозгового слоя надпочечников — адреналина и норадреналина. Соматотропный гормон гипофиза также обладает жиромобилизирующим действием. Аналогично действует тироксин — гормон щитовидной железы. Тормозят мобилизацию жира глюкокортикоиды — гормоны коркового слоя надпочечника, вероятно, вследствие того, что они несколько повышают уровень глюкозы в крови. Действие инсулина связано с повышением активности внутриклеточной фосфодиэстеразы, что приводит к снижению концентрации цАМФ и угнетению липолиза. Таким образом, инсулин усиливает синтез жира и уменьшает скорость его мобилизации. Имеются данные, свидетельствующие о возможности прямых нервных влияний на обмен жиров. Симпатические влияния тормозят синтез триглицеридов и усиливают их распад. Парасимпатические влияния, напротив, способствуют отложению жира в депо.
Статья добавлена 31 мая 2016 г.